Biografia
Frederick Sanger nasce il 13 agosto del 1918 a Rendcombe, in Inghilterra ed è il secondo di tre figli. Il padre, anche lui di nome Frederick, è un medico, missionario e uomo molto religioso, e la madre Cicely, è la figlia di un ricco produttore di cotone. Sin da piccolo dimostra grande capacità nei lavori manuali, adora la pittura e la falegnameria. Dal 1932 al 1936 frequenta la Bryanston School, dove si appassiona alla biologia e alla chimica e successivamente viene ammesso al St John’s College di Cambridge.
Nonostante le difficoltà incontrate nel suo primo anno di università non si perde d’animo e si laurea nel 1939. Decide di proseguire lo studio della biochimica, a cui è molto appassionato, iscrivendosi ad un corso. Nel 1940 sposa Joan Howe, da cui ha tre figli, due maschi e una femmina.
Si distingue nel corso di biochimica e decide di proseguire su questa strada con un dottorato che consegue nel 1943 con una tesi dal titolo “Il metabolismo della lisina nel corpo animale”. Dopo il dottorato riceve il prestigioso premio Beit Memorial Fellowship for Medical Research e dal 1951 fino al 1983 è ricercatore presso il Medical Research Council.
A partire dal 1983 si ritira nella sua abitazione in una cittadina vicina a Cambridge e muore, all’età di 95 anni, il 19 novembre 2013.
FOCUS: L’invenzione del metodo di sequenziamento Sanger
Frederick Sanger entra nel gruppo di ricerca del biochimico Albert Chibnall, che in quel momento si occupava di studiare gli amminoacidi da cui era costituita l’insulina, l’ormone secreto dal pancreas che, a partire dal 1920, fu utilizzato per trattare il diabete.
La struttura dell’insulina e il primo Premio Nobel
Fu proprio Frederick Sanger a scoprire la struttura amminoacidica dell’insulina bovina (Figura 1) nel 1954. Grazie all’utilizzo della cromatografica di ripartizione e della cromatografia su carta, comprese come l’insulina fosse costituita da due catene polipeptidiche, tenute assieme da due ponti disolfuro. Da qui, passò all’identificazione degli amminoacidi di entrambe le catene: una di 21 amminoacidi e l’altra di 30. Questa scoperta gli ha permesso di ottenere il Premio Nobel per la chimica nel 1958.
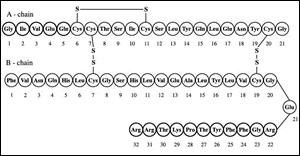
Continuò a studiare la struttura dell’insulina di differenti mammiferi e ne comparò i risultati. Tra il 1956 e il 1962, mise a punto delle procedure in grado di determinare la sequenza di proteine marcate in maniera radioattiva.
L’interesse per gli acidi nucleici e il secondo Premio Nobel
Nel 1958 decide di orientare le sue ricerche verso la biologia molecolare, per cui diviene ricercatore presso il The Medical Council Research Laboratory of Molecular Biology. Qui comincia ad interessarsi agli acidi nucleici e, in particolar modo, al sequenziamento dell’RNA con metodiche che sfruttano la radioattività. Nel 1967 viene sequenziato il primo RNA, seguito, nel 1969, da tRNA.
Nel 1970 i tempi sono maturi per passare al sequenziamento del DNA. Questa volta, però, mette a punto un nuovo metodo, basato sull’utilizzo di un gel di acrilammide. Questa metodica, che porta il suo nome, viene utilizzata per sequenziare il DNA a singolo filamento di un virus. Nel 1977, Sanger e il suo gruppo riescono a sequenziare il DNA del batteriofago ɸX174 (phi X174), il primo genoma in assoluto ad essere sequenziato (Figura 2). Tre anni dopo riceve il secondo Premio Nobel. Prima di ritirarsi nel 1983, si occupa di sequenziare il genoma mitocondriale umano e bovino.

Il sequenziamento Sanger
Frederick Sanger ha ideato un metodo di sequenziamento in grado di sequenziare gli acidi nucleici, dai più semplici ai più complessi. La metodica, comunemente nota con il nome di sequenziamento Sanger, prende il nome di metodo della terminazione della catena.
La tecnica consiste nell’utilizzo di dideossinucleotidi (ddNTP), che, rispetto ai normali deossinucleotidi (dNTP), presentano una modificazione a livello dello zucchero: mancano del gruppo ossidrile anche al 3′ (Figura 3). Questa loro particolare struttura impedisce la formazione di un legame fosfodiesterico e, quindi, il legame di un altro nucleotide. Di conseguenza una volta che legano una sequenza nucleotidica nascente, ne bloccano la sintesi.
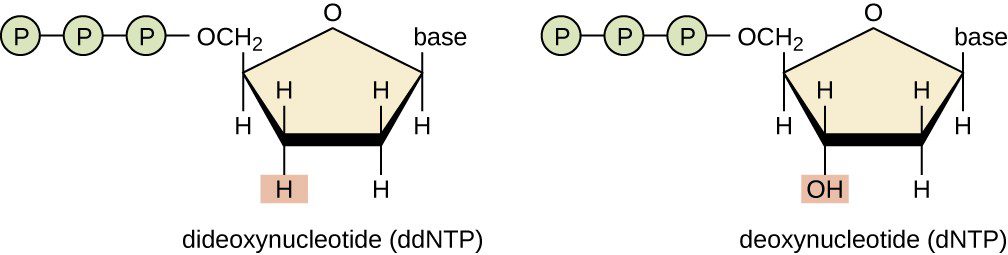
Il campione di partenza è un DNA a doppio filamento che viene denaturato, in modo tale da sfruttare l’azione della DNA polimerasi di utilizzare il filamento come stampo per sintetizzare il filamento complementare. Vengono effettuate in contemporanea quattro reazioni differenti, ciascuna delle quali contiene un primer di innesco, una DNA polimerasi e i quattro dNTP. La differenza tra le quattro reazioni sta nel ddNTP che viene aggiunto – in quantità stechiometricamente inferiori rispetto ai dNTP – a ciascuna reazione, che è stato opportunamente marcato. In questo modo quindi il filamento di nuova sintesi, complementare allo stampo, si allungherà incorporando i dNTP e si bloccherà quando verrà incorporato il ddNTP. In questo modo si creeranno frammenti di lunghezza differente, che saranno separati su un gel di poliacrilammide. Dall’osservazione delle differenti bande del gel si riuscirà a risalire alla sequenza nucleotidica (Figura 4).

Contributo scientifico
Il Progetto Genoma Umano
Il sequenziamento ideato da Sanger ha dato inizio all’Era Genomica e, in pochi anni sono stati raggiunti vari traguardi, come il sequenziamento di Haemophilus influenzae (1995) e di altri organismi molto utili nell’ambito della ricerca, fino ad arrivare al sequenziamento del genoma umano (2001).
Il Progetto Genoma Umano è stato avviato nel 1990 e ha visto l’impegno di tantissimi gruppi di ricerca internazionali (principalmente centri di ricerca di Stati Uniti, Regno Unito, Canada e Nuova Zelanda). La prima bozza del genoma si è avuta nel 2000 e il completamento della sequenza nel 2003. Questo grande successo ha permesso di compiere grandi passi in avanti in differenti ambiti, tra cui spicca quello biomedico. Ad oggi, infatti, poiché si riesce ad ottenere il genoma di un individuo in poco tempo, è possibile effettuare studi di variabilità genetica non solo tra individui, ma anche tra tessuti di uno stesso individuo, o, ancora, tra cellule sane e cellule tumorali.
Next Generation Seqeuncing (NGS)
Nonostante il sequenziamento Sanger abbia portato al sequenziamento dell’intero genoma umano, numerosi centri di ricerca si sono adoperati per migliorare quelli che sono i limiti di questa metodica di sequenziamento. Questo ha permesso lo sviluppo delle metodiche di Next Generation Sequencing (NGS), che raggruppa metodiche di seconda e terza generazione.
La differenza fondamentale rispetto al primo metodo di sequenziamento è l’high-troughput, cioè l’alta resa di queste metodiche, che permette di analizzare molte sequenze in parallelo. In questo modo non solo si sono ridotti i tempi di analisi, ma anche i costi. Per il Progetto Genoma Umano, infatti, sono stati investiti ben 100 milioni di dollari a fronte dei soli 1500, che ad oggi sono richiesti per il sequenziamento di un genoma umano. Il tutto in tempi ridotti rispetto ai 10 anni che ci sono voluti per ottenere il primo genoma umano.
Riconoscimenti
Frederick Sanger è la quarta persona nella storia ad aver ricevuto due volte il Premio Nobel: la prima volta nel 1958, grazie ai suoi studi sulla struttura delle proteine che l’hanno portato ad identificare la struttura dell’insulina bovina; la seconda volta nel 1980, assieme a Paul Berg e Walter Gilbert, per aver determinato la sequenza nucleotidica del DNA.
Grazie al suo straordinario lavoro nell’ambito della genetica e delle biotecnologie, ha ricevuto anche altri riconoscimenti:
- 1954: riceve il Fellowship of the Royal Society;
- 1963: diviene Commendatore dell’Ordine dell’Impero Britannico;
- 1969: riceve la Royal Society’s Royal Medal;
- 1977: riceve la Copley Medal;
- 1986: diviene Membro dell’Ordine al Merito del Regno Unito.
Nel 1992 il Wellcome Trust e il British Medical Research Council fondano il Sanger Centre (oggi Sanger Institute) in suo onore (Figura 5).

Fonti
- https://aulascienze.scuola.zanichelli.it/come-te-lo-spiego/2018/04/18/dal-metodo-sanger-a-oggi-40-anni-di-sequenziamento-del-dna/;
- Sanger, Frederick, Steven Nicklen, and Alan R. Coulson. “DNA sequencing with chain-terminating inhibitors.” Proceedings of the national academy of sciences 74.12 (1977): 5463-5467;
- https://it.wikipedia.org/;
- https://www.famousscientists.org/;