Generalità
La tubercolosi (TBC) è una malattia infettiva che ha come agente causale Mycobacterium tuberculosis. É caratterizzata da lesioni degenerative e necrotiche dei tessuti colpiti con formazione di granulomi tubercolari, entro i quali il micobatterio protetto prolifera. Il recente reinsorgere della tubercolosi nei Paesi industrializzati, dopo decenni durante i quali si pensava che questa infezione fosse stata debellata, ha portato nuovamente in primo piano il bisogno di nuovi agenti terapeutici e diagnostici antitubercolari. Molto allarmante è anche l’aumento dei casi di tubercolosi resistenti al trattamento con antibiotici, fenomeno noto come multidrug-resistant (MDR) tuberculosis.
La TBC è, ancora oggi, una delle principali minacce per la salute a livello mondiale. Nel 2016, l’Organizzazione mondiale della sanità (OMS) ha stimato che Mycobacterium tuberculosis abbia ucciso più persone di qualsiasi altro patogeno. Sono stati registrati, infatti, 10,4 milioni di casi di tubercolosi e 1,7 milioni di morti. A causa di questi preoccupanti numeri, l’OMS ha fissato l’obiettivo “END TBC” entro il 2035, riconoscendo che il successo dipende dallo sviluppo di migliori interventi preventivi, diagnostici e terapeutici.

La scelta della terapia farmacologica
La strategia terapeutica, a seguito di diagnosi di tubercolosi, varia a seconda delle caratteristiche del ceppo batterico responsabile dell’infezione e della malattia (ceppi sensibili o resistenti). Per questo motivo è importante eseguire un antibiogramma, cioè un test che indichi a quali farmaci è sensibile il bacillo della tubercolosi. Successivamente, una volta iniziata la terapia, questa deve essere articolata considerando anche la localizzazione intra/extracellulare del micobatterio e la presenza di patogeni nella sostanza caseosa del granuloma tubercolare, che rappresenta la tipica lesione tissutale associata alla malattia. Nel caso di una precoce identificazione dei casi infetti (seppur questa sia ostacolata da un lento ritmo di crescita del batterio), il trattamento con farmaci antitubercolari consente, in linea generale, di eradicare l’infezione.
La terapia antitubercolare dispone, ad oggi, di farmaci di “scelta primaria” e “scelta secondaria”, questi ultimi utili in associazione con i primi a motivo della loro più modesta attività. Un posto preminente tra gli antitubercolari di scelta primaria è occupato da un regime di trattamento combinato standard che comprende l’uso di isoniazide (INH), rifampicina (RIF), pirazinamide (PZA) ed etambutolo (EMB), seguiti subito dopo dalla streptomicina. In particolare, il trattamento standard per la tubercolosi prevede una fase intensiva con isoniazide e rifampicina, nonché pirazinamide ed etambutolo per due mesi, seguita da una fase di continuazione che comprende l’uso concomitante di isoniazide e rifampicina per ulteriori quattro mesi. Invece, tra i farmaci antitubercolari di seconda scelta ritroviamo: etionamide, cicloserina, acido p-aminosalicilico (PAS) e linezolid.
Il trattamento di infezioni tubercolari dura alcuni mesi e prevede che vengano combinati tra loro tre o quattro farmaci. L’associazione di più farmaci consente, infatti, di ridurre al minimo il rischio che si sviluppino dei ceppi resistenti.
Meccanismo d’azione
Ancora oggi per molti degli antibiotici antitubercolari si ignora l’esatto meccanismo di azione e ciò dimostra le enormi difficoltà in cui, all’inizio del terzo millennio, si muove la ricerca antitubercolare. Per poter analizzare più da vicino il modo in cui alcuni farmaci antitubercolari agiscono è opportuno conoscere soprattutto la composizione dell’involucro del micobatterio (Fig. 2):
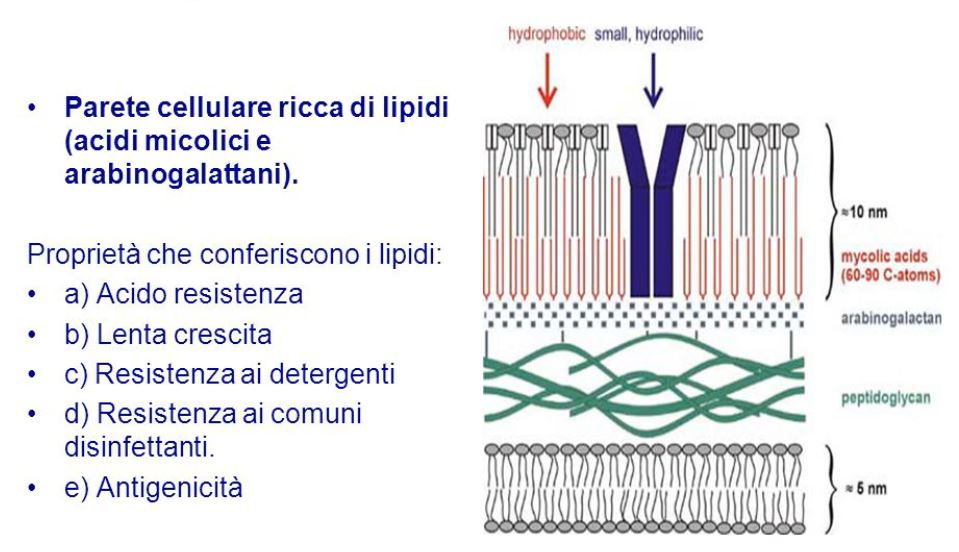
La maggior parte dei farmaci antimicobatterici hanno come bersaglio principale la biosintesi di uno o più costituenti della parete cellulare e questo porterà ad un danneggiamento della stessa. Conseguentemente, ciò determinerà o la morte o uno stato di quiescenza del batterio. Nello specifico possiamo associare a un determinato principio attivo il costituente della parete cellulare batterica su cui agisce:
- L’etanbutolo agisce sugli arabinogalattani;
- L’isoniazide è il principale inibitore della sintesi degli acidi micolici;
Principi attivi e loro farmacologia
Gli antibiotici antitubercolari si possono classificare in base alla loro azione. Parliamo, infatti, di battericidi quando sono capaci di colpire il batterio in fase replicativa attiva, causandone la morte. Facciamo riferimento, invece, ai batteriostatici quando colpiscono il batterio a metabolismo rallentato in condizioni di poca ossigenazione, ricordando quindi che si tratta di un bacillo aerobio obbligato. Inoltre, è importante ricordare che alla categoria dei farmaci antitubercolari appartengono sia alcuni antibiotici (rifampicina, streptomicina) che alcuni farmaci di sintesi (isoniazide, etanbutolo, pirazinamide). Tra i farmaci citati è possibile differenziare la diversa attività:
- L’isoniazide inibisce la biosintesi degli acidi micolici: all’interno del M. tuberculosis, INH viene convertita in un radicale isonicotinoilico ad opera di una catalasi-perossidasi (KatG). Nella forma radicalica si combina con il NAD+ presente al sito attivo di due enzimi NADH dipendenti che sono coinvolti nella biosintesi degli acidi micolici, componente essenziale per la sintesi della parete batterica. L’isoniazide possiede azione battericida quando il micobatterio della tubercolosi è in fase di crescita mentre, nella fase di riposo del bacillo, ha effetti batteriostatici;
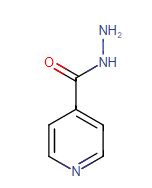
- L’etanbutolo porta ad inibizione dell’enzima arabinosiltrasferasi, coinvolto nella biosintesi della dell’arabinogalattano: è un tubercolostatico attivo sui micobatteri resistenti alla isoniazide e alla streptomicina, e in ciò consiste il suo particolare valore clinico;
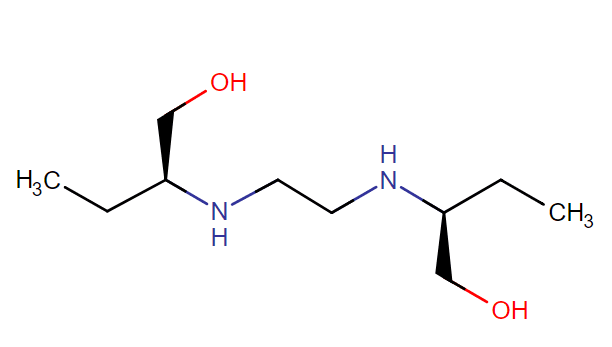
- La rifampicina inibisce la sintesi dell’RNA DNA-dipendente interferendo con la RNA-polimerasi batterica ed è attiva verso il micobatterio nello stato intracellulare ed extracellulare;
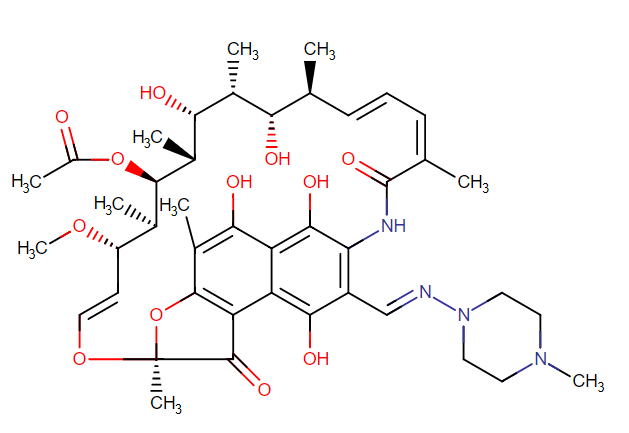
- La pirazinamide viene convertita nel corrispondente acido dal micobatterio portando ad interferenza con la catena di trasporto degli elettroni nel mitocondrio e nella biosintesi degli acidi grassi: possiede attività batteriostatica ed è battericida verso i micobatteri che si replicano attivamente (stato intracellulare del micobatterio);
Tra i farmaci di scelta secondaria l’acido p-aminosalicilico è quello più conosciuto e studiato. E’ un analogo dell’acido p-aminobenzoico (PAB), nei confronti del quale esercita azione competitiva nella biosintesi dell’acido folico. Fu fondamentale la constatazione che la crescita del bacillo di Koch era influenzata positivamente dalla presenza degli acidi benzoico o salicilico. Ciò indusse i ricercatori a sintetizzare derivati dell’acido salicilico simili al PAB per usarli come antimetaboliti nei riguardi del micobatterio tubercolare.
Tossicità ed effetti indesiderati
L’epatotossicità, una delle reazioni avverse più comuni e importanti, è associata ai tre più importanti farmaci di prima linea: isoniazide, rifampicina e pirazinamide. É un fenomeno più frequentemente correlato alla dose (solo alcuni casi sono causati da ipersensibilità ai farmaci) e varia dall’aumento asintomatico degli enzimi epatici all’insufficienza epatica fulminante. Il danno epatico indotto da farmaci anti-TB (DILI anti-TB) porta ad un aumento della morbilità e della mortalità.
Pertanto, può comportare l’interruzione del trattamento, la sostituzione del farmaco, l’aggiustamento del regime posologico, la non aderenza e la resistenza ai farmaci. È stato riportato che l’incidenza complessiva di DILI anti-TB varia dal 5% al 33% e il meccanismo rimane, ancora oggi, poco chiaro. Se volessimo fare un esempio tra tutti, l’isoniazide provoca epatotossicità attraverso l’aumento dello stress ossidativo, la generazione di specie reattive dell’ossigeno (ROS) e la perossidazione lipidica.
Al di là di questa comune caratteristica di alcuni degli antibiotici antitubercolari, c’è da considerare anche le possibili reazioni avverse specifiche di ogni farmaco. Ad esempio INH ha tra le reazioni avverse: eruzioni cutanee, febbre e raramente neurotossicità. EMB, invece, può causare neurite ottica data da complessazione con Zn. Infine, per quanto riguarda il farmaco di seconda scelta cicloserina, c’è la possibilità che si presenti sonnolenza, confusione o addirittura paralisi.
Resistenza antibiotica
L’emergenza globale della resistenza antimicrobica rappresenta una sfida importante e a questa non sfugge nemmeno il Mycobacterium tuberculosis. Ad oggi, nonostante la richiesta di accesso universale ai test di suscettibilità ai farmaci per terapie personalizzate dirette, i costi elevati e la carenza in molti paesi delle adeguate competenze fa sì che solo il 22% di circa 600.000 pazienti che necessitano di un trattamento per la tubercolosi multiresistente venga diagnosticato e trattato (dati del 2016 ottenuti da linee guida della WHO), facilitando la trasmissione successiva di ceppi multiresistenti.
Se da una parte il regime di trattamento standard di 6 mesi è altamente efficace per la tubercolosi suscettibile ai farmaci, dall’altra l’uso di più antibiotici per lunghi periodi di tempo può causare una resistenza ai farmaci con conseguenti rischi di fallimento del trattamento. Ad oggi, queste caratteristiche hanno permesso di classificare i farmaci più adatti per il trattamento della tubercolosi polmonare multiresistente, nota con la sigla Mdr-Tb. I ceppi batterici più soggetti al fenomeno della resistenza, invece, sono noti come Xdr-Tb. Questi, infatti, risultano resistenti a isoniazide, rifampicina, pirazinamide, etambutolo, fluorochinoloni e farmaci antitubercolari iniettabili come l’amikacina e la kanamicina.
Attualmente, sono in studio nuove molecole per il trattamento della turbercolosi multiresistente e negli ultimi anni sono stati introdotti sul mercato la bedaquilina e il delamanid. In particolare, la prima agisce inibendo la pompa protonica dell’enzima ATP sintasi, necessario al batterio della tubercolosi per ottenere energia. La seconda, blocca la sintesi dell’acido metossi-micolico e dell’acido keto-micolico (due componenti essenziali della parete batterica del bacillo di Koch) determinando la morte del microrganismo.
Il monitoraggio terapeutico del farmaco (TDM) potrebbe ridurre l’incidenza di reazioni avverse all’antimicrobico e aumentare la probabilità di successo del trattamento.
Fonti
- Antonelli, Clementi, Pozzi, Rossolini- Principi di Microbiologia Medica; Ed. Ambrosiana (terza edizione 2017)
- Lina Tao, Xiaoyu Qu , Yue Zhang , Yanqing Song , Si-Xi Zhang. (2019 Jan 10) Prophylactic Therapy of Silymarin (Milk Thistle) on Antituberculosis Drug-Induced Liver Injury: A Meta-Analysis of Randomized Controlled Trials; NCBI
- Rihwa Choi, M.D., Byeong-Ho Jeong, M.D., Won-Jung Koh, M.D., and Soo-Youn Lee, M.D. (2016 Dec 20) Recommendations for Optimizing Tuberculosis Treatment: Therapeutic Drug Monitoring, Pharmacogenetics, and Nutritional Status Considerations; NCBI
- http://www.salute.gov.it/imgs/C_17_opuscoliPoster_183_allegato.pdf
- https://www.pharmamedix.com/patologiavoce.php?pat=Tubercolosi&vo=Farmaci+e+terapie
- https://docplayer.it/22942083-Farmaci-antimicobatterici.html