Introduzione
Negli anni Ottanta, un medico della Marina imperiale giapponese, Takaki Kanehiro, osservò per la prima volta la correlazione tra una malattia chiamata beri beri e un’alimentazione a base di riso brillato. Il consumo di questo riso, privo del rivestimento esterno, era infatti tipico dei paesi asiatici e in particolar modo tipico della popolazione più povera che non poteva permettersi di mangiare carne. Questa ultima osservazione portò a pensare che la mancanza di proteine fosse la causa alla base del beri beri, credenza che continuò per molti anni, fino al 1912. In questo anno uno scienziato tedesco, Casmir Funk, basandosi su un articolo di Umetaro Suzuki, individuò per la prima volta la vera molecola incriminata, che chiamò “vitamina”, ovvero amina vitale. La vitamina in questione era la tiamina, o vitamina B1: non trovandosi essa nel riso brillato e non potendo essere sintetizzata nel nostro corpo, la sua mancanza causava la malattia.
La tiamina è stata dunque la prima vitamina ad essere scoperta, ed è anche il precursore della molecola che esamineremo in questo articolo: la tiamina pirofosfato (TPP).
Struttura molecolare
La tiamina pirofosfato (TPP) è il coenzima derivante dalla tiamina e differisce da essa per la sola presenza di due gruppi fosfato legati ad un gruppo etilico.
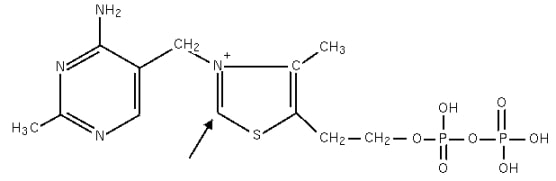
Come mostrato nella Figura 2, la tiamina pirofosfato, e dunque anche la tiamina, consta di due anelli, uno pirimidinico e uno tiazolico, legati insieme attraverso un ponte metilenico.
L’unico centro attivo della molecola è però l’anello tiazolico. Esso possiede infatti un carbonio, situato tra un atomo di azoto e uno di zolfo, particolarmente acido, che tende quindi a perdere un protone caricandosi negativamente.
Funzioni biologiche
La tiamina pirofosfato è, come detto, un coenzima: partecipa cioè alle reazioni chimiche come “aiutante” dell’enzima. In particolare, le reazioni a cui prende parte fanno parte del catabolismo dei carboidrati e sono reazioni di:
- Decarbossilazione degli α-chetoacidi
- Trasferimento di un gruppo chetolico
In entrambi i casi il carbonio C-2, carico negativamente, opera un attacco nucleofilo al carbonio carbonilico, il quale, legato con l’ossigeno, rappresenta l’elettrofilo.

Un esempio di decarbossilazione è quella operata dalla piruvato decarbossilasi, enzima che nella fermentazione alcolica trasforma il piruvato in acetaldeide.
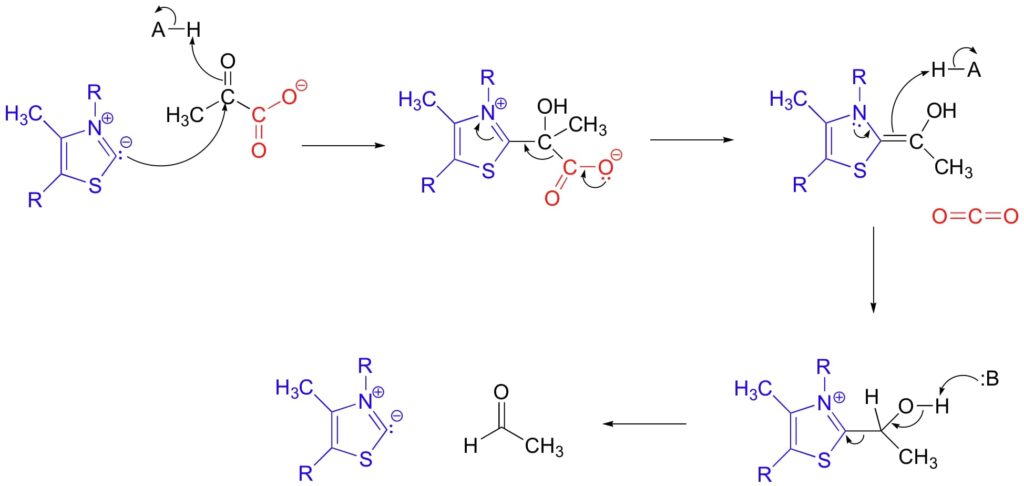
Come mostrato nella figura 4, l’intermedio che si forma dall’attacco nucleofilo perde il gruppo carbossilico sotto forma di anidride carbonica. Questa eliminazione viene favorita dalla stabilizzazione per risonanza data dalla presenza dell’anello tiazolico, il quale si comporta da trappola per gli elettroni.
L’ultima tappa prevede infine la scissione dell’acetaldeide tramite ri-protonazione.
La tiamina pirofosfato a questo punto viene liberata e può partecipare ad un’altra reazione del catabolismo
Nella via dei pentosio fosfati la tiamina pirofosfato svolge invece un altro compito. Nella reazione che vede il trasferimento di un’unita bicaboniosa dallo xilosio 5-fosfato ad un secondo zucchero, interviene l’enzima transchetolasi, il quale agisce mediante TPP. Analogamente a prima, si crea un intermedio covalente a seguito di un attacco nucleofilo, ma questa volta a staccarsi non è più l’anidride carbonica ma bensì uno zucchero.

Via biosintetica
La sintesi della tiamina pirofosfato avviene a partire dalla tiamina o vitamina B1, che però non può essere né sintetizzata né immagazzinata all’interno del nostro organismo. Possiamo dunque considerare come primo step della formazione di TPP, l’assunzione di tiamina tramite la dieta. In particolare, tra gli alimenti ricchi di tiamina troviamo i piselli, i fagioli, le lenticchie, i lieviti e le carni.
Una volta arrivata nel tratto gastrointestinale, la tiamina deve essere assorbita dalle cellule dell’intestino tenue. L’assorbimento può avvenire o mediante trasporto attivo, quando ci troviamo a basse concentrazioni, oppure mediante diffusione passiva, ad alte concentrazione. Ad interferire con l’assorbimento concorrono due fattori: assunzione di alcol, in quanto l’etanolo altera un corretto assorbimento, e la presenza di tiaminasi, enzima che demolisce la tiamina nei suoi due anelli costitutivi.
Una volta arrivati all’interno delle cellule, la sintesi di TPP avviene nel citosol mediante reazione con ATP. In particolare, l’enzima tiamina pirofosfochinasi trasferisce i gruppi fosfato alla tiamina producendo AMP e tiamina pirofosfato.
Immagini



Fonti
- Donald Voet, Judith G. Voet, Charlotte W. Pratt – Principi di biochimica – ed. Zanichelli
- https://it.wikipedia.org/wiki/Vitamine#Storia
- https://en.wikipedia.org/wiki/Thiamine_pyrophosphate
I commenti sono chiusi.