Plasminogeno: un enzima umano
Il plasminogeno è una proteina tipicamente presente nel sangue umano. Si tratta di una molecola formata da sette domini (Fig.1): i cinque principali, che compongono il “corpo” della proteina sono detti Kringle, mentre alle due estremità opposte della catena troviamo il dominio terminale N PAp (dall’inglese Pan Apple domain) e il terminale C serina proteasi, fondamentale per la funzione del plasminogeno.
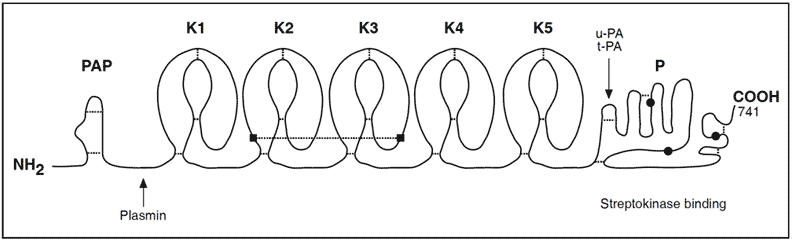
Figura 1 – struttura del plasminogeno
Nella sua forma inattiva, la struttura della proteina è “chiusa”, non in grado di svolgere azione enzimatica. Dopodiché, grazie al legame con specifici attivatori (es: gli enzimi tPA o uPA, ma anche la fibrina che agisce da co-attivatore) il plasminogeno assume un cambio di conformazione, aprendosi e quindi diventando l’enzima attivo plasmina. Essa svolge una funzione fondamentale nel sistema circolatorio: degradare proteine del sangue, principalmente la fibrina, essenziale componente di coaguli e trombi.
NET: la trappola antibatterica
E quindi come può la plasmina essere coinvolta nella protezione di batteri patogeni dal nostro stesso sistema immunitario? Partiamo dal principio: uno dei migliori strumenti antimicrobici presenti nel corpo umano sono le NET (Neutrophil Extracellular Trap). Esse sono letteralmente dei network, o reti in italiano, composte da materiale extracellulare tra cui fibre, DNA, proteine globulari ed istoni. Sono prodotte dalle cellule neutrofileed il loro obbiettivo è catturare ed abbattere patogeni.

Figura 2 – struttura della NET
L’efficacia delle NET è determinata soprattutto dagli istoni che ne fanno parte. Queste molecole infatti, oltre ad essere pilastri della struttura del nostro DNA, a livello extracellulare sono presenti numerosi tra i filamenti delle NET, e quasi tutti (in particolar modo H2A, H2B ed H3) svolgono una potente attività antibatterica, data la loro capacità di distruggere sia la parete cellulare di batteri Gram-positivi sia la membrana esterna nei Gram-negativi.
Il meccanismo di difesa di streptococchi e stafilococchi tramite plasminogeno
Tra le varie proteine processate dalla plasmina vi sono inclusi gli istoni extracellulari. Diversi studi hanno dimostrato come alcuni batteri patogeni, tra cui Streptococcus pyogenes e Staphylococcus aureus, siano in grado di legare il plasminogeno, attivare il cambio di conformazione in plasmina e mantenervisi ancorati, mentre l’enzima degrada gli istoni extracellulari salvaguardando quindi l’incolumità del batterio.
Queste specie possiedono infatti un impressionante arsenale di proteine ancorate alla parete cellulare, comunemente denominate CWA (Cell Wall Anchored proteins) le quali svolgono svariate funzioni. Alcune di esse, come ad esempio le FnBPs (Fibronectin Binding Proteins) riescono a legarsi a proteine umane come fibronectina, fibrinogeno e plasminogeno, portandole sulla superficie batterica.
A quel punto il plasminogeno può essere accostato ad un attivatore espresso dal batterio, streptochinasi nel caso di S. pyogenes o stafilochinasi nel caso di S. aureus : queste proteine “imitano” gli attivatori naturali del plasminogeno come tPA, permettendogli di assumere la conformazione enzimatica della plasmina pur rimanendo ancorato alla superficie del batterio tramite le altre CWA. Grazie a ciò questi patogeni sopravvivono alla presenza di istoni extracellulari nell’ambiente circostante e possono, sempre grazie all’azione degradante del plasminogeno, spostarsi attraverso i coaguli di sangue.
L’importanza delle CWA
Tali studi confermano l’importanza delle proteine CWA per la sopravvivenza di queste specie una volta invaso il nostro organismo. Di fatti si può dedurre che, nella battaglia farmacologica contro batteri patogeni, specialmente per quanto riguarda specie dotate di altissima adattabilità contro gli antibiotici (es: ceppi di S. aureus meticillina-resistenti) queste proteine di superficie potrebbero essere target ideali per la creazione di nuovi farmaci in grado di inibire l’avanzata di questi organismi nell’infezione e proliferazione nel corpo umano.
Bibliografia
- J Innate Immun. 2016;8(6):589-600. Epub 2016 Aug 18. “Streptococcus pyogenes Escapes Killing from Extracellular Histones through Plasminogen Binding and Activation by Streptokinase.” Nitzsche R, Köhler J, Kreikemeyer B, Oehmcke-Hecht S.
- J Biol Chem. 2019 Mar 8;294(10):3588-3602. doi: 10.1074/jbc.RA118.005707. Epub 2019 Jan 8. “Fibronectin-binding protein B (FnBPB) from Staphylococcus aureus protects against the antimicrobial activity of histones.” Pietrocola G, Nobile G, Alfeo MJ, Foster TJ, Geoghegan JA, De Filippis V, Speziale P.
- The Journal of Immunology. “Neutrophil Extracellular Traps: Double-Edged Swords of Innate Immunity”. Mariana J. Kaplan and Marko RadicJ Immunol September 15, 2012, 189 (6) 2689-2695; DOI: https://doi.org/10.4049/jimmunol.1201719