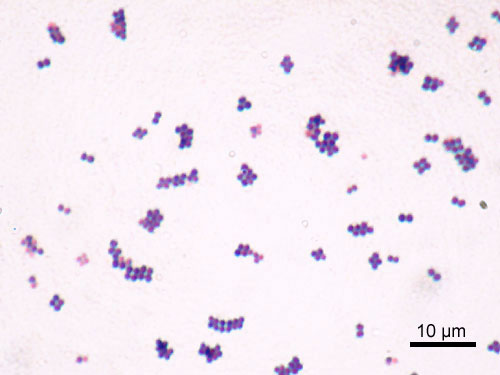
Quando la parete cellulare diventa impenetrabile
Negli anni ’50 del secolo scorso, mentre gli stafilococchi iniziavano a sviluppare resistenza alla penicillina, i ricercatori della Eli Lilly isolarono da campioni di terreno del Borneo un composto prodotto da Amycolatopsis orientalis (allora classificato come Streptomyces orientalis). Lo chiamarono vancomicina, dal termine “vanquish” (sconfiggere), perché sembrava in grado di sconfiggere anche i batteri più resistenti. All’epoca fu considerata troppo tossica e relegata a farmaco di seconda scelta. Sessant’anni dopo, con l’emergenza globale di Staphylococcus aureus meticillino-resistente (MRSA) e enterococchi vancomicina-resistenti (VRE), vancomicina e teicoplanina hanno assunto un ruolo centrale nella lotta contro i Gram-positivi.
I glicopeptidi rappresentano una classe di antibiotici strutturalmente complessi, composti da peptidi glicosilati con peso molecolare elevato (circa 1.500 Da). Oltre alla vancomicina, il rappresentante clinicamente più rilevante è la teicoplanina, isolata da Actinoplanes teichomyceticus e approvata in Europa negli anni ’80. Entrambi agiscono sulla sintesi della parete cellulare batterica, ma con un meccanismo radicalmente diverso rispetto ai beta-lattamici: invece di inibire gli enzimi che costruiscono il peptidoglicano, si legano direttamente ai precursori peptidici impedendone l’incorporazione nella parete.
Questa differenza meccanicistica spiega perché i glicopeptidi rimangono efficaci contro batteri resistenti ai beta-lattamici. Un batterio MRSA che produce PBP2a con bassa affinità per la meticillina è completamente sensibile alla vancomicina, perché questa non ha bisogno di legarsi alle PBP per funzionare. Ma l’evoluzione batterica non si ferma mai, e anche contro i glicopeptidi stanno emergendo meccanismi di resistenza sofisticati che minacciano di erodere l’efficacia di questi antibiotici di ultima linea.
Il meccanismo molecolare: abbracciare il nemico
Per comprendere come funzionano i glicopeptidi bisogna prima capire come viene costruita la parete batterica. Il peptidoglicano è un polimero tridimensionale formato da catene di zuccheri (N-acetilglucosamina e acido N-acetilmuramico) interconnesse da ponti peptidici. La sintesi avviene attraverso precursori chiamati lipidi II, molecole costituite da un carrier lipidico ancorato alla membrana citoplasmatica che trasporta un’unità disaccaride-pentapeptide destinata a essere aggiunta alla parete in crescita.
La vancomicina è una molecola rigida, a forma di coppa, con una cavità idrofobica centrale. Questa cavità è perfettamente complementare alla sequenza D-Ala-D-Ala presente all’estremità del pentapeptide del lipide II. La vancomicina abbraccia letteralmente questo dipeptide terminale formando cinque legami idrogeno estremamente stabili, come una mano che stringe un oggetto. Questo legame impedisce alle transpeptidasi (le PBP) di accedere al substrato per catalizzare la cross-linkage tra catene peptidiche adiacenti.
Il risultato è una parete cellulare strutturalmente debole, incapace di sopportare la pressione osmotica interna. Le nuove unità di peptidoglicano vengono sintetizzate ma non possono essere incorporate correttamente nella rete tridimensionale. Il batterio tenta di crescere, la parete cede sotto la pressione, e la cellula va incontro a lisi osmotica. È un’azione battericida lenta ma inesorabile, particolarmente efficace contro batteri Gram-positivi in fase di crescita attiva.
La teicoplanina condivide lo stesso meccanismo di base ma presenta differenze strutturali importanti. Possiede una catena lipidica che le conferisce maggiore affinità per la membrana citoplasmamica e un’emivita plasmatica molto più lunga (circa 70-100 ore contro 4-6 ore della vancomicina). Questo permette somministrazione una volta al giorno dopo dosi di carico, migliorando l’aderenza terapeutica e riducendo la necessità di accessi venosi multipli. Inoltre, la teicoplanina può essere somministrata per via intramuscolare, opzione non disponibile per la vancomicina a causa della grave irritazione locale che causerebbe.
Quando la resistenza riscrive le regole: VRE, VISA e VRSA
La resistenza ai glicopeptidi è emersa prima negli enterococchi, poi negli stafilococchi, attraverso meccanismi molecolari affascinanti e preoccupanti.
VRE
Gli enterococchi vancomicina-resistenti (VRE) sono stati identificati per la prima volta in Europa nel 1988, appena tre anni dopo l’introduzione della vancomicina per via endovenosa come standard terapeutico. Il meccanismo principale coinvolge cluster genici van che codificano per enzimi capaci di modificare il target della vancomicina. Invece di terminare il pentapeptide con D-Ala-D-Ala (l’obiettivo perfetto per la vancomicina), i batteri resistenti sostituiscono l’ultima D-alanina con D-lattato (D-Lac) o D-serina (D-Ser), producendo precursori D-Ala-D-Lac o D-Ala-D-Ser.
Questo cambiamento apparentemente minuscolo, la sostituzione di un singolo atomo di azoto con ossigeno, riduce l’affinità di legame della vancomicina di circa 1.000 volte. La struttura rigida della vancomicina non riesce più a formare legami idrogeno stabili con il target modificato. Esistono diversi fenotipi di resistenza van, classificati da VanA a VanN, ciascuno con profilo di resistenza e trasferibilità diversi. VanA e VanB sono i più diffusi clinicamente: VanA conferisce resistenza elevata sia a vancomicina che a teicoplanina, mentre VanB conferisce resistenza variabile a vancomicina ma mantiene sensibilità a teicoplanina.
VRSA
La situazione è ancora più preoccupante perché i geni van sono spesso localizzati su elementi genetici mobili (plasmidi e trasposoni) che possono trasferirsi orizzontalmente tra batteri. Nel 2002 è stato documentato il primo caso di Staphylococcus aureus vancomicina-resistente (VRSA) negli Stati Uniti, in un paziente coinvolto con VRE. L’analisi genomica ha confermato che lo stafilococco aveva acquisito il cluster genico VanA dall’enterococco attraverso trasferimento genico orizzontale. Fortunatamente, VRSA rimane estremamente raro (meno di 20 casi documentati globalmente fino al 2024), probabilmente perché il trasferimento plasmidico tra enterococchi e stafilococchi è inefficiente e il fitness dei ceppi VRSA è ridotto.
VISA
Più insidiosi sono gli stafilococchi con sensibilità intermedia alla vancomicina (VISA) e gli stafilococchi eteroresistenti (hVISA). Questi ceppi non hanno acquisito i geni van ma hanno sviluppato resistenza attraverso ispessimento progressivo della parete cellulare. La parete diventa più spessa (fino a 2-3 volte il normale), con maggiore quantità di peptidoglicano non cross-linkato che presenta terminazioni D-Ala-D-Ala libere. Queste terminazioni libere fungono da “esche molecolari”, legando molecole di vancomicina e impedendo loro di raggiungere la membrana citoplasmatica dove avviene la sintesi attiva di parete. È una resistenza per sequestro, non per modifica del target.
I ceppi hVISA sono particolarmente problematici perché contengono sottopopolazioni resistenti non rilevabili dai metodi di routine di laboratorio (MIC formalmente sensibile, < 2 μg/mL) ma che possono espandersi durante la terapia con vancomicina, portando a fallimento clinico. La prevalenza di hVISA tra isolati MRSA varia dal 5% al 50% a seconda delle popolazioni studiate e dei metodi di rilevazione, rappresentando una minaccia silenziosa non adeguatamente monitorata.
Vancomicina orale: l’arma contro Clostridioides difficile
Mentre per la maggior parte delle infezioni sistemiche la vancomicina viene somministrata per via endovenosa, esiste un’applicazione clinica specifica che richiede somministrazione orale: l’infezione da Clostridioides difficile (CDI). C. difficile è un batterio anaerobio sporigeno che colonizza il colon quando la flora intestinale normale viene alterata da antibiotici ad ampio spettro. Produce tossine (TcdA e TcdB) che causano diarrea acquosa profusa, colite pseudomembranosa, megacolon tossico e potenzialmente morte. L’incidenza di CDI è aumentata drammaticamente negli ultimi vent’anni, con l’emergenza di ceppi ipervirulenti come NAP1/BI/027 che producono quantità maggiori di tossine e sono associati a outcome clinici peggiori.
La vancomicina somministrata per via orale non viene assorbita a livello gastrointestinale, rimanendo concentrata nel lume intestinale dove raggiunge livelli straordinariamente elevati (circa 500-1.000 μg/g di feci). Questo la rende ideale per eradicare C. difficile direttamente nel sito dell’infezione. La dose standard è 125 mg quattro volte al giorno per 10 giorni per episodi lievi-moderati, fino a 500 mg quattro volte al giorno per forme severe o complicate.
Studi clinici
Gli studi clinici hanno dimostrato che la vancomicina orale è superiore al metronidazolo (precedente standard terapeutico) in termini di risoluzione clinica, particolarmente nelle infezioni severe. Il trial randomizzato controllato di Zar et al. ha documentato tassi di guarigione del 81% con vancomicina versus 73% con metronidazolo (p=0.02), con differenza ancora più marcata nei casi severi (97% vs 76%, p=0.001). Per questo motivo, le linee guida internazionali raccomandano vancomicina orale come terapia di prima linea per CDI, riservando metronidazolo solo a infezioni non severe in contesti con risorse limitate.
Un problema significativo è la ricorrenza post-trattamento, che si verifica nel 15-35% dei pazienti entro 8 settimane dalla fine della terapia. Le ricorrenze sono generalmente causate da germinazione di spore sopravvissute (contro cui né vancomicina né metronidazolo sono efficaci) o da reinfezione con nuovo ceppo. Strategie per ridurre le ricorrenze includono regimi di tapering e pulsing della vancomicina, utilizzo di fidaxomicina (antibiotico più recente con minore impatto sul microbioma), trapianto di microbiota fecale per ricorrenze multiple, e anticorpi monoclonali antitossine (bezlotoxumab).
Monitoraggio terapeutico e nefrotossicità: sul filo del rasoio
La vancomicina presenta una finestra terapeutica stretta, il che significa che la differenza tra concentrazioni efficaci e concentrazioni tossiche è relativamente piccola. Questo rende essenziale il monitoraggio terapeutico del farmaco (TDM, therapeutic drug monitoring) per ottimizzare l’efficacia e minimizzare la tossicità.
Tradizionalmente, il TDM della vancomicina si basava sulla misurazione dei livelli di trough (concentrazione minima pre-dose), con target di 10-20 μg/mL per la maggior parte delle infezioni. Per infezioni severe come endocarditi, osteomieliti, meningiti e batteriemie complicate, si raccomandavano livelli di trough più elevati (15-20 μg/mL) per massimizzare la probabilità di successo clinico. Tuttavia, studi successivi hanno dimostrato che livelli di trough elevati sono associati a rischio significativamente aumentato di nefrotossicità senza chiaro beneficio clinico addizionale.
Le linee guida aggiornate del 2020 pubblicate congiuntamente da ASHP, IDSA, PIDS e SIDP raccomandano un approccio basato sull’area sotto la curva (AUC) piuttosto che sui soli livelli di trough. Il target farmacocinamico ottimale è un rapporto AUC₂₄/MIC ≥ 400-600, calcolato utilizzando modelli bayesiani che integrano livelli plasmatici misurati con parametri farmacocinetici del paziente. Questo approccio richiede software specializzati ma promette migliore predizione dell’efficacia e riduzione della tossicità rispetto al semplice monitoraggio di trough.
Nefrotossicità
La nefrotossicità rappresenta la principale tossicità dose-limitante della vancomicina, manifestandosi come danno tubulare acuto (ATN) con aumento della creatinina sierica. L’incidenza varia ampiamente negli studi (5-43%) a seconda delle definizioni utilizzate, delle popolazioni studiate e dei fattori di rischio concomitanti. Il meccanismo coinvolge accumulo del farmaco nelle cellule del tubulo prossimale, stress ossidativo mitocondriale, disfunzione lisosomiale e apoptosi.
I fattori di rischio per nefrotossicità includono livelli di trough elevati (> 20 μg/mL), durata prolungata della terapia (> 7 giorni), uso concomitante di altri farmaci nefrotossici (aminoglicosidi, FANS, mezzo di contrasto iodato, piperacillina-tazobactam), età avanzata, obesità, malattia renale preesistente, stato critico, ipovolemia. La combinazione di vancomicina e piperacillina-tazobactam è particolarmente problematica, con meta-analisi che documentano rischio di nefrotossicità circa 3 volte superiore rispetto a vancomicina combinata con altri beta-lattamici.
La buona notizia è che la nefrotossicità da vancomicina è generalmente reversibile dopo sospensione del farmaco, con recupero completo della funzionalità renale nella maggioranza dei casi. Il monitoraggio richiede dosaggio della creatinina sierica almeno 2-3 volte a settimana durante la terapia, con calcolo della clearance o della eGFR per aggiustamenti posologici tempestivi.
La teicoplanina presenta un profilo di nefrotossicità significativamente più favorevole rispetto alla vancomicina, con incidenze riportate inferiori al 2-5% anche con terapie prolungate. Questo, combinato con la comodità della somministrazione una volta al giorno, rende la teicoplanina un’alternativa attraente quando disponibile, sebbene l’esperienza clinica sia meno estesa rispetto alla vancomicina e il costo possa essere superiore. I glicopeptidi incarnano il paradosso della terapia antimicrobica moderna: antibiotici potenti, salvavita, indispensabili contro patogeni multiresistenti, ma con finestra terapeutica stretta, necessità di monitoraggio attento, tossicità significativa e resistenza emergente.
Conclusioni su vancomicina e teicoplanina
La vancomicina, “l’antibiotico che non volevamo usare” negli anni ’50, è diventata “l’antibiotico che non possiamo permetterci di perdere” nel 2026. Ogni prescrizione richiede considerazione attenta di indicazione, dosaggio, monitoraggio, durata. Ogni giorno di utilizzo inappropriato è un giorno che avvicina l’era in cui anche questi farmaci di ultima linea smetteranno di funzionare.
Fonti
- Levine DP. Vancomycin: a history. Clin Infect Dis. 2006;42 Suppl 1:S5-12. doi:10.1086/491709
- Patel S, Preuss CV, Bernice F. Vancomycin. [Updated 2023]. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2024. Available from: https://www.ncbi.nlm.nih.gov/books/NBK459263/
- Liu C, Bayer A, Cosgrove SE, et al. Clinical practice guidelines by the Infectious Diseases Society of America for the treatment of methicillin-resistant Staphylococcus aureus infections in adults and children. Clin Infect Dis. 2011;52(3):e18-e55. doi:10.1093/cid/ciq146
- Svetitsky S, Leibovici L, Paul M. Comparative efficacy and safety of vancomycin versus teicoplanin: systematic review and meta-analysis. Antimicrob Agents Chemother. 2009;53(10):4069-4079. doi:10.1128/AAC.00341-09
- Kahne D, Leimkuhler C, Lu W, Walsh C. Glycopeptide and lipoglycopeptide antibiotics. Chem Rev. 2005;105(2):425-448. doi:10.1021/cr030103a
- Appelbaum PC. The emergence of vancomycin-intermediate and vancomycin-resistant Staphylococcus aureus. Clin Microbiol Infect. 2006;12 Suppl 1:16-23. doi:10.1111/j.1469-0691.2006.01344.x
- Cetinkaya Y, Falk P, Mayhall CG. Vancomycin-resistant enterococci. Clin Microbiol Rev. 2000;13(4):686-707. doi:10.1128/CMR.13.4.686
- Howden BP, Davies JK, Johnson PD, Stinear TP, Grayson ML. Reduced vancomycin susceptibility in Staphylococcus aureus, including vancomycin-intermediate and heterogeneous vancomycin-intermediate strains: resistance mechanisms, laboratory detection, and clinical implications. Clin Microbiol Rev. 2010;23(1):99-139. doi:10.1128/CMR.00042-09
- Barna JC, Williams DH. The structure and mode of action of glycopeptide antibiotics of the vancomycin group. Annu Rev Microbiol. 1984;38:339-357. doi:10.1146/annurev.mi.38.100184.002011
- Wood MJ. The comparative efficacy and safety of teicoplanin and vancomycin. J Antimicrob Chemother. 1996;37(2):209-222. doi:10.1093/jac/37.2.209
- Arthur M, Courvalin P. Genetics and mechanisms of glycopeptide resistance in enterococci. Antimicrob Agents Chemother. 1993;37(8):1563-1571. doi:10.1128/AAC.37.8.1563
- Courvalin P. Vancomycin resistance in gram-positive cocci. Clin Infect Dis. 2006;42 Suppl 1:S25-34. doi:10.1086/491711
- Chang S, Sievert DM, Hageman JC, et al. Infection with vancomycin-resistant Staphylococcus aureus containing the vanA resistance gene. N Engl J Med. 2003;348(14):1342-1347. doi:10.1056/NEJMoa025025
- Hiramatsu K, Aritaka N, Hanaki H, et al. Dissemination in Japanese hospitals of strains of Staphylococcus aureus heterogeneously resistant to vancomycin. Lancet. 1997;350(9092):1670-1673. doi:10.1016/S0140-6736(97)07324-8
- van Hal SJ, Paterson DL. Systematic review and meta-analysis of the significance of heterogeneous vancomycin-intermediate Staphylococcus aureus isolates. Antimicrob Agents Chemother. 2011;55(2):405-410. doi:10.1128/AAC.01133-10
- Leffler DA, Lamont JT. Clostridium difficile infection. N Engl J Med. 2015;372(16):1539-1548. doi:10.1056/NEJMra1403772
- McDonald LC, Gerding DN, Johnson S, et al. Clinical Practice Guidelines for Clostridium difficile Infection in Adults and Children: 2017 Update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA). Clin Infect Dis. 2018;66(7):e1-e48. doi:10.1093/cid/cix1085
Crediti immagini
- Immagine in evidenza: https://www.repstatic.it/content/contenthub/img/2020/09/11/004648514–a0d1eb39-65fd-472e-ac1d-c671af4e9b9b.jpg
- Figura 1: https://it.wikipedia.org/wiki/File:Staphylococcus_aureus_Gram.jpg