Il monitoraggio ambientale per la gestione del ceppo microbico
La flora batterica normalmente presente nell’ambiente può essere causa di contaminazione del prodotto farmaceutico. I microorganismi batterici si possono suddividere nelle seguenti classi:
| Forma | Descrizione |
| Cocchi | Sferica, sferoidale |
| Bacilli | Bastoncini |
| Vibrioni | Bastoncini incurvati a virgola |
| Spirilli | Forma a spirale |
| Spirochete | Forma a spirale sottili e filamentosi |
| Attinomiceti | Forme Filamentose |
Il microbiota ambientale è in continuo sviluppo poiché ogni evento che si sviluppa nei reparti di produzione o in laboratorio può farla variare (ad esempio l’inserimento di un nuovo operatore modificherà la flora batterica introducendo quella presente sull’operatore). Per questo motivo è molto importante che i metodi di analisi siano in grado di rilevarla per poter controllare gli effetti sugli intermedi di sintesi e sul prodotto finito.
Sviluppare un approccio logico da seguire per ottenere l’identificazione dei microorganismi che possono essere rinvenuti sui campioni analitici è di fondamentale importanza. Questo si può ottenere utilizzando le caratteristiche fenotipiche dei microorganismi, inoltre è molto utile mappare ed indentificare la normale contaminazione batterica al fine di utilizzarla per rafforzare il giudizio di Growth Promotion test dei terreni di coltura utilizzati per il controllo microbiologico.
Mappa microbica per la gestione del ceppo nel monitoraggio ambientale
Per prima cosa si procede con una fase iniziale di raccolta e sommaria classificazione dei microorganismi rilevati durante il routinario monitoraggio ambientale, si va cioè a creare una mappa microbiologica. Questa mappa verrà poi integrata con una classificazione per rappresentatività delle varie specie isolate. Questo passaggio servirà per scegliere i microorganismi prevalenti, di questi ne verranno scelti un numero deciso dal team del laboratorio di microbiologia e questi verranno identificati mediante valutazioni fenotipiche a livello di genere e specie; i laboratori più attrezzati bypassano le metodiche di identificazioni più classiche utilizzando dei sistemi strumentali di identificazione microbiologica. I microorganismi verranno a questo punto inseriti nel test di Growth Promotion insieme a quelli di farmacopea.
Per eseguire l’identificazione di un microorganismo si possono seguire le seguenti fasi:
- Aspetto della colonia su piastra
- Isolamento dei vari stipiti evidenziati
- Visione microscopica
- Reazioni biochimiche ed enzimatiche.
Aspetto delle colonie su piastra
La verifica dell’aspetto è la prima osservazione che viene effettuata; infatti le colonie possono avere dimensioni, forme e colore diverse a seconda della specie e del terreno che viene utilizzato. In figura 1 alcuni esempi di aspetti morfologici di colonie:
Figura 1 – Aspetti morfologici di colonie per la gestione del ceppo nel monitoraggio ambientale
Isolamento dei vari stipiti
Una volta evidenziato la varietà dei microorganismi presenti sulla piastra, bisogna procedere all’isolamento in colture pure per non avere risultati errati nei test che seguiranno. Per fare ciò si preleva la colonia di interesse con un’ansa sterile, si sospende la colonia in soluzione fisiologica.
Poi con un’altra ansa sterile si preleva una goccia di sospensione e si piastra su opportuno terreno con movimenti regolari. Dopo questa operazione si mette la piastra ad incubare alla temperatura di crescita ottimale (30°-35°) per 24 – 48 ore. Ogni colonia che si svilupperà sarà una colonia pura, e ognuna di esse verrà trapiantata in TSA per le forme batteriche e SDA per i miceti. In questo modo si avrà una quantità sufficiente per effettuare tutti i test che seguiranno.

Visione microscopica
Questa fase permette una rapida classificazione in base alla loro morfologia. Per l’esame a fresco si stempera una piccolissima quantità di ceppo sul vetrino su cui è stata depositata una goccia di soluzione fisiologica. Si copre con il vetrino copri oggetti e si osserva al microscopio a contrasto di fase a 400 ingrandimenti.
Reazioni biochimiche ed enzimatiche
Di seguito i principali test :
| Test del Gram | Test alternativo al Gram (KOH) |
| Ossidazione/Fermentazione del glucosio | Mobilità |
| Citocromo Ossidasi | Tipo respiratorio |
| Catalasi | ——————- |
Test del Gram: L’esame si basa sulla colorazione delle cellule con un colorante basico e lavaggio con un mordenzante per favorire la penetrazione del colore nella struttura che deve essere colorata. Successivamente il materiale organico viene lavato con una soluzione decolorante.
I batteri Gram + trattengono il colorante basico, mentre i Gram – rimangono rosso grigiastri, privi di colorazione.
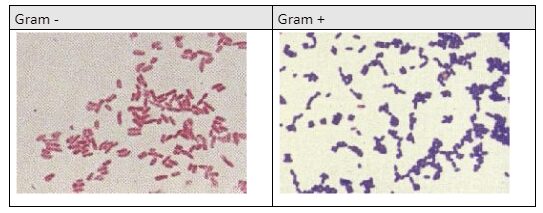
La differenza nella capacità di trattenere il colorante basico è data dalla diversa composizione della parete cellulare, molto spessa nei Gram positivi che fissa il Crystal violetto della colorazione e non permette la sua eliminazione con l’etanolo a differenza dei Gram negativi i quali hanno una parete più sottile.
Test alternativo al Gram (KOH): mescolare un’ansata di KOH 3% con un’ansata dalla colonia. I Gram negativi saponificano diventando viscosi e filanti, i Gram positivo no.
Ossidazione/Fermentazione del glucosio: basato sull’utilizzo del glucosio il quale libera come prodotto di reazione quantità di acido che vengono rivelate da un indicatore. Preparare due fiale di API-OF contenenti un supporto agarizzato al glucosio e indicatore, ricostituendole mediante bollitura per cinque minuti e successivo raffreddamento. Con una bacchetta di plastica sterile si preleva una piccolissima quantità di ceppo da testare e si seminano per infissione le due fiale. Ricoprire una delle due fiale con paraffina liquida per assicurare l’anaerobiosi, è necessaria per verificare l’utilizzo del glucosio per via fermentativa, incubare a 30° – 35° per 24h. Dopo l’incubazione osservare le fiale; un viraggio al giallo dell’indicatore indica reazione positiva.
Si possono ottenere i seguenti risultati:
- OF-O negativo /inerte/alcalino
- OF-O positivo
- OF-O positivo
- OF-F negativo
- OF-F negativo
- OF-F positivo
Citocromo Ossidasi: il test deve essere effettuato su una coltura fresca di non più di 24h. Preparare una sospensione concentrata di ceppo test stemperando con un’ansa in 0,2 ml di Acqua sterile o soluzione fisiologica in una provetta. Aggiungere tre gocce di reattivo per Ossidasi e agitare delicatamente. La reazione positiva è evidenziata dalla formazione di colore blu entro i primi tre minuti.
Con la combinazione dei test precedenti è possibile già avere alcune importanti informazioni sul tipo di specie corrispondenti.

Catalasi: la catalasi è un enzima, prodotto da microrganismi che vivono in ambienti ossigenati per neutralizzare le forme tossiche di metaboliti dell’ossigeno, H2O2, che viene scisso in 2H2O + O2. L’enzima catalasi neutralizza gli effetti battericidi del perossido di idrogeno creando una resistenza. Gli anaerobi generalmente non possiedono l’enzima catalasi. La catalasi libera ossigeno gassoso in presenza di H2O2. Preparare una sospensione concentrata di ceppo test stemperando con un’ansa in 2 ml di Acqua sterile o soluzione fisiologica in una provetta sterile. Aggiungere 2 – 3 gocce di H2O2 (acqua ossigenata) 30% fresca; non agitare. La formazione di bolle di O2 evidenzia la positività del test.
Mobilità: inoculare il ceppo test per infissione, con una bacchetta di plastica sterile, i primi 5 – 8 mm di una provetta contente un TSA allo 0,3 % di agar e incubare a 30° – 35° C per 24h. La mobilità eventuale viene evidenziata dalla formazione di filamenti di crescita microbica che si dipartono dalla zona inoculata o con crescita diffusa in tutto il terreno.
Tipo respiratorio: inoculare il ceppo test per infissione, con una bacchetta di plastica sterile, con un movimento elicoidale dal basso verso l’alto una provetta contente un TSA fuso a circa 40 °C. Dopo l’inoculo raffreddare immediatamente in posizione verticale e incubare a 30 – 35 °C per 24h.
Il tipo di respirazione viene verificata nel seguente modo:

Per i microorganismi anaerobi il test può essere eseguito utilizzando un terreno al Tioglicolato, ideale per la loro crescita, con l’aggiunta del 3% di Agar.
Identificazione
Una volta stabilito il genere appartenente al microorganismo ignoto, per determinarne la specie è necessario procedere con una serie di test biochimici/enzimatici più specifici. Per questo scopo si può utilizzare indifferentemente due tecniche: metodo fenotipico semiautomatico o un metodo manuale come ad esempio le gallerie pronte costituite da una serie di tubi contenenti substrati specifici per il genere ricercato.
I risultati ottenuti vengono interpretati in due modi: i sistemi semiautomatici forniscono direttamente un report in cui sono riportate le percentuali di probabilità del riconoscimento del microorganismo; le gallerie manuali sono corredate di un software che analizza il codice numerico ottenuto dalla lettura e produrrà come risultato una percentuale di probabilità di riconoscimento. Da prassi si considera valido un risultato maggiore all’80%.
Una volta che si è creata una mappa del microbiota ambientale e sulla base del monitoraggio ambientale vengono scelti i microorganismi più rappresentativi (questa viene dettata dalla frequenza di ritrovamento). Questi microorganismi diventato a tutti gli effetti degli standard di riferimento per le analisi del laboratorio di microbiologia.
La delicatezza di questi standard impone precauzioni particolari per non alterarne le caratteristiche o al limite perdita di vitalità. La conservazione avviene in provette contenenti glicerolo e terreno di coltura e poste in congelatore a -18 °C per un tempo limitato di circa qualche mese. Al momento d’uso le provette verranno rivitalizzate a bagnomaria a 30 °C fino al loro scioglimento, verrà effettuato un trapianto a fresco su terreno idoneo ed incubato alla temperatura idonea per 18-24h e questa brodocoltura sarà il nuovo standard di lavoro.
Fonti
- Farmacopea Europea
- Farmacopea US
- Microbiologia-Cristina Paglia, Giunti ed.
- Microbiologia industriale-Matilde Manzoni, CEA
- SOP aziendali