Acidimicrobium sp. A6 è il primo batterio in grado di scindere il legame C-F dei composti perfluorurati
La chimica dei composti composti perfluorurati
I fluorocarburi (Fig. 1), composti perfluorurati a volte detti perfluorocarburi (PFC), sono composti chimici formati soltanto da atomi di fluoro (F) e carbonio (C).

Figura 1 – Struttura chimica dei fluorocarburi
Il legame carbonio-fluoro è il più forte legame singolo in chimica organica. Di conseguenza i fluorocarburi che contengono solo legami singoli (fluoroalcani) hanno una stabilità termica e un’inerzia chimica maggiore dei corrispondenti alcani, e trovano svariate applicazioni come: agenti di finissaggio per tessuti, componenti di agenti antincendio, bagni galvanici, oli lubrificanti e trasportatori di ossigeno per ricerche sulla respirazione liquida.
I fluorocarburi liquidi sono incolori. Hanno densità elevata, fino ad oltre il doppio dell’acqua, a causa del loro elevato peso molecolare.
Reattività e tossicità
I fluoroalcani hanno però lo svantaggio di essere potenti gas serra, per cui rappresentano un importante inquinante ambientale di cui limitare assolutamente le emissioni. La loro pericolosità è data dalla loro scarsa reattività chimica che li rende immuni ai più comuni processi di biodegradazione.
Fortunatamente, i fluorocarburi contenenti doppi o tripli legami (fluoroalcheni e fluoroalchini) sono invece più reattivi dei corrispondenti idrocarburi, grazie alle loro insaturazioni, per cui sono spesso usati come reagenti in processi industriali.
Pochi esseri viventi usano legami C-F. Uno di questi è il batterio Gram-positivo Streptomyces cattleya (Fig. 2) in grado di produrre la 4-fluoro-L-treonina, un metabolita coinvolto nella biosintesi dell’amminoacido L-treonina.
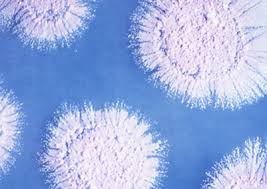
Figura 2 – Colonie batteriche della specie Streptomyces cattleya
L’enzima capace di costruire un legame C-F si chiama adenosil-fluoruro sintasi o fluorinasi ed è l’unico conosciuto fino ad oggi.
Al contrario della natura, la chimica del legame C-F non ha fermato l’uomo dal sintetizzare un elevato numero di composti basati su questo legame, a causa della loro stabilità e delle proprietà speciali che questo legame conferisce alle molecole che ne sono dotate.
In particolare, molecole con tutti i legami saturati dal fluoro sono estremamente idrofobiche e tendono ad avere una bassissima coesione, per cui appaiono come cere amorfe, se di grande dimensioni di catena, oppure come liquidi, stabili per lungo tempo e con elevate tensioni di vapore.
La somma di queste proprietà li ha portati a dominare certi settori: polimeri perfluorurati come il teflon, PTFE, liquidi perfluorurati come alcuni tipi di freon, utili nei circuiti frigoriferi o per scacciare l’acqua da mezzi porosi (ma estremamente tossici), rivestimenti antiaderenti o anti-bagnatura e cere da sci più performanti.
Tuttavia, la stabilità di queste catene perfluorurate o parzialmente fluorurate è tale solo in certe condizioni: la presenza di eteroatomi (per esempio l’idrogeno) e l’effetto dei raggi ultravioletti o di un forte riscaldamento porta ad una loro decadenza nel tempo. Questo fenomeno ha contribuito al cosiddetto buco dell’ozono.
Inoltre, l’ingestione di tali composti da parte dell’uomo comporta seri rischi per la sua salute come documentato da alcuni episodi del passato in Italia, precisamente in Veneto, e in Usa, a causa dello sversamento nella falda idrica di reflui industriali, rispettivamente dell’azienda Miteni e Dupont.
Finora nessuno aveva trovato il modo di risolvere il problema dell’accumulo di perfluorurati nel suolo e nelle acque. Come è possibile depurare l’ambiente da queste molecole così “estranee” alla biosfera?
La scoperta storica casuale
Uno studio di settembre 2019, descritto sulla rivista internazionale Environmental Science and Technology, ha dimostrato che il batterio Acidimicrobium sp. A6 (Fig. 3) è in grado di metabolizzare il fluoro organicato sfruttando reazioni di ossido-riduzione.

Figura 3 – Fotografia di una piastra Petri contenente uno striscio di Acidimicrobium sp.
L’ossidazione di idrogeno e ammoniaca cede elettroni ad uno ione ferro, che si riduce passando da Fe3+ a Fe2+, ed un composto perfluorurato. La riduzione del composto organico genera la scissione del legame C-F con conseguente liberazione di uno ione fluoruro (F–).
Tuttavia, la ricerca degli autori di tale studio mirava alla scoperta di nuovi meccanismi di degradazione dell’ammoniaca presente nei terreni umidi del New Jersey, mirando ad utilizzare classi di batteri in grado di attuare il processo naturale di ossidazione dell’ammonio chiamato Feammox. Infatti, dopo parecchi anni di lavoro il team di scienziati è stato in grado di isolare l’Acidimicrobium A6.
La svolta della loro scoperta è stata la sostituzione di un elettrodo di ferro come accettore di elettroni al fine di poter agire anche su terreni poveri di ferro. Nello svolgere le prove di questa ipotesi si resero conto della possibilità di biodegradare materiali clorurati. Lo step finale è stato la dimostrazione del successo di tale approccio anche per la degradazione dei composti perclorurati e perfluorurati.
Prima della loro scoperta l’uso di alcune specie del genere Pseudomonas aveva portato ad un risultato apparentemente simile ma senza la produzione di ione fluoruro, dunque senza l’eliminazione del fluoro organico.
Invece ad oggi, per la prima volta, abbiamo davanti la possibilità di estrarre un sistema enzimatico da questa specie batterica e attivare artificialmente reazioni in grado di attaccare il legame C-F.
Tale scoperta rappresenta una grande speranza per lo sviluppo di future tecnologie in grado di abbattere l’inquinamento ambientale dovuto ai composti perfluorurati.
Nicola Di Fidio
Sitografia
- Claudio Della Volpe (settembre 2019, La Chimica e la Società). Un enzima che degrada il legame C-F!. Estrapolato da: https://ilblogdellasci.wordpress.com/2019/09/30/un-enzima-che-degrada-il-legame-c-f/
- Wikipedia, l’enciclopedia libera (settembre 2019). Fluorocarburi. Estrapolato da: https://it.wikipedia.org/wiki/Fluorocarburi
Bibliografia
- Huang, S., & Jaffé, P. R. (2019). Defluorination of Perfluorooctanoic Acid (PFOA) and Perfluorooctane Sulfonate (PFOS) by Acidimicrobium sp. Strain A6. Environmental science & technology.
Crediti immagini
- Huang, S., & Jaffé, P. R. (2019). Defluorination of Perfluorooctanoic Acid (PFOA) and Perfluorooctane Sulfonate (PFOS) by Acidimicrobium sp. Strain A6. Environmental science & technology. https://pubs.acs.org/doi/full/10.1021/acs.est.9b04047
- https://en.wikipedia.org/wiki/Fluorocarbon
- http://www.actino.jp/DigitalAtlas/subwin.cgi?target=8-8
- https://www.researchgate.net/publication/271626425_Isolation_and_Characterization_of_Novel_Iron-Oxidizing_Autotrophic_and_Mixotrophic_Bacteria_from_Boiling_Springs_Lake_an_Oligotrophic_Acidic_Geothermal_Habitat/figures?lo=1