L’elettrochimica è quella branca della chimica che si occupa dei processi che coinvolgono il trasferimento di elettroni tramite un circuito elettrico esterno e non per scambio diretto come per le reazioni di ossidoriduzione (definite comunemente redox). Essa tratta quindi le trasformazioni chimiche prodotte dal passaggio di elettricità in determinati sistemi chimici e la produzione/immagazzinamento di elettricità per mezzo di trasformazioni chimiche.
La bioelettrochimica è una branca dell’elettrochimica che studia il trasporto di carica, il potenziale di membrana e le reazioni elettrochimiche che riguardano gli enzimi redox. In generale, un sistema bioelettrochimico (SBE) è un tipo di bioreattore in cui possono essere eseguiti contemporaneamente processi biologici e processi elettrochimici per generare elettricità, idrogeno o altri prodotti di interesse.
Da un punto di vista storico, i primi studi nel campo della bioelettrochimica risalgono al 1902 con il fisiologo tedesco Julius Bernstein, il quale svolse indagini sulla differenza di potenziale determinata dalla differenza di concentrazione degli ioni in corrispondenza delle pareti di una membrana cellulare. Tuttavia, nel corso del XX secolo i campi di applicazione della bioelettrochimica si sono moltiplicati, estendendosi anche a quelli di medicina, biosensori e, più recentemente, persino al campo della chimica delle fermentazioni.
Infatti, l’elettro-fermentazione (EF) è una nuova tipologia di processo biotecnologico basato sul controllo elettrochimico del metabolismo fermentativo dei microrganismi mediante l’ausilio di elettrodi. Quest’ultimi possono agire come dissipatori oppure come fonte di elettroni, alterando la normale fermentazione. Inoltre, possono modificare le caratteristiche elettrochimiche del terreno di coltura cambiando il bilancio redox.
Tale controllo elettrochimico esercita effetti significativi non solo sul metabolismo microbico e sulla regolazione cellulare, ma anche sulle interazioni inter-specie e sulla selezione di popolazioni batteriche in colture miste.
In questo contesto, un nuovo tipo di BES è stato recentemente proposto come nuovo mezzo per controllare e stabilizzare il processo di fermentazione, con la possibilità di superare i limiti metabolici delle reazioni bilanciate. Infatti, i processi di fermentazione sono comunemente usati per produrre diversi tipi di molecole solubili (ad esempio alcoli o acidi carbossilici), a volte con rilascio concomitante di un biogas contenente idrogeno e/o metano. Le fermentazioni sono effettuate da una grande varietà di microrganismi, in colture pure o miste, che possono utilizzare una vasta gamma di substrati, compresi i rifiuti organici. I principali parametri che influenzano i percorsi fermentativi includono la composizione del terreno, il pH, la temperatura, la velocità di agitazione, la pressione parziale dell’ossigeno, l’accumulo di prodotti finali e/o tossici.
A tutti questi parametri va ad aggiungersi un altro molto importante ma meno conosciuto rappresentato dal potenziale di ossido-riduzione (oxidation–reduction potential, ORP) del brodo di coltura, noto anche come ORP extracellulare. Esso è un parametro rilevante che controlla il metabolismo microbico in quanto un processo di fermentazione corrisponde ad una cascata di reazioni di ossido-riduzione che devono essere mantenute in equilibrio. Sebbene queste reazioni siano per lo più termodinamicamente favorevoli e spontanee, sono anche vincolate da regole biologiche all’interno dei microorganismi ed in interazioni inter-specie. Nello stesso modo in cui il pH è una misura dell’attività protonica, l’ORP extracellulare corrisponde all’attività degli elettroni presenti nel mezzo. Esso è principalmente influenzato dalla temperatura, dalla composizione chimica del brodo e dal grado di riduzione dei metaboliti prodotti dalla fermentazione. Può essere facilmente misurato con un sensore ORP situato nel mezzo. L’ORP extracellulare è particolarmente importante perché può successivamente influenzare l’ORP intracellulare attraverso il bilancio NAD ridotto/ossidato (NADH/NAD+). L’ORP intracellulare, che rappresenta lo stato redox all’interno di una cellula, può essere stimato dal rapporto NADH/NAD+ a causa dell’omeostasi redox intracellulare. È noto che tale rapporto controlla l’espressione genica e la sintesi degli enzimi, influenzando così l’intero processo biochimico e metabolico della cellula. Il controllo chimico dell’ORP extracellulare è già stato implementato con successo per migliorare la produzione di metaboliti come il succinato o l’1,3-propandiolo. In questo contesto, i BES possono essere usati per modificare l’ORP extracellulare fornendo o raccogliendo energia sotto forma di corrente elettrica attraverso l’uso di elettrodi, in un processo noto appunto come elettro-fermentazione (Fig. 1).
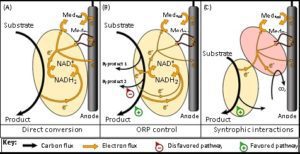
Negli ultimi anni sono stati scoperti tantissimi nuovi batteri elettro-attivi così come tante nuove interazioni specifiche inter-specie. Ciò apre la strada a funzioni metaboliche non ancora note da esplorare e descrivere. Ne deriva un campo di ricerca ampio ed entusiasmante per la messa a punto di nuovi e migliorati processi di elettro-fermentazione utilizzando un’ampia varietà di substrati, catalizzatori microbici e prodotti di interesse ad alto valore aggiunto.
Nicola Di Fidio
Sitografia
Bibliografia
- Roman Moscoviz, Javiera Toledo-Alarcón, Eric Trably, and Nicolas Bernet. Electro-Fermentation: How To Drive Fermentation Using Electrochemical Systems. Trends in Biotechnology, DOI: http://dx.doi.org/10.1016/j.tibtech.2016.04.009. In Press.
Crediti immagini
- http://www.ansa.it/canale_scienza_tecnica/notizie/biotech/2018/09/12/i-batteri-dellintestino-producono-elettricita-_74936201-0d6e-4595-b126-f2755da27610.html
- Roman Moscoviz, Javiera Toledo-Alarcón, Eric Trably, and Nicolas Bernet. Electro-Fermentation: How To Drive Fermentation Using Electrochemical Systems. Trends in Biotechnology, DOI: http://dx.doi.org/10.1016/j.tibtech.2016.04.009. In Press.