Lo chiamano cross-feeding e rappresenta una mutua convenienza tra stipiti batterici diversi che condividono lo stesso spazio vitale. Ma è anche molto più di questo. Spesso, è l’unico spazio di manovra per uscire dal terrifico stato infiammatorio acuto e cronico che brucia il nostro intestino, e le sue irrinunciabili funzioni. Il Faecalibacterium prausnitzii, però, è un eroe fragile. I suoi benefìci spuntano solo in una particolare, vincente abbinata.
Dai disordini alle sindromi infiammatorie
Sotto il tetto delle Patologie Infiammatorie Intestinali (Inflammatory Bowel Disease, IBD) riparano molteplici gradazioni disfunzionali dell’intero tratto digerente: morbo di Crohn e coliti ulcerose, le portabandiera di uno stato d’allarme ormai a sirene spiegate.
Qui, vige già uno stato infiammatorio cronico ed un danno tissutale distale, fino a livello dell’ileo e del colon (Figura 1). E la patogenesi viene ascritta tanto a predisposizione genetica quanto a stimoli ambientali. Stimoli, poi. Le nostre brutte abitudini. E già. L’occidentalizzazione dei canoni alimentari. Con il che si intende la predominanza di alimenti follemente elaborati, dalla astronomica densità calorica e dal valore nutritivo nullo. Anzi negativo, dal momento che alcuni di questi alimenti sottraggono e sperperano le nostre stesse risorse minerali e vitaminiche. Chi non dona nulla al nostro metabolismo, pesa anche, col proprio smaltimento, sulle piccole essenziali riserve esistenti. Magari, alla prossima pizza con doppia mozzarella e farcitura di affettati e patatine, ci si pensa un secondo in più.

Fonte immagine: https://www.lnage.it/assorbimento-intestinale-funzioni-intestino/villi-intestinali/
Ma prima che tutto precipiti nel patologico, c’è un allarme, a dire il vero sempre meno ignorato, che si definisce disbiosi. Già seria alterazione della composizione microbica locale, può tuttavia reclamare ed ottenere una rapida risoluzione della prima debolezza di barriera. Scongiurando esiti peggiori. D’altronde, poiché studi paralleli, sull’uso sempre più regolare di farmaci antinfiammatori ammettono ripercussioni collaterali anche in questi profondi distretti, è bene ormai riporre ogni speranza nell’impiego terapeutico mirato di batteri probiotici ad hoc.
Dove c’è salute c’è Faecalibacterium
Tra i principali ceppi commensali dell’intestino umano, il Faecalibacterium prausnitzii produce acidi grassi a catena corta che rappresentano l’ambrosia per i colonociti. Garantiscono funzionalità e forza di reazione, in caso di improvvise invasioni microbiche o di altre alterazioni. Purtroppo, però, il batterio risulta altamente sensibile all’ossigeno e questo lo bolla come difficile da impiegare in formule probiotiche. Tutto ciò, ha spinto un gruppo di ricerca, condotto da Heejung Kim, a documentare fattori e condizioni di crescita di tale stipite batterico ed ottenerne, così, ugualmente, un incremento endogeno, seppure per via indiretta.
Faecalibacterium prausnitzii (Figura 2) fa parte del cluster IV di Clostridium, nel phylum dei Firmicutes ed è uno dei più abbondanti ceppi residenti commensali del tratto digerente, in adulti sani. Uno studio recente conferma la sua peculiare capacità antinfiammatoria sia in vitro che in vivo. Addirittura, secondo Daniela Parada Venegas ed il suo gruppo di ricerca, il ceppo batterico, scarso in soggetti affetti da IBD, abbonda in soggetti clinicamente sani e può dirsi, perciò, biomarker di piena salute enterica.
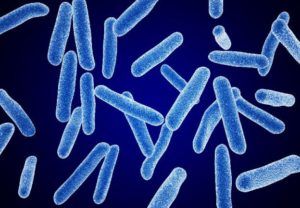
Figura 2 – Faecalibacterium prausnitzii 
Figura 3 – Mucosa del colon
Sarà pure che esso produce butirrato e che tale prodotto di fermentazione è la migliore fonte energetica per i colonociti (Figura 3), senza dimenticare, comunque, il suo ruolo di modulatore dell’espressione genica, differenziamento cellulare ed apoptosi delle cellule ospiti. Tutti gli acidi grassi a catena corta (SCFA) sono frutto di fermentazione di fibre vegetali, giunte con i migliori alimenti integrali e le più fresche verdure di stagione. Amido resistente, inulina e FOS: i batteri intestinali non chiedono di più, per proliferare. Certo, la resa dei preziosi metaboliti batterici varia in base a chi siano gli agenti fermentanti, e da quanti siano.
Prodotti i metaboliti, possibile il cross-feeding!
Poichè ogni ceppo batterico è responsabile della produzione di un certo metabolita, succede che la convivenza felice nel micro-habitat si declini, anche, in un reciproco nutrimento, a gioia e conforto dello stesso ospite. Ecco il cross-feeding. Nel neonato, per esempio, è noto e provvidenziale proprio il cross-feeding tra Bifidobacterium e Faecalibacterium: l’uno produttore di lattato ed acetato, l’altro consumatore di acetato e produttore di butirrato. Certo, il Bifidobacterium è in grado di produrre i suoi fermentati solo se presenti fonti energetiche locali di amido e FOS.
Eppure, nonostante la cruciale funzione protettiva e nutritiva di un simile ceppo batterico, ancora pochi sono i lavori che lo riguardano.
Faecalibacterium sotto la lente d’ingrandimento: lo studio
Il Dr. Kim, dunque, ed i suoi collaboratori hanno impiegato isolati fecali di Faecalibacterium prausnitzii ATCC27768 ed A2-165, oltre a 7 ceppi di Bifidobacterium, provenienti da neonati sani. I due ceppi di Faecalibacterium hanno effettuato crescita in anaerobiosi. Per 24 ore a 37°C, su brodo per clostridi modificato e rinforzato, in appositi tubi di Hungate. Intanto, i 7 ceppi di Bifidobacterium hanno risposto a crescita in anaerobiosi su MRS supplementato con 0.05% v/v di L-cisteina, per 18 ore a 37°C.
Ogni singolo ceppo ha, poi, fatto parte di un inoculo all’1% v/v in 10 uL di medium YCFOS (estratto di lievito, casitone e FOS). Le co-colture, ancora, allestite con differenti batteri in rapporto 1:1. Su queste, nessuna aggiunta di SCFA ma supplementi di amido, inulina e FOS (3.5g/L per ogni). Naturalmente, tutte le pratiche sperimentali hanno richiesto condizioni di anaerobiosi. Camera anaerobica a 37°C, atmosfera all’80% di azoto, 10% di idrogeno e 10% di anidride carbonica.
Tanto le monocolture quanto le co-colture hanno subìto misurazione di densità ottica (OD 650nm), conta cellulare, valutazione del pH e degli SCFA prodotti.
Il modello murino
Necessitando di un sistema modello, i ricercatori si sono premurati di ottenere l’approvazione della commissione etica della Seoul National University, Institutional Animal Care and Use Committee, prima di allestirne uno murino.
Gli esperimenti hanno, così, riguardato 24 esemplari maschili C57BL/6, acclimatati per una settimana prima delle fasi analitiche. Essi hanno dato vita a 4 differenti gruppi di prova. Il gruppo F ha subìto somministrazione di solo Faecalibacterium prausnitzii. Quello FB ha ricevuto Faecalibacterium prausnitzii e Bifidobacterium catenulatum. Un gruppo B, solo il Bifidobacterium ed il gruppo C (controllo), solo soluzione salina sterile. Dosi batteriche da 200 uL giornaliere, per 14 giorni, in alimentazione forzata. Prima di sacrificare gli animali, i ricercatori hanno raccolto ogni campione fecale al fine di determinare, in primis, l’abbondanza relativa dei batteri fecali.
Un secondo esperimento ha, invece, riguardato 45 esemplari femminili C57BL/6, separati in 5 gruppi. Il gruppo detto “non trattato” o gruppo n. Un gruppo M che, su substrato YCFOS, ha subìto somministrazione di DSS (Destrano Sodio Solfato). Ancora un gruppo FB cui, però, i ricercatori, hanno somministrato il sovranatante proveniente dalla co-coltura di Faecalibacterium prausnitzii e Bifidobacterium catenulatum, insieme a DSS. I gruppi F e B, ai quali, invece sono stati somministrati rispettivamente i sovranatanti delle monocolture dei due ceppi batterici, oltre al DSS.
Il DSS al 2% w/v, nell’acqua da bere, era a disposizione per 7 giorni consecutivi, seguiti poi da 2 giorni a normale acqua potabile.
Perché il Destrano Sodio Solfato?
Per giungere finalmente al cuore della complessità eziologica, a cavallo tra la biochimica e la biologia molecolare, che chiama in causa l’ambiente di crescita, la genetica ereditata e le disfunzioni della barriera difensiva intestinale, i modelli patologici umani e animali si sono rivelati essenziali. Uno dei più popolari e comuni è quello che si avvale dell’impiego di DSS (a basso peso molecolare), aggiunto all’acqua potabile nei modelli murini. Perchè. Per indurre danno epiteliale ed una robusta risposta infiammatoria nel colon, che duri per giorni, durante i quali si procederà con prove ed ipotesi sperimentali d’intervento. Si ingenera, dunque, volutamente una colite acuta.
Le coliti possono, infatti, essere causate da infezioni virali, batteriche, da insulto ischemico o patologie autoimmuni. Ma possono derivare anche da stimoli chimici, tra i quali, quello da DSS, è uno dei più semplici e con gli esiti più vicini alle coliti ulcerose autoimmuni umane.
I gusti del Faecalibacterium
In base all’analisi ottica condotta, Faecalibacterium prausnitzii non pare crescer bene su fonti di carbonio come quelle testate in monocoltura; di contro, il Bifidobacterium è risultato, invece, in monocoltura, carbonio-dipendente, durante la crescita. La stimolazione di crescita esplicata dalla co-coltura batterica, ancora, è emersa anch’essa essere carbonio-dipendente.
Tutti i batteri vagliati crescono meglio su glucosio e, come seconda scelta, su FOS. Il che sta ad indicare che essi metabolicamente prediligano zuccheri a catena corta o addirittura monosaccaridi, rispetto a fonti carboniose a catena più lunga e complessa, come l’amido o l’inulina.
Dopo 24 ore di co-coltura, infatti, i risultati sono chiari:
- FOS favoriscono il 54.1%-109% di crescita batterica, rispetto a quella ottimale su glucosio
- inulina, il 23.1-62.3%
- amido, il 22-29.9%.
In co-coltura, Faecalibacterium prausnitzii e Bifidobacterium catenulatum crescono discretamente con FOS ed inulina. Il solo Bifidobacterium catenulatum, in particolare, cresce meglio con questi due nutrienti, rispetto agli altri bifidobatteri inclusi nello studio.
Alla felicità batterica seguono SCFA
A conferma della preferenza dietetica dei due compagni di co-coltura, la maggior quantità di acidi grassi a catena corta (SCFA) si è resa rilevabile nel mezzo colturale dotato di glucosio. E tra gli SCFA, acetato, soprattutto. Questo, nelle co-colture composte dai due attori principali. Altre, invece, formate da bifidobatteri quali B. catenulatum KCTC 3221, B. bifidum BGN4 e B. longum RD72, hanno prodotto prevalentemente lattato. E quest’ultimo, principalmente in co-coltura.
Intanto, il numero di cellule di Faecalibacterium prausnitzii, in monocoltura, decresce dopo 24 ore: da 6.82 a 6.45 CFU/mL. In co-coltura con il fido Bifidobacterium catenulatum, invece, la popolazione di Faecalibacterium prausnitzii cresce nel tempo: di più tra le 18 e le 24 ore successive all’allestimento dell’abbinata. E, nonostante il pH colturale decresca qui considerevolmente, da 7.34 a 5.28, Faecalibacterium prausnitzii cresce, eccome.
Se ne deduce, allora, che lo stimolo alla crescita, per il Faecalibacterium, sia il butirrato da sè stesso prodotto. E che a tale fioritura di popolazione, tuttavia, contribuisca anche il B. catenulatum, velocizzando la degradazione delle fibre e producendo acetato.
La “prova dei fatti” negli esemplari murini
Chiariti gli estremi organici e chimico-fisici dei ceppi in co-coltura, i ricercatori hanno sottoposto dati e deduzioni alla prova dei fatti. Sommistrati, dunque, i ceppi agli esemplari murini, si è osservata una notevole riduzione di diarree e di decessi. L’analisi microbiologica delle feci ha parlato di prevalenza di Faecalibacterium prausnitzii e Firmicutes, in progressione tra le 3 e le 5 settimane dall’inizio della sperimentazione.
E sulla scorta delle indagini molecolari in RT-qPCR, compendiate dai dati microbiologici, è emerso che Faecalibacterium prausnitzii sia più abbondante in topi dei gruppi F ed FB (più in FB) che in quelli non trattati (controlli). Con abbondanza di Bifidobacterium, invece, nei gruppi B ed FB (più in B).
Nulla di strano. Semplicemente Faecalibacterium prausnitzii, da solo, difetta nella colonizzazione e nella conseguente proliferazione, ma viene messo presto a proprio metabolico agio dall’accostamento al Bifidobacterium.
Ultimi, gli effetti sull’infiammazione colica
Le proprietà antinfiammatorie sono state valutate ed apprezzate nel sovranatante prelevato dalle co-colture, poichè in esso si concentrano i frutti biochimici del felice connubio. Somministrato, infatti, agli sfortunati esemplari cui, i ricercatori, hanno inflitto colite ulcerosa DSS-dipendente, gli aggiustamenti immunologici non si sono fatti attendere.
Quando il sovranatante proveniva dalla co-coltura FB, il livello sierico di IL-8 si è ridotto notevolmente, sia rispetto al controllo negativo, sia rispetto agli esiti dei sovranatanti monocolturali F e B. Addirittura, il contributo antinfiammatorio del sovranatante FB è del tutto paragonabile a quello esplicato dal sodio butirrato 1 mM.
Ma non basta. Esponendo anche la linea cellulare RAW 264.7, modello macrofagico murino per studi di risposta cellulare a microrganismi e loro prodotti, al prodigioso sovranatante FB, i ricercatori hanno registrato un crollo delle citochine, IL-6 e TNF-α, pro-infiammatorie.
Prove in vivo hanno, inoltre, restituito dati d’espressione genica. Il DSS somministrato ai topi, pur dovendo, prevedibilmente, incrementare l’espressione genica in mRNA di Il8 ed Il6, è, invece, parso contrastato dall’intervento del sovranatante FB. In grado di ridurre sensibilmente i livelli di espressione del gene Il8. Il sovranatante F, invece, ha manifestato effetti di riduzione sull’espressione di Il6. Gli altri, derivanti dai gruppi batterici M e B, non hanno inciso significativamente sui livelli espressivi dell’mRNA per Tnf-α.
Tirando somme microbiologiche
L’effetto sorprendente del sovranatante FB può verosimilmente dipendere dalla sua ricchezza in butirrato di sodio. Esso riduce il pH del colon favorendo lo sviluppo del ceppo Eubacterium cylindroides, il quale, poi, promuove la secrezione di mucina da parte della mucosa enterica. La mucina, a sua volta, stimola la proliferazione di Akkermansia muciniphila, che degrada il muco, rilascia oligosaccaridi, produce propionato ed acetato. Non solo. Akkermansia regola l’espressione dei geni coinvolti nell’immunità, nel metabolismo e nella funzionalità della barriera intestinale. Faecalibacterium prausnitzii e Akkermansia muciniphila, infatti, sono sempre presenti nella mucosa enterica di soggetti sani. Ed indicativamente ridotti, invece, nei gravi disordini intestinali.
Per questo, il risultato generale di questo ultimo studio si allinea perfettamente nel solco di una evidente ed indispensabile co-azione dei due ceppi sperimentalmente abbinati, in grado così di sostenersi a vicenda ed alleviare, nell’ospite, le pene delle progressioni patologiche. Lo chiamano cross-feeding.
Riferimenti bibliografici
- https://www.mdpi.com/2076-2607/8/5/788
- Immagine d’anteprima fonte: https://www.eurekalert.org/pub_releases/2019-02/cfgr-wmc020119.php
- Figura 2 fonte: https://www.pinterest.it/pin/464222674076315692/
- Figura 3 fonte https://www.google.com/url?sa=i&url=https%3A%2F%2Fwww.eurekalert.org%2Fpub_releases%2F2019-02%2Fcfgr-wmc020119.php&psig=AOvVaw1fkP-MKgI9Zdod8qotUr8t&ust=1604591144656000&source=images&cd=vfe&ved=0CAkQjhxqFwoTCLiw-I3m6-wCFQAAAAAdAAAAABAD
- https://www.microbiologiaitalia.it/batteriologia/amidi-resistenti-sano-microbiota-e-perdita-peso/