Lo studio computazionale dei complessi LH2 dei batteri fotosintetici viola punta a spiegare l’adattamento delle forma di vita agli ambienti scarsamente illuminati
Fotosintesi e strutture biologiche
Il processo di fotosintesi, in piante, alghe o batteri, inizia con l’assorbimento della luce solare da parte dei complessi proteici di raccolta della luce (LH) contenenti diversi cromofori. Quest’ultimi sono molecole o sistemi di legami chimici in grado di assorbire radiazioni elettromagnetiche nel campo del visibile e dell’ultravioletto.
Un ramo della biologia strutturale cerca di capire sia come tali enormi complessi biochimici siano in grado di assorbire la luce dall’ambiente sia come siano in grado di adattarsi a ambienti differenti.
Oramai è ben noto alla comunità scientifica che tali antenne biologiche fanno parte di una struttura più grande, chiamata fotosistema (Fig. 1), che si trova nelle membrane fotosintetiche degli organismi autotrofi (Fig. 2).

Un tipico fotosistema ha diversi complessi di antenne attorno a un nucleo proteico centrale avente un centro di reazione (RC). I componenti interni dei complessi LH e RC sono disposti in modo da formare una scala energetica che faccia sì che la luce sia catturata sotto forma di fotoni dai complessi periferici e poi scenda attraverso i vari passaggi di trasferimento di energia tra cromofori fino a raggiungere il centro di reazione, dove iniziano le reazioni chimiche della fotosintesi.
I batteri fotosintetici viola
I batteri viola non solforosi (Fig. 3) sono in grado di adattare i propri complessi antenna in risposta alle diverse condizioni di irraggiamento luminoso, in maniera analoga alla nostra capacità di sintonizzare una radio su frequenze diverse.

Grazie alla capacità di esprimere i diversi geni codificanti per le proteine di diversi complessi LH, questi particolari batteri possono modificare l’ambiente proteico intorno ai propri cromofori, che per questi microrganismi prendono il nome di “batterioclorofille a” (Fig. 4).

Il cambiamento nella sequenza proteica modifica le energie di eccitazione delle batterioclorofille a nel complesso LH. I dati sperimentali mostrano che quando questi batteri vengono coltivati in condizioni di scarsa illuminazione, esprimono complessi LH con il massimo assorbimento a valori di lunghezze d’onda inferiori (800-820 nm) rispetto a quelli cresciuti in condizioni di elevata illuminazione (800-850 nm).
Tale spostamento verso il blu dello spettro della radiazione elettromagnetica aumenta la differenza di energia LH-RC e favorisce il trasferimento di energia verso il centro di reazione.
Ciò rappresenta un’importante caratteristica adattativa per i batteri viola che vivono nelle profondità di stagni, laghi, mari e oceani come microrganismi fotosintetici anaerobici.
Il contributo della chimica computazionale
Ma quali sono le caratteristiche strutturali responsabili della capacità dei batteri viola di spostare lo spettro di assorbimento della luce verso il blu in presenza di una scarsa illuminazione?
Per rispondere a questa domanda il Dottor Felipe Cardoso Ramos, dottorando di ricerca presso la Scuola di Dottorato in Scienze Chimiche e dei Materiali del Dipartimento di Chimica e Chimica Industriale dell’Università di Pisa, insieme al resto del gruppo di ricerca di chimica computazionale guidato dalla Prof.ssa Benedetta Mennucci, si è concentrato, nella sua attività di ricerca, sulla caratterizzazione computazionale delle antenne periferiche di due specie di batteri viola, quali Rhodopseudomonas acidophila e Rhodopseudomonas palustris.
Inoltre, i risultati ottenuti da questo approccio computazionale, che unisce microbiologia, chimica-fisica e bioinformatica, sono stati confrontati e validati con i risultati ottenuti sperimentalmente combinando analisi di spettroscopia di assorbimento e studi di cristallografia delle proteine coinvolte in questi sistemi biologici.
Sinergia tra approccio sperimentale e approccio computazionale
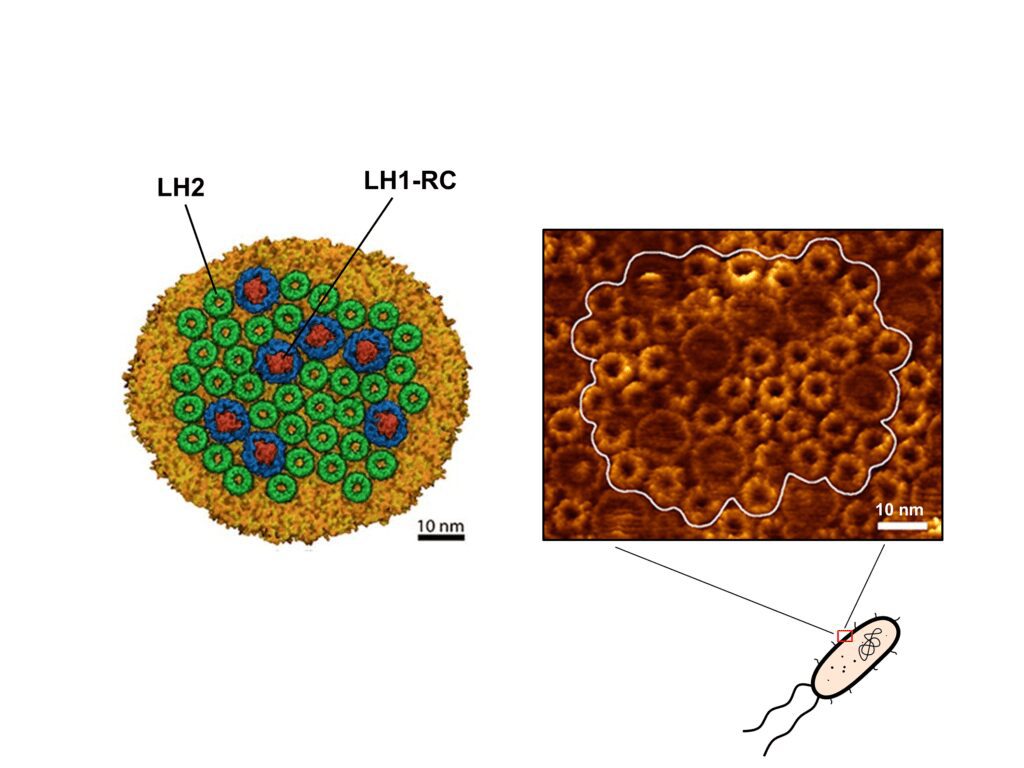
Secondo il Dottor Cardoso Ramos: “Gli studi sperimentali hanno fornito preziose informazioni alla comunità scientifica sulla struttura e la composizione dei complessi LH. Nel caso dei batteri viola non solforosi, l’apparato per la raccolta della luce è composto dai complessi LH1 e LH2 (Fig. 2). Il loro processo adattivo in carenza di luce riguarda solo LH2. Per questo motivo ho concentrato il mio studio sulla descrizione strutturale del complesso LH2.”
Inoltre, l’autore dell’articolo scientifico dal titolo “The molecular mechanisms of light adaption in light-harvesting complexes of purple bacteria revealed by a multiscale modeling”, pubblicato sulla prestigiosa rivista “Chemical Science” ha sottolineato: “Nonostante gli studi cristallografici possano fornire importanti informazioni strutturali, essi non consentono un’analisi dell’evoluzione temporale dei complessi proteina-cromoforo. In effetti, è noto che molte proprietà dei sistemi biologici possono essere meglio comprese solo attraverso approcci dinamici. Pertanto, simulazioni computazionali dipendenti dal tempo di “Molecular Dynamics” sono cruciali per lo studio di tali fenomeni. Inoltre, in combinazione con i calcoli della meccanica quantistica, la dinamica molecolare classica diventa un potente strumento per descrivere i processi fotoindotti in ambienti biologici.”
Lo studio computazionale italiano
Da questo innovativo studio italiano, è emerso come i legami idrogeno generati dall’ambiente intorno alle batterioclorofille a controllano dinamicamente i gradi di libertà sia all’interno dei pigmenti sia tra pigmenti diversi. Solo la combinazione di questi due effetti può spiegare completamente la modulazione delle energie dello stato eccitato delle batterioclorofille a e spiegare le differenze spettroscopiche osservate tra i complessi LH2 in presenza di alta e scarsa illuminazione.
Il giovane ricercatore ha spiegato: “Al fine di studiare l’origine delle differenze spettrali tra i complessi in presenza e carenza di luce, in questo studio abbiamo analizzato tre complessi antenna LH2, di cui due della specie Rps. acidophila e uno della specie Rps. palustris. Quest’ultimo non ha una struttura cristallografica disponibile nei database delle strutture proteiche, per cui è stata effettuata una predizione strutturale basata sull’omologia di sequenza. Esso rappresenta un’analisi comparativa molto utile sia per gli studi sulla struttura delle proteine sia in bioinformatica.“
La simulazione computazionale: meccanica quantistica e dinamica molecolare
Dallo studio condotto dai ricercatori di Pisa è emerso come la struttura dei complessi LH2 cambia poco tra le due specie di batteri viola. Generalmente si osserva la stessa disposizione e composizione delle molecole di batterioclorofilla a in tali complessi.
C’è sempre la formazione di due anelli, uno superiore e uno inferiore (Fig. 5). Ciò che cambia è l’ambiente biochimico intorno alle molecole dell’anello superiore. Infatti, la banda di assorbimento a 800 nm proviene dall’assorbimento delle molecole dell’anello inferiore, che hanno un ambiente proteico conservato. Per questo motivo solo una banda dello spettro si sposta.

Il sistema di regolazione dei batteri viola
A tal proposito, secondo il Dott. Cardoso Ramos: “Per essere più preciso, cambia il numero di legami idrogeno tra il cromoforo e la proteina (Fig. 6). Maggiore è il numero di legami idrogeno, più rigido sarà l’anello superiore e questo avrà un impatto sia sulla flessibilità interna del cromoforo sia sull’interazione cromoforo-cromoforo”.

Ha inoltre aggiunto: “Nel complesso I, le batterioclorofille a si muovono meno e interagiscono meglio. Ciò favorisce l’accoppiamento elettronico tra i cromofori dell’anello superiore (Fig. 6). Maggiore è l’accoppiamento elettronico, maggiore è la differenza tra le due bande dello spettro. Inoltre, è importante notare che la semplice presenza o mancanza di un residuo proteico vicino al cromoforo può cambiare la sua energia di eccitazione. Pertanto, oltre all’effetto dell’interazione cromoforo-cromoforo, la rimozione di un legame idrogeno provoca uno spostamento verso il blu nello spettro”.
Uno sguardo al futuro: la fotosintesi artificiale
In generale, la combinazione tra microbiologia, chimica-fisica e bioinformatica offre dei potenti strumenti di analisi e descrizione di moltissimi processi biologici. Inoltre, tale approccio computazionale consente di ottenere informazioni importanti su tantissimi fenomeni evolutivi che hanno permesso ai microrganismi di adattarsi agli ambienti più estremi, come, in questo caso, i fondali marini e/o oceanici scarsamente illuminati dalla luce solare.
Il Dottor Cardoso Ramos ha concluso con un’importante prospettiva sul suo progetto di ricerca: “Attraverso il presente studio è stato possibile chiarire un intrigante meccanismo di adattamento molecolare dei complessi LH2 in condizioni di scarsa luminosità. Le spiegazioni fornite aprono un nuovo scenario per lo sviluppo di strategie di mutagenesi basate sulla struttura dei fotosistemi che mirino a controllare l’energia relativa tra i cromofori nei complessi LH2. Ciò potrebbe avere importanti implicazioni future sullo sviluppo, ad esempio, di dispositivi di fotosintesi artificiale in grado di contribuire alle richieste energetiche dell’uomo”.
Nicola Di Fidio
Sitografia:
- Mara Magistroni (17 ottobre 2018, Wired.it). La vita sul nostro pianeta un tempo era viola? Estrapolato da: https://www.wired.it/scienza/spazio/2018/10/17/vita-aliena-terra-viola/?refresh_ce=
- Massimo Aloisi (17 maggio 2018, Biopills). Fase luminosa della Fotosintesi. Estrapolato da: https://www.biopills.net/fase-luminosa-della-fotosintesi/
- Nicola Di Fidio (19 giugno 2019, Microbiologia Italia). Bio-batterie a base di batteri e nanoparticelle magnetiche. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/bio-batterie-a-base-di-batteri-e-nanoparticelle-magnetiche/
Bibliografia:
- Ramos, F. C., Nottoli, M., Cupellini, L., & Mennucci, B. (2019). The molecular mechanisms of light adaption in light-harvesting complexes of purple bacteria revealed by a multiscale modeling. Chemical science, 10(42), 9650-9662.
Crediti immagini:
- https://www.sciencedirect.com/science/article/pii/S0006349514004470
- https://littlemicrobes.wordpress.com/bmm-usage/phototropic-bacteria-purple-non-sulfur-bacteria/
- https://slideplayer.it/slide/596280/
- https://pubs.rsc.org/en/content/articlehtml/2019/sc/c9sc02886b