Il microbiota nel bambino
La formazione precoce del microbiota intestinale nel bambino è influenzata da vari fattori tra cui la modalità del parto (parto cesareo o parto naturale), l’allattamento al seno rispetto all’alimentazione con latti formulati, l’uso di antibiotici e i tempi di introduzione degli alimenti solidi, ossia la fase dello svezzamento. Leggi la prima parte dell’articolo tramite il seguente link:
Fattori che influenzano il microbiota
Lo sviluppo e la maturazione del microbiota intestinale nel bambino sono processi altamente dinamici e influenzati da varie condizioni perinatali, inclusi fattori esterni (per esempio tipo di parto, alimentazione, uso di antibiotici, stile di vita e variabili geografiche) e fattori legati all’ospite (fattori genetici).

Tipologia di parto
La tipologia di parto esercita un impatto cruciale sul tipo di microbiota ingerito dal bambino alla nascita.
L’impatto del parto persiste per mesi dopo la nascita in quanto contribuisce allo sviluppo del microbiota, che può influenzare i normali processi fisiologici.
Durante il parto, il neonato, passando nella vagina, viene esposto alla complessa popolazione di microrganismi che vi risiedono.
Studi hanno rilevato che il microbiota della vagina materna presenta somiglianze con quello intestinale dei figli, suggerendo un’importante influenza del primo contatto, costituito dal parto, nello sviluppo del microbiota del neonato.
Una conferma ulteriore deriva dall’evidenza secondo la quale bambini partoriti con taglio cesareo hanno un microbiota intestinale diverso da quello dei nati da parto naturale, proprio perché non hanno il contatto con il microbiota vaginale.
Il principale microbiota che colonizza l’intestino del bambino, quindi, è simile per composizione al microbiota vaginale, con una componente minore proveniente dall’ambiente circostante.
In seguito a parto naturale, il neonato entra in contatto, oltre che con il microbiota vaginale, anche con quello intestinale della madre.
Al contrario, un neonato partorito con taglio cesareo non entra in contatto con il microbiota vaginale e la componente principale del microbiota intestinale infantile in questo caso è data dall’ambiente circostante e dal microbiota cutaneo della madre.
L’intestino dei bambini nati per via vaginale viene prima di tutto colonizzato dai batteri presenti nella vagina e nell’intestino della madre. È stato ipotizzato che l’assenza di tale trasmissione in caso di parto cesareo possa avere conseguenze a lungo termine sulla salute del bambino, come lo sviluppo di obesità, asma e celiachia.
Inoltre i Bacteroides, più abbondanti dopo un parto per via vaginale, influenzano la maturazione del sistema immunitario.
In caso di parto naturale, quindi, il microbiota intestinale nel bambino assomiglia al microbiota vaginale nella madre, che è dominato dai generi Lactobacillus, Prevotella o Sneathia.
Il microbiota dei neonati nati da taglio cesareo, invece, è più simile al microbiota cutaneo, che è dominato da Staphylococcus, Corynebacterium e Propionibacterium.
Alcuni studi hanno dimostrato, inoltre, che la colonizzazione da parte di Bacteroides e Bifidobacterium è ritardata a un mese dopo la nascita, mentre è abbondante Clostridium difficile.

Età gestazionale
I neonati vengono definiti pretermine quando nascono prima di 37 settimane di gestazione.
A seconda del grado di prematurità, questi neonati possiedono organi immaturi e possono pertanto andare incontro a numerose difficoltà sviluppando gravi problemi di salute.
Presentano sovente un intestino immaturo, problemi immunitari, respiratori, neurologici e sono esposti a estesi trattamenti antibiotici e farmacologici.
Inoltre trascorrono lunghe degenze negli ospedali, spesso sottoposti a respirazione artificiale e alimentati artificialmente. Tutti questi fattori interferiscono con il modello naturale di acquisizione e sviluppo del microbiota, che risulta alterato nella sua composizione (ibidem).
Nei neonati a termine, la tipologia di parto e l’alimentazione rappresentano i principali driver dello sviluppo del microbiota; nei neonati pretermine, invece, l’età gestazionale sembra esercitare il maggiore impatto sull’assemblaggio della comunità intestinale.
Per un nato pretermine la principale fonte microbica disponibile è costituita da batteri derivanti dall’ambiente della terapia intensiva neonatale.
Si tratta per lo più di ceppi implicati in infezioni nosocomiali tra cui Enterococcus spp., Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter spp., Pseudomonas aeruginosa e altre Enterobacteriaceae con il loro carico di geni di resistenza agli antibiotici.
Il processo di colonizzazione, quindi, sembra riflettere una serie di variabili nosocomiali, quali un’elevata carica batterica e una frequente esposizione agli antibiotici, insieme a un ritardo nell’esposizione alla pelle della madre e al microbiota del latte materno.
Questi fattori sono i principali responsabili della ridotta diversità microbica intestinale nei neonati pretermine, con un aumento della colonizzazione da parte di microrganismi patogeni.
Inoltre gli antibiotici, normalmente somministrati a questi neonati, a loro volta perturbano il processo di colonizzazione uccidendo i batteri acquisiti durante la nascita e promuovendo la crescita di taxa significativamente diversi da quelli riscontrati in situazioni più fisiologiche.
Il microbiota di neonati pretermine, quindi, sembra essere più instabile di quello presente nei neonati a termine e si ritiene che sia associato a un ritardo nella creazione di un microbiota di tipo adulto.
Tali alterazioni possono influenzare la salute nel breve e lungo periodo, in quanto l’interazione tra il microbiota alterato e il sistema immunitario immaturo può causare risposte infiammatorie e facilitare le malattie infettive.
Dieta materna durante la gravidanza
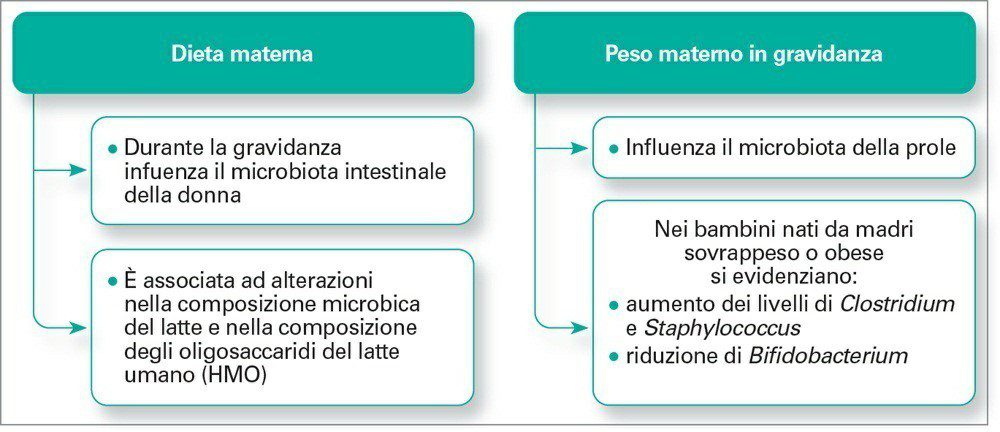
La composizione microbica dell’intestino varia con la dieta e lo stato di salute dell’ospite: durante la gravidanza questi fattori possono influenzare il microbiota intestinale materno, che a sua volta può condizionare quello del bambino in utero e dopo la nascita.
In un recente studio Meyer e altri, usando due trattamenti dietetici, hanno riferito che il cambiamento della dieta materna è associato ad alterazioni significative nella composizione microbica del latte e nella composizione dell’oligosaccaride del latte umano (HMO).
I risultati suggeriscono, quindi, un possibile ruolo delle abitudini alimentari materne durante e dopo la gravidanza nello sviluppo del microbiota intestinale infantile.
Il microbiota materno svolge un ruolo cruciale nell’acquisizione e nello sviluppo del microbiota del neonato, ed è la chiave per stabilire una simbiosi ospite-microbioma sana con effetti di lunga durata sulla salute.
Dopo la nascita il bambino continua ad acquisire direttamente ceppi intestinali materni da diverse fonti (pelle, bocca, latte) e questi probabilmente diventeranno colonizzatori stabili dell’intestino infantile.
La composizione del microbiota fecale del bambino è influenzata anche dal BMI (Body Mass Index o IMC, indice di massa corporea) e dall’aumento di peso della madre durante la gravidanza.
È stato ipotizzato che il diabete e l’obesità materni condizionino il rischio della prole di sviluppare malattie metaboliche croniche, attraverso cambiamenti nella composizione microbica materna durante la gravidanza e l’allattamento.
La composizione microbica dei neonati da madri affette da obesità, infatti, è diversa rispetto a quella di bambini nati da madri normopeso.
Alcuni studi hanno mostrato un aumento dei livelli di Clostridium e Staphylococcus e una riduzione di Bifidobacterium nel microbiota di bambini nati da madri sovrappeso o obese rispetto ai bambini nati da madri normopeso.
Poiché il microbiota intestinale svolge importanti funzioni metaboliche e nutrizionali, queste alterazioni nella composizione microbica potrebbero esercitare un impatto negativo sulla salute materna e su quella della prole, favorendo la trasmissione di un microbioma “obesogeno”.
Esposizione materna agli antibiotici
L’esposizione alla terapia antibiotica e i suoi effetti modulatori sul microbioma umano possono iniziare in utero e continuare durante le fasi di crescita e sviluppo.
È stato dimostrato che le alterazioni del microbiota intestinale dei neonati le cui madri sono state trattate con antibiotici sono simili alle alterazioni osservate nei neonati che hanno assunto antibiotici, evidenziando l’influenza dei farmaci materni sulla salute dei bambini.
Il trattamento antibiotico intra-partum a scopo profilattico è diventato pratica comune nella medicina ostetrica e questo lo rende la fonte più frequente di esposizione agli antibiotici da parte del neonato.
In una recente revisione sistematica Zimmermann e colleghi hanno riportato che il microbiota intestinale di bambini esposti alla profilassi antibiotica intrapartum per Streptococcus di gruppo B presenta bassa biodiversità batterica, con una minore abbondanza relativa di Actinobacteria, in particolare Bifidobacteriaceae, e una maggiore abbondanza relativa di Proteobacteria rispetto ai neonati non esposti.
Tali interferenze durante la “finestra critica” della prima infanzia, quando il microbiota intestinale e la risposta immunitaria si stanno sviluppando, possono avere un’influenza importante sullo sviluppo immunitario.
Questi risultati indicano che l’assunzione di antibiotici da parte delle madri può influenzare il microbioma intestinale dei bambini.
Anche la somministrazione di antibiotici ai neonati ha effetti profondi sullo sviluppo del microbiota intestinale, spostandone la composizione verso un’elevata abbondanza di Proteobacteria e una bassa abbondanza di popolazioni di Actinobacteria, diminuendo la diversità complessiva del microbiota del bambino e selezionando batteri resistenti ai farmaci. Inoltre, l’uso di antibiotici nelle prime fasi della vita aumenta il rischio di sviluppare malattie allergiche quali asma, malattia atopica, eczema e diabete di tipo 1.
Allattamento al seno
Anche l’allattamento è fondamentale per lo sviluppo del microbiota intestinale del bambino.
Fino a poco più di 15 anni fa si pensava che il latte materno fosse sterile; oggi sappiamo che nel latte sono presenti circa 50 generi e circa 600 specie, provenienti da fonti interne ed esterne alla mammella.
Si parla di MOM, ossia di milk – oriented microbiota, cioè di microbiota orientato dal latte materno che è molto simile a quello dell’intestino umano.
Il microbiota del latte materno e gli HMO entrano in contatto diretto con i lattanti e possono modificare la loro composizione microbica intestinale.
I neonati allattati al seno ricevono, con il latte materno, un mix complesso (costituito da nutrienti, proteine ad azione antimicrobica, SCFA, anticorpi, batteri vivi, prebiotici come gli HMO) che influenzerà l’ambiente in cui si svilupperà il loro microbiota.
Si stima che i bambini allattati al seno ricevano 104-106 batteri al giorno, sulla base di un consumo medio giornaliero di 800 ml di latte.
È stato proposto che questi raggiungano la ghiandola mammaria attraverso una via endogena detta “via entero-mammaria”, ancora oggi oggetto di studio. Il microbiota intestinale di neonati allattati al seno è diverso da quello dei neonati alimentati con latte artificiale.
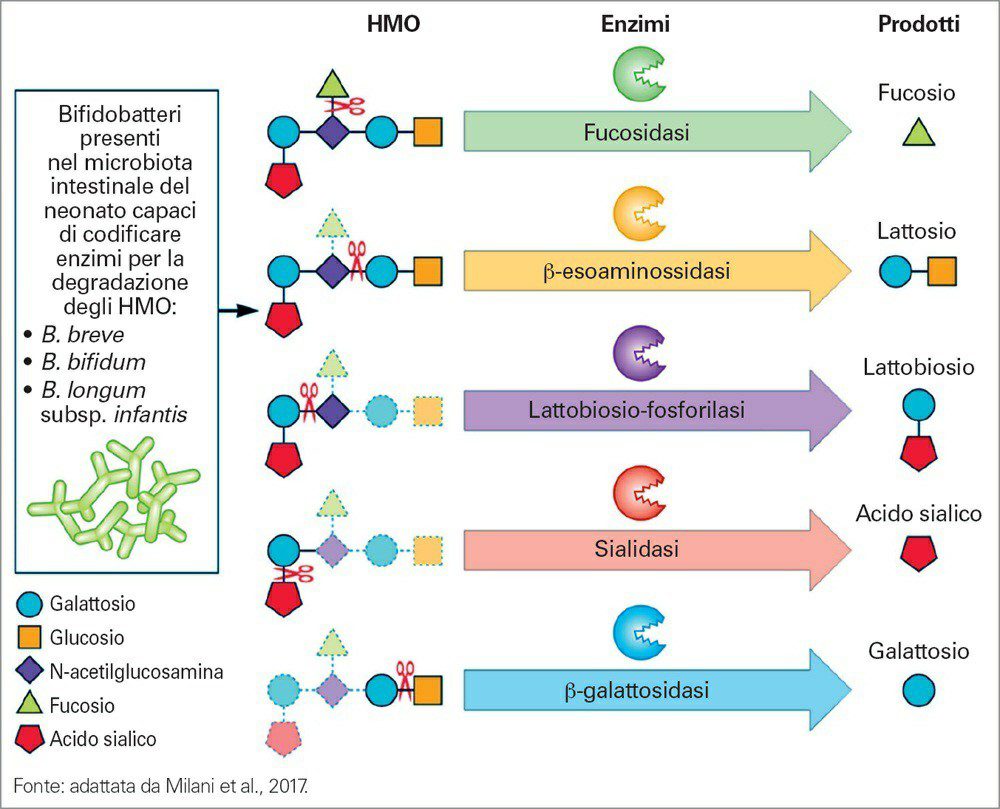
Gli oligosaccaridi del latte umano (HMO) sono i costituenti principali del latte materno e incentivano la crescita di specifici taxa batterici intestinali nel neonato.
Gli oltre 100 diversi HMO identificati si presentano in quantità e composizioni che variano sostanzialmente tra le donne e nel corso dell’allattamento.
Questo fa sì che non tutti i bambini che ricevono latte umano siano esposti alla stessa serie di HMO. Gli HMO influenzano la composizione del microbiota in quanto vengono digeriti solo parzialmente nell’intestino tenue e raggiungono il colon, dove vengono fermentati, principalmente da Bifidobacterium, per produrre SCFA.
Il microbiota intestinale dei neonati allattati al seno, infatti, presenta una composizione più ricca in specie di Bifidobacterium tra cui B. breve, B. bifidum e B. longum.
L’integrazione del latte in formula con galatto-oligosaccaridi (GOS) e frutto-oligosaccaridi (FOS), in rapporto 9:1, sembra imitare l’effetto degli HMO sul microbiota intestinale, stimolando l’arricchimento in Bifidobacterium.
Nonostante questo, i bambini allattati con latte artificiale, rispetto ai neonati allattati al seno, presentano caratteristiche distinte nei loro microbioti, come l’alta conta di Clostridium difficile.
Svezzamento
Durante il periodo dell’allattamento al seno il microbiota intestinale è specializzato nel metabolismo del lattato e dei glicani di origine vegetale, incluso l’amido.
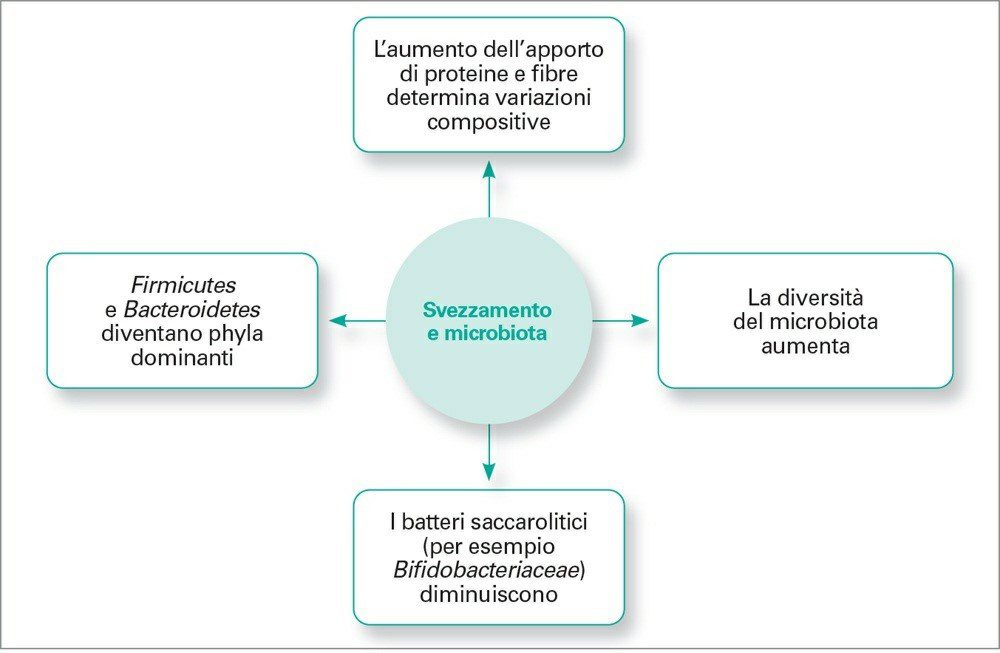
La transizione verso alimenti più variati e solidi è un passo importante nello sviluppo del microbiota intestinale nella prima infanzia; i bambini iniziano a essere esposti a una gamma più ampia di nutrienti e carboidrati non digeribili, che promuovono la sopravvivenza e la proliferazione di taxa batterici più vari.
In generale, l’abbondanza relativa dei microbi intestinali è fortemente influenzata dai modelli e dalle abitudini alimentari.
Con lo svezzamento la diversità aumenta; Proteobacteria e Actinobacteria sono sostituiti da Firmicutes e Bacteroidetes come phyla dominanti, in una struttura compositiva più adulta.
La cessazione dell’alimentazione basata sul consumo di latte è correlata anche alla diminuzione dei batteri saccarolitici quali Bifidobacteriaceae (phylum: Actinobacteria). Inoltre l’aumento dell’apporto proteico si associa a un aumento di Lachnospiraceae (phylum: Firmicutes) e l’ingestione di fibre a livelli più alti di Prevotellaceae (phylum: Bacteroidetes).
I lattanti nutriti con latte artificiale non mostrano una transizione così marcata della flora gastrointestinale all’introduzione di alimenti solidi esterni.
Questo perché, sin dalla nascita, l’allattamento artificiale li espone a una dieta che include alcuni composti complessi, stabilendo così una comunità microbica di supporto.
Giuseppe Chindemi
Fonti
- Brooks B., Olm M.R., Firek B.A., Baker R., Thomas B.C., Morowitz M.J., Banfield J.F. “Strain-resolved analysis of hospital rooms and infants reveals overlap between the human and room microbiome” Nature Communications 2017; 8: 1814.
- Chu D.M., Meyer K.M., Prince A.L., Aagaard K.M. “Impact of maternal nutrition in pregnancy and lactation on offspring gut microbial composition and function” Gut Microbes 2016; vol. 7, n. 6, 459–470.
- Singh R.K., Chang H., Di Yan W., Lee K.M., Ucmak D., Wong K. et al. “Infuence of diet on the gut microbiome and implications for human health” J Transl Med 2017; 15:73.
- Kumbhare S.V, Patangia D.V., Patil R.H, Shouche1 Y.S., Patil N.P. “Factors influencing the gut microbiome in children: from infancy to childhood” J Biosci. 2019; 44:49.
- Rinninella E., Raoul P., Cintoni M., Franceschi F., Miggiano G.A.D., Gasbarrini A., Mele M.A. “What is the healthy gut microbiota composition? A changing ecosystem across age, environment, diet, and diseases” Microorganisms 2019; 7, 14.
Articolo interessante! Ormai le tecnologie vanno avanti… Leggendo, penso quante coppie oggi si trovano in difficolta ad avere i figli. Grazie alle tecnologie modernizzate tutto è possibile, come sappiamo già esistono le varie tecniche di procreazione assistita. Sfogliando le pagine internet mi sono imbattuta in un articolo di legge: https://maternita-surrogata-centro.it/maternita_surrogata.pdf.