Uno studio pubblicato sulla nota rivista scientifica Nature, mette in luce i processi infiammatori che avvengono nel sistema nervoso centrale, illustrando quali sono i meccanismi in grado di influenzarli.
I ricercatori hanno focalizzato l’attenzione sulla proteina AHR (aryl hydrocarbon receptor), particolarmente espressa in alcune cellule della glia (quali astrociti e microglia), osservando che è possibile regolare la sua azione attraverso i metaboliti prodotti a partire dal triptofano, assunto attraverso la dieta e controllati dai batteri intestinale.
Cellule gliali e il loro ruolo
Le cellule gliali costituiscono un importante tessuto di sostegno del sistema nervoso, contribuendo alla formazione della barriera emato-encefalica tra sangue e tessuto nervoso. Fagocitano le sostanze estranee, producono il liquido cerebrospinale e formano la guaina mielinica attorno agli assoni.
La proteina AHR è particolarmente espressa su due tipi di cellule gliali: astrociti e microglia.
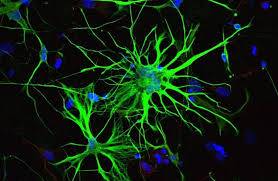
Gli astrociti (Fig.1) sono cellule gliali dalla forma stellata, data dai numerosi processi citoplasmatici. Queste cellule rilasciano molecole in grado di promuovere la formazione di giunzioni serrate tra le cellule endoteliali dei capillari. Le cellule endoteliali, con le loro giunzioni serrate, formano la barriera emato-encefalica, la quale protegge i neuroni da sostanze tossiche che si possono trovare nel sangue. Inoltre permette lo scambio di metaboliti e cataboliti tra neuroni e sangue.
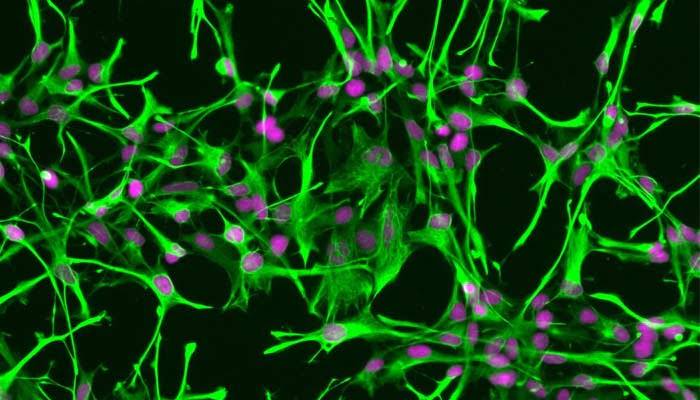
Le cellule della microglia sono cellule immunitarie del sistema nervoso centrale (SNC), che diventano mobili e capaci di fagocitosi in risposta all’infiammazione. Infatti fagocitano tessuto necrotico, microrganismi e sostanze estranee che invadono il SNC.
Lo studio
La proteina AHR è coinvolta nella progressione della encefalomielite autoimmune. E’ una malattia in cui il sistema immunitario attacca le cellule del sistema nervoso centrale, utilizzata per questo come modello sperimentale della sclerosi multipla (SM).
I ricercatori hanno condotto una serie di esperimenti su modelli animali con encefalomielite autoimmune, osservando che quando l’attività di AHR nelle cellule della microglia è bloccata i sintomi della malattia peggiorano, aumentando la demielinizzazione e il reclutamento di monociti nel SNC. Questo processo coinvolge dei mediatori molecolari prodotti dalla microglia, utili ad accendere o spegnere l’infiammazione agendo a loro volta sugli astrociti. La delezione microgliale dell’AHR ha sovraregolato l’espressione di geni negli astrociti associati all’infiammazione e alla neurodegenerazione, come Ccl2 , Il1b e Nos2.
Azione della proteina AHR
I ricercatori hanno scoperto che l’AHR espressa nella microglia regola l’espressione dei geni che codificano due proteine, TGF-α (fattore di crescita trasformante alfa) e VEGF-B (fattore di crescita dell’endoteliovascolare B) che, a loro volta, modulano l’attività pro-infiammatoria degli astrociti.
In particolare, il TGF-α, la cui produzione è inibita dall’eliminazione di AHR, smorza le risposte infiammatorie degli astrociti all’ encefalomielite autoimmune, mentre il VEGF-B, la cui produzione è stimolata dall’eliminazione di AHR, peggiora la condizione patologica.
Ruolo del triptofano nella modulazione dell’infiammazione
I ricercatori hanno osservato che è possibile regolare l’azione dell’AHR attraverso i metaboliti prodotti a partire dal triptofano. Diete ricche di triptofano riescono, infatti, a migliorare i sintomi della malattia in topi con encefalomielite autoimmune, ma non riescono a farlo negli animali in cui AHR è stata eliminata. Questo perché i prodotti del triptofano modulano l’infiammazione attraverso l’azione che esercitano su questa proteina.
La proteina AHR si lega a metaboliti del triptofano alimentare prodotto dai batteri intestinali. Dunque gli studiosi hanno sottoposto diversi gruppi di topi con encefalomielite a una dieta ricca oppure povera di triptofano. Nei topi con encefalomielite, ma con AHR, la carenza di triptofano ha aggravato la malattia. Invece la presenza di triptofano l’ha alleviata. Nei topi con deficit di AHR nella microglia, invece, nessuna delle due diete ha avuto effetti sul decorso della malattia, dato che in questi animali, i metaboliti alimentari del triptofano non possono legarsi alla AHR per smorzare le risposte immunitarie. L’efficienza con cui vengono prodotti questi metaboliti è legata alla specifica composizione della flora batterica intestinale. I cambiamenti nel microbioma intestinale possono alterare l’attività del sistema immunitario cerebrale alleviando oppure aggravando il decorso della malattia.
Conoscere questi meccanismi molecolari potrebbe essere utile per lo sviluppo di nuove terapie per la sclerosi multipla e altre malattie neurologiche.
Anna Maria Musto
Fonti
- Veit Rothhammer, Davis M Borucki, Emily C Tjon, Maisa C Takenaka, Chun-Cheih Chao, Alberto Ardura-Fabregat, Kalil Alves de Lima, Cristina Gutiérrez-Vázquez, Patrick Hewson, Ori Staszewski, Manon Blain, Luke Healy, Tradite Neziraj, Matilde Borio, Michael Wheeler, Loic Lionel Dragin, David A Laplaud, Jack Antel, Jorge Ivan Alvarez, Marco Prinz, Francisco J Quintana, “Microglial control of astrocytes in response to microbial metabolites“. Nature.
- Vanputte, Regan, Russo “Anatomia Umana” IV Edizione.