Caratteristiche
Il Mycobacterium tuberculosis (detto anche bacillo di Koch), scoperto nel 1882 da Robert Koch da cui prende il nome, è il bacillo responsabile della tubercolosi nell’uomo (TBC).
Il Mycobacterium tubercolosis possiede due classi di antigeni, rispettivamente di natura polisaccaridica e di natura proteica.
La struttura del Mycobacterium tubercolosis è a strati, sono presenti peptidoglicano, arabinogalattino e glicolipidi di superficie dove si ancorano gli acidi micolici. I glicolipidi di Mycobacterium sono detti anche micosidi; gli acidi micolici sono lipidi a 60-90 atomi di carbonio uniti a carboidrati tramite legami covalenti.
Il Mycobacterium tubercolosis non viene classificato né come Gram-negativo né come Gram-positivo in quanto ha caratteristiche comuni ad entrambi. Appartenenti alla famiglia delle Mycobacteriacee, sono bacilli immobili, non sporigeni, aerobi obbligati, delle dimensioni di 0,2-0,6 x 1-10 µm, caratterizzati dalla lenta crescita, da una parete ricca di acidi micolici e da un DNA con elevato contenuto di guanina e citosina (60-70%).
Ancora oggi, l’infezione tubercolare é la causa di malattia con un minimo di 2 casi per 100.000 abitanti ed un massimo, in alcuni paesi in via di sviluppo, di 500 casi per 100.000 abitanti. Nell’uomo l’infezione si manifesta per via inalatoria. Va considerato, però, che il bacillo tubercolare può entrare nell’organismo praticamente attraverso tutte le vie di infezione e può localizzarsi in molti organi e tessuti, dove determinerà una serie di eventi che sono sostanzialmente sovrapponibili a quelli che si verificano nell’infezione polmonare.
Micobatteri
I micobatteri in medicina vengono suddivisi in due diversi gruppi, a seconda della loro patogenicità. Il primo gruppo comprende i micobatteri tubercolari, responsabili di scatenare la tubercolosi nell’ospite animale. Questo gruppo è costituito dai tre batteri del cosiddetto Mycobacterium tuberculosis complex:
- Mycobacterium tuberculosis (responsabile della tubercolosi umana);
- Mycobacterium africanum (correlato alla stessa patologia del M. tuberculosis, seppure leggermente differente sotto il profilo biochimico ed isolato con maggiore frequenza in Africa);
- Mycobacterium bovis (responsabile della tubercolosi bovina, zoonosi trasmissibile all’uomo per via alimentare).
Un altro gruppo è costituito dai micobatteri non tubercolari, ossia da micobatteri che scatenano una serie di patologie diverse dalla tubercolosi nell’ospite umano, ma solo in concomitanza di particolari condizioni che abbassino le difese immunitarie dell’organismo colonizzato (si configurano perciò come parassiti opportunisti).
Filogenesi
| Dominio | Prokaryota |
| Regno | Bacteria |
| Phylum | Actnobacteria |
| Ordine | Actinomycetales |
| Famiglia | Mycobacteriacee |
| Genere | Mycobacterium |
| Specie | M. tubercolosis |
Morfologia delle Colonie
Mycobacterium tuberculosis può essere coltivato in laboratorio ma rispetto ad altri batteri comunemente studiati, M. tuberculosis ha un tasso di crescita notevolmente lento, raddoppiando all’incirca una volta al giorno. I terreni di coltura comunemente usati includono brodi come Middlebrook 7H9 o 7H12, terreni solidi a base di uova come Lowenstein-Jensen e terreni agarizzati come Middlebrook 7H11 o 7H10. Le colonie visibili richiedono diverse settimane per crescere su piastre di agar.
Patogenesi
La tubercolosi nella maggior parte dei casi interessa le vie aeree (i polmoni); si trasmette attraverso goccioline di saliva emesse da persone infette durante la fonazione, i colpi di tosse, gli sputi e gli starnuti. La maggior parte delle persone che entrano a contatto con questi germi non sviluppa i sintomi della malattia, che viene efficacemente spenta sul nascere dal sistema immunitario.
Nella tubercolosi polmonare, il bacillo di Koch è localizzo a livello degli alveoli dove viene fagocitato dai magrofagi alveolari. Attraverso la struttura della parete cellulare e alla presenza dal fattore cordale, il bacillo è capace di inattivare i macrofagi, poiché causa il blocco della fusione fagosoma-lisosoma, un processo importante per l’eliminazione degli agenti patogeni fagocitati. Questo blocco permette al batterio di sopravvivere e replicarsi all’interno dei macrofagi ormai inattivati.
Tale replicazione intracellulare forma dei nuovi bacilli, detriti cellulari e batterici, e scatena l’innesco di una risposta immunitaria cellulo-mediata che provoca l’attivazione di linfociti T e macrofagi. L’infezione e l’attivazione del sistema immunitario forma dei cosiddetti granulomi o tubercoli (dal quale deriva il nome “tubercolosi”). Al centro dei tubercoli è presente una necrosi caseosa circondata da cellule di Langhans (cellule grandi multinucleate in cui i nuclei sono disposti a ferro di cavallo), a loro volta attorniate da linfociti T e plasmacellule, il tutto racchiuso da uno strato di tessuto fibroso.
Poiché il sistema immunitario non è capace di eliminare l’agente patogeno avviene la formazione dei granulomi. La strategia più utile per arginare l’infezione consiste nel creare un “involucro” di tessuto all’interno del quale il bacillo di Koch è isolato dal resto dell’organismo. I bacilli presenti nei granulomi possono essere eliminati, oppure possono restare latenti per lunghi periodi di tempo (mesi o addirittura anni). Nel caso in cui il paziente non manifesti sintomi per anni, esso potrà risultare positivo al test per la tubercolosi ma non sarà contagioso.
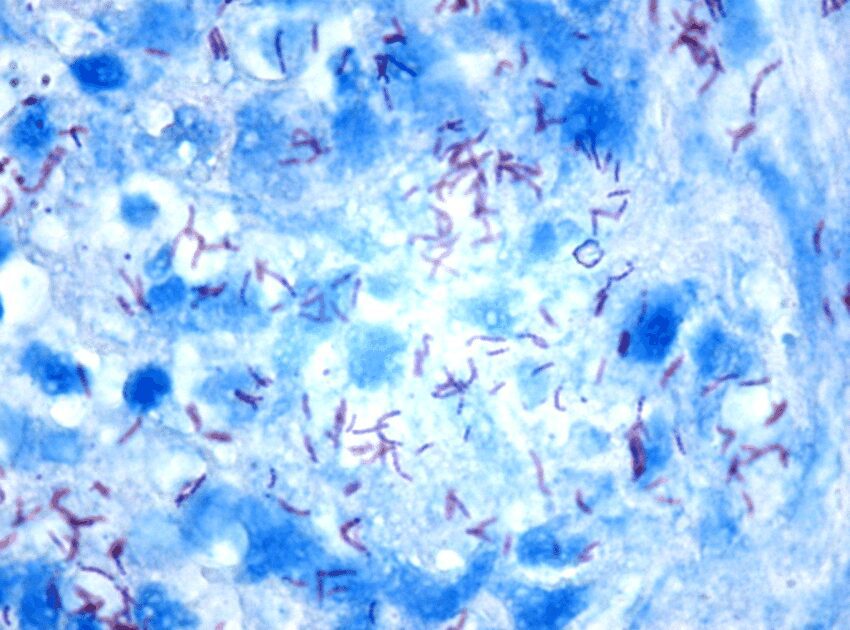
Metodi di Identificazione

La patologia da Mycobacterium tuberculosis si diagnosticata ricercando la presenza di germi acido-alcool-resistenti. La tecnica di colorazione di Ziehl-Nielsen è quella principalmente seguita. Altri esami colturali sono poi necessari per andare ad identificare il micobatterio. Inoltre, poiché il numero di micobatteri che possono essere presenti nei campioni biologici può essere molto basso, è facile intendere come, al contrario, molto alto sia il numero dei falsi negativi.
Particolare risalto è dato attualmente all’utilità della PCR per l’identificazione del Mycobacterium tuberculosis con i seguenti vantaggi: rapidità diagnostica (2 giorni contro 1 mese), diminuzione del rischio biologico, possibilità di mettere in evidenza il micobatterio anche quando la sua concentrazione è minima; diventa dunque possibile la sua ricerca nel sangue e/o espettorato. Inoltre, attraverso l’amplificazione della regione 16s – 23s dell’RNA ribosomiale, si ha la certezza di poter differenziare il Mycobacterium tuberculosis da altri Micobatteri e soprattutto questo è l’ unico sistema in grado di determinare la presenza vitale del Mycobacterium.
Terapia
Per il trattamento della tubercolosi vi è una gestione terapeutica sulla base di alcuni aspetti. In soggetti con TBC attiva senza coinvolgimento del sistema nervoso centrale le terapie prevedono una fase più aggressiva con l’uso di isoniazide (con piridossina), rifampicina, pirazinamide ed etambutolo per i primi 2 mesi, o isoniazide (con piridossina) e rifampicina per i successivi 4 mesi. Invece per i soggetti con TBC attiva del sistema nervoso centrale per una prima fase più aggressiva si utilizza l’isoniazide (con piridossina), rifampicina, pirazinamide ed etambutolo per i primi 2 mesi, successivamente si utilizza isoniazide (con piridossina) e rifampicina per gli ulteriori 10 mesi. In entrambi i casi successivamente alla prima fase più aggressiva, l’uso isoniazide (con piridossina) e rifampicina viene identificato come terapia di mantenimento.
Bisogna tenere conto che il regime terapeutico viene modificato sulla base di test di sensibilità ai farmaci.
Vengono, inoltre, utilizzate misure di prevenzione per prevenire la trasmissione, e alle volte è compreso anche l’isolamento respiratorio. Le mascherine chirurgiche facciali per la tubercolosi vengono raccomandate nei pazienti collaboranti. Le precauzioni sono necessarie fino a che il trattamento farmacologico non riduce significativamente la possibilità di contagio.
Per i pazienti con una significativa sensibilità al farmaco o tubercolosi multiresistente, le precauzioni sono mantenute sino al raggiungimento di una risposta clinica alla terapia (in genere, da 1 a 2 settimane). Nelle forme di tubercolosi a multi-resistenza estesa, la risposta alla terapia può essere più lenta, e vi è una maggiore conseguenza di trasmissione.