La globale emergenza sanitaria dovuta alla progressiva inservibilità dei trattamenti antibiotici, in caso di infezioni batteriche, guida ormai la ricerca verso i diretti responsabili microbici. Alcune sottopolazioni antibiotico-resistenti di Salmonella enterica, note come “persisters“, sono appena state chiamate in causa.
Le salmonellosi: tra sottospecie e sierotipi
Infezioni tra le più frequenti nell’uomo, le salmonellosi si distinguono in due tipologie:
- forme tifoidee, per le quali l’uomo rappresenta l’unico serbatoio del batterio;
- forme non tifoidee, con oltre 2000 varianti trasmesse all’uomo da alimenti contaminati di origine prevalentemente avicola.
Le forme non tifoidee sono, dunque, causate da Salmonelle definite “minori” o “zoonotiche”, come la Salmonella Typhimurium e la Salmonella Enteritidis. Si tratta di sierotipi (inglese serovar), cioè di ulteriori suddivisioni delle sottospecie, sulla base di presenza o meno di particolari elementi distintivi (antigeni).
La nomenclatura classica, quindi, per distinguerli anche graficamente dalle sottospecie, convenzionalmente assegna lettera maiuscola al nome che segue la specie: Salmonella Typhimurium, oppure, per esteso, Salmonella enterica subsp. enterica ser. Typhimurium.
Contagio, sintomi, degenerazioni
Le Salmonelle vivono nell‘intestino animale ed umano, sopravvivendo a lungo anche nell’ambiente, nonostante condizioni anche molto avverse.
La via d’infezione umana più comune è quella orale, per ingestione di alimenti contaminati: carni, uova e latte, consumati senza previo idoneo trattamento termico. Ma anche fonti idriche possono veicolare il pericoloso batterio di D. E. Salmon (1850-1914 Fig.1).

Figura 1 – D. E. Salmon (1850-1914) scopritore dell’omonimo ceppo batterico
Nell’uomo, la gravità dei sintomi varia notevolmente, passando da chiari disturbi gastro-intestinali con febbre (dolore addominale, nausea, vomito, diarrea), per giungere, in soggetti immuno-depressi, ad infezioni focali su ossa e meningi, con batteriemie.
Negli animali, invece, l’infezione da Salmonelle può decorrere silenziosamente ed asintomatica, pur lasciando i capi animali infettati “portatori sani” del batterio.
Se insisti e “persister” raggiungi e conquisti!
Parafrasando liberamente il grande Trilussa, si descrive pienamente l’efficacia microbiologica di queste tenaci sottopopolazioni batteriche.
Molte infezioni croniche da Salmonella, E. coli, Staphylococcus, Streptococcus, Pseudomonas e Mycobacterium sono particolarmente perniciose a causa dei loro stratagemmi genetici. La loro famigerata virulenza, infatti, origina già dalla scarsa sensibilità ai presidi antibiotici (Fig.2), dovuta, almeno in parte, alla presenza di persisters.
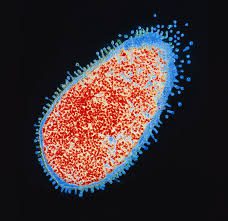
Figura 2 – Azione antibiotica su Salmonella Typhimurium (fonte Dr Kari Lounatmaa/science Photo Library)
Le cellule persisters non hanno acquisito mutazioni che donano loro resistenza antibiotica, ma praticano su di sè un cambio fenotipico transiente. Mediante adattamento reversibile della propria fisiologia, quindi, entrano in uno stato privo di crescita, in cui sono praticamente invulnerabili agli attacchi farmacologici. Queste cellule in “stato dormiente”, a trattamento antibiotico concluso, riprendono facilmente la propria crescita (“resurrezione”) proseguendo l’infezione, che al clinico apparirà intermittente. Tali scaltrissime cellule, inoltre, si differenziano in persisters in modo del tutto casuale e con una frequenza minima che può essere accelerata in risposta a segnali ambientali di pericolo per la sopravvivenza betterica.
Da comuni mortali a persisters
Dimensioni e composizione delle sottopolazioni persisters, nelle regolari comunità microbiche, sono costantemente controllate dal Sistema SOS di risposta allo stress.
In particolare, l’agente responsabile dello sviluppo di persisters è l’allarmone ppGpp: si tratta di una molecola-segnale che permette la sopravvivenza della cellula nel suo migliore stato fisiologico, anche in condizioni ambientali ostili. Tale molecola “dialoga” con il materiale genetico (mediante l’enzima RNA polimerasi), coordinando il rallentamento della sintesi proteica nelle cellule batteriche. Così si avvia il blocco temporaneo della crescita batterica, fino a superare i tempi grami sotto trattamento antibiotico.
La generazione di questi aspiranti highlander microbici è stata lentamente ottenuta in seguito a numerose risposte allo stress, causato dall’assunzione di dosi sub-letali di farmaci anti-microbici. Emerge, dunque, a monte, una responsabilità squisitamente umana nella proliferazione di popolazioni batteriche resistenti.
Persisters, untori di antibiotico-resistenza
Le cellule persister, oltre ad essere tolleranti agli antibiotici, sembrano diffondere la loro resistenza mediante particolari pathway di segnale. Tali cellule possono concorrere all’incremento di vere e proprie mutazioni genetiche, mediante l’attivazione di elementi genetici mobili (plasmidi).
Da cambio fenotipico individuale a trasmissione della resistenza: lo studio
I ricercatori, guidati da Erik Bakkeren dell’Institute of Microbiology Department of Biology di Zurigo (Svizzera), hanno indagato proprio se tali forme di persisters potessero anche favorire la diffusione di plasmidi resistenti ad altre popolazioni del microbiota intestinale umano.
Diversamente dalle mutazioni genetiche, il trasferimento di plasmidi resistenti richiede la contemporanea presenza di un ceppo batterico donatore e di uno ricevente.
I plasmidi sono filamenti di DNA batterico chiusi a formare un cerchio, a guisa di istruzioni di sopravvivenza “portatili” o “esportabili”: contengono, infatti, tutti i geni fondamentali per la vita della cellula che ne hanno storicamente consentito l’evoluzione ed il proverbiale adattamento.
Per i loro esperimenti, i ricercatori hanno selezionato, insieme al sierotipo Salmonella Typhimurium, anche il classico residente enterico E. coli.
Scoperti serbatoi duraturi di S.Typhimurium
Il ser. Typhimurium forma persisters che sopravvivono a terapie antibiotiche, in molti tessuti ospiti.
Dai dati emersi, i ricercatori dimostrano che tali sottopopolazioni “persistenti”, associate ai tessuti, possiedano un nutrito serbatoio di plasmidi donatori e riceventi. La creazione di queste scorte plasmidiche è garantita dalla presenza, nel genoma di Salmonella Typhimurium, dell’isola di patogenicità ISP-1 e/o di ISP-2 in tessuti associati intestinali o siti sistemici.
I geni che codificano per i classici effettori di patogenicità batterica, infatti, sono fisicamente riuniti in precisi segmenti di DNA, definiti isole di patogenicità, probabilmente acquisite orizzontalmente.
Trans-coniugazione genetica persisters-microbiota
La ri-semina, nel lume intestinale, effettuata dai ricercatori, ha mostrato la compresenza di ceppi donatori e riceventi intestinali resistenti, quindi si è registrata la capacità dei persisters di trasferire i propri plasmidi resistenti a vari ceppi di Enterobacteriaceae.
Bakkeren e colleghi hanno, quindi, osservato una trans-coniugazione genetica superiore al 99%, nell’arco di 2-3 giorni dalla ri-semina. Inoltre, modelli matematici hanno evidenziato che eventi pur sporadici di ri-semina siano sufficienti ad ottenere una elevatissima frequenza di coniugazione genetica. Questa “integrazione” diffonderà inesorabilmente la capacità batterica di resistenza agli antibiotici.
Meno frecce al nostro arco e più buonsenso
Una idonea vaccinazione, fortunatamente, riduce di molto la creazione di serbatoi di persisters post-infezione orale da Salmonella Typhimurium, contenendo, quindi, anche la trasmissione di plasmidi di resistenza agli antibiotici. Questa doverosa profilassi deve, però, rispecchiarsi anche in un habitus mentale sempre meno farmaco-dipendente.
Riferimenti bibliografici
- https://www.nature.com/articles/s41586-019-1521-8?fbclid=IwAR22gQURS6Twmdx2c-nNvy5ri0VYs4RNftE2yuQlTrM3ieSk3z_95RnHuBk
- https://www.nature.com/articles/nrmicro1614
- https://www.liebertpub.com/doi/abs/10.1089/fpd.2017.2403
- https://science.sciencemag.org/content/305/5690/1622
I commenti sono chiusi.