Il syngas o gas di sintesi
Il gas di sintesi o syngas è la miscela gassosa ottenuta dal processo di gassificazione termica di biomasse, rifiuti organici e/o rifiuti plastici. La produzione di syngas avviene a temperature elevate (superiori a 700-800 °C) in presenza di un quantitativo sotto stechiometrico di un agente ossidante. Quest’ultimo è tipicamente rappresentato da aria, ossigeno o vapore.
Da un punto di vista chimico, il syngas è costituito essenzialmente da monossido di carbonio (CO) e idrogeno (H2), insieme ad una quantità minoritaria variabile di metano (CH4) e anidride carbonica (CO2). Il gas di sintesi non va confuso con il biogas, il quale è ottenuto da processi di digestione anaerobica di materiale organico. Inoltre, il biogas è costituito prevalentemente da anidride carbonica e metano.
Il syngas presenta numerose applicazioni industriali e rappresenta una promettente fonte di energia rinnovabile in quanto deriva da biomasse e rifiuti organici. Solitamente, esso viene impiegato come combustibile, per generare energia elettrica attraverso l’uso di una turbina a gas, motore a ciclo diesel o in modo diretto tramite le pile a combustibile (fuel cells) di tipo DMFC; come reagente, ad esempio nel processo Fischer-Tropsch; come fonte di idrogeno, ad esempio per la sintesi di ammoniaca o per la produzione di energia elettrica mediante celle a combustibile a carbonati fusi (Fig. 1).

Un nuovo modello di bioraffineria del syngas
Un’innovativa applicazione del syngas consiste nella sua fermentazione in processi di bioraffineria per la produzione di molecole a valore aggiunto. Tali prodotti a base biologica sono rappresentati prevalentemente da etanolo e acidi organici volatili (AOV), come acido acetico, acido propionico, acido butirrico e acido esanoico (Fig. 2).
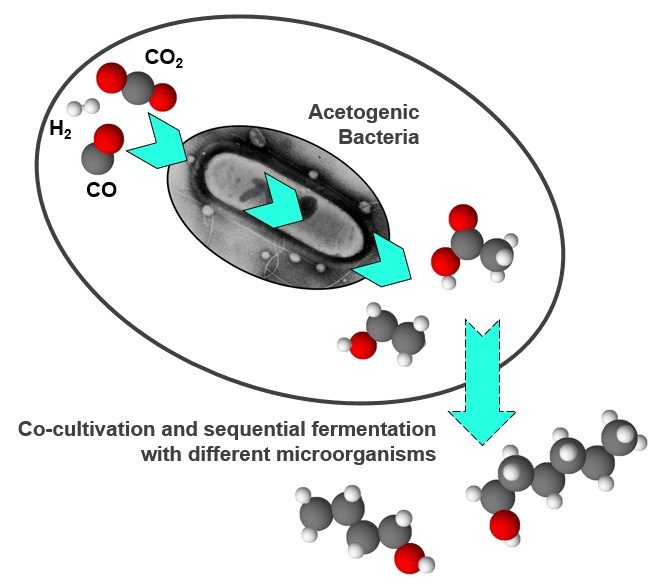
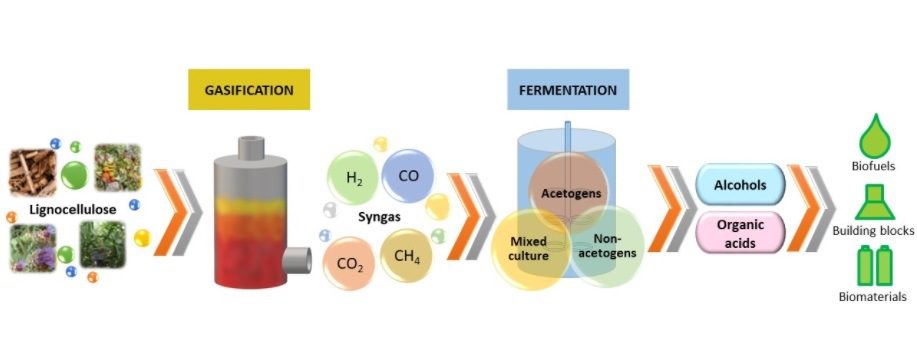
Da un punto di vista di processo, dopo lo step di gassificazione delle biomasse e la bioconversione del syngas in alcoli e acidi organici, le molecole prodotte potrebbero essere utilizzate per la produzione di biocarburanti (es. bioetanolo), prodotti chimici di intesse farmaceutico, nutraceutico e industriale, e biomateriali (es. bioplastiche) (Fig. 3).
La fermentazione del gas di sintesi avviene in bioreattori caratterizzati da un design ad hoc (Fig. 4) in grado di massimizzare il trasferimento di massa del gas, ossia della fonte di carbonio dei microrganismi, nel mezzo di coltura.

La fermentazione del syngas
I microrganismi maggiormente utilizzati nei processi di fermentazione del syngas, singolarmente o in colture miste, sono batteri appartenenti principalmente alle specie Clostridium aceticum (per la produzione di acido acetico) Butyribacterium methylotrophicum, Clostridium drakei, Clostridium scatologenes (per la produzione di butanolo) Clostridium carboxidivorans (per la produzione di butanolo e tracce di esanolo e acido esanoico), Clostridium ragsdalei (per la produzione di etanolo e AOV).
I batteri più adoperati in processi su scala industriale sono gli acetogeni, ossia microrganismi anaerobi obbligati in grado di utilizzare CO e/o CO2 insieme all’H2 per produrre acidi organici, alcoli e altri prodotti chimici di rilevanza industriale. Ad oggi, più di 100 specie acetogeniche sono note, appartenenti a 22 generi, le quali sono state isolate da habitat diversi.
Acetobacterium e Clostridium sono i più rappresentativi di questi generi. Nonostante l’ampia diversità metabolica esistente tra questi microrganismi, per la fermentazione del syngas viene comunemente utilizzata la via metabolica Wood – Ljungdahl (Fig. 5).
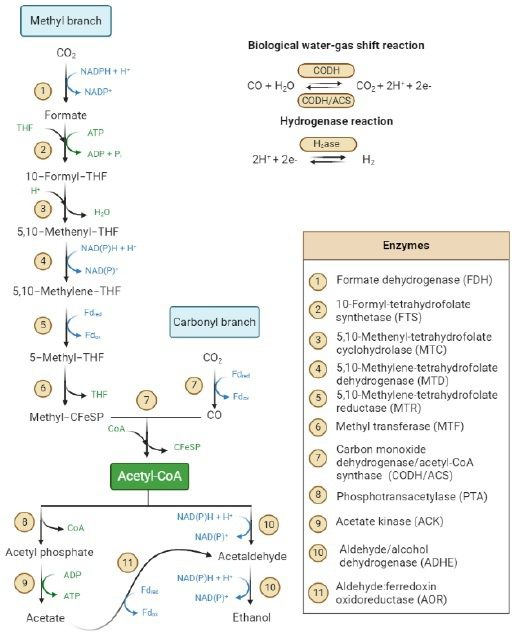
Vantaggi dei modelli di bioraffineria basati sul syngas
I vantaggi di questo moderno schema di bioraffineria ibrido, basato su processi di conversione termica e biologica, consistono in:
- Come in qualsiasi gassificazione, è indifferente la tipologia e la composizione chimica della biomassa utilizzata;
- È ottenuta una completa conversione della biomassa lignocellulosica, inclusa la lignina;
- Comparando la composizione chimica ed il costo del glucosio con quelli della CO2 del syngas si ottiene che il carbonio del glucosio ha un costo pari a 0,875 euro/kg mentre il carbonio del gas di sintesi ha un costo circa cinque volte inferiore pari a 0,185 euro/kg;
- I biocatalizzatori microbici sono altamente selettivi per la produzione di etanolo mentre impiegando i catalizzatori chimici si ottiene un ampio spettro di prodotti di reazione;
- Molti dei batteri sono tolleranti ai contaminanti presenti nel syngas (composti a base di cloro e zolfo), i quali, anche in tracce, possono facilmente avvelenare i catalizzatori metallici;
- La fermentazione è condotta a valori ambientali di pressione e temperatura, riducendo significativamente i costi del processo di conversione;
Sfide della fermentazione del syngas
Al contempo, però, vi sono ancora diverse sfide scientifiche e limitazioni che la ricerca sta cercando di risolvere al fine di assicurare una piena sostenibilità tecnologica ed economica di questo moderno processo biotecnologico.
Tali limitazioni sono rappresentate da:
- Limitazioni nel trasferimento di massa del gas nel liquido di fermentazione;
- Bassa produttività di etanolo, di solito correlata ad una bassa densità cellulare causata dalla produzione di sottoprodotti tossici del metabolismo microbico;
- Sensibilità dei microrganismi alle condizioni ambientali (pH, ossigenazione, potenziale redox).
La fermentazione del syngas è una promettente tecnologia per la conversione di gas ricchi di CO e CO2 in una varietà di preziose sostanze chimiche. Biomasse lignocellulosiche, rifiuti solidi urbani e rifiuti polimerici sono materie prime adatte per la gassificazione. Tuttavia, l’aumento delle rese di processo e l’incremento del trasferimento di massa del gas nel mezzo di coltura rappresentano le due principali sfide che questa tecnologia dovrà affrontare nei prossimi anni.
Nicola Di Fidio
Sitografia:
- SynPol project (2012-2016). Biopolymers from Syngas Fermentation. Estrapolato da: http://www.synpol.org/www-synpol-org/
- Francesco Centorrino (26 agosto 2016, Microbiologia Italia). Biocarburante in arrivo: tutto merito di Clostridium ljungdahlii! Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/biocarburante-arrivo-merito-clostridium-ljungdahlii/
- Nicola Di Fidio (11 aprile 2018, Microbiologia Italia). Dalle raffinerie alle bioraffinerie grazie a batteri, lieviti e microalghe. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/dalle-raffinerie-alle-bioraffinerie-grazie-a-batteri-lieviti-e-microalghe/
- Nicola Di Fidio (28 agosto 2019, Microbiologia Italia). Sinergia tra batteri metanogeni, acidogeni e solfobatteri per la produzione di biometano. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/sinergia-tra-batteri-metanogeni-acidogeni-e-solfobatteri-per-la-produzione-di-biometano/
- F. Battista (febbraio 2015, Verticale Contenuti Tecnico Scientifici). Fermentazione di gas: un’innovativa fonte di carbonio. Estrapolato da: https://www.verticale.net/fermentazione-di-gas-un-innovativa-fonte-8823
Bibliografia:
- Ciliberti, C., Biundo, A., Albergo, R., Agrimi, G., Braccio, G., de Bari, I., & Pisano, I. (2020). Syngas Derived from Lignocellulosic Biomass Gasification as an Alternative Resource for Innovative Bioprocesses. Processes, 8(12), 1567.
- Phillips, J. R., Huhnke, R. L., & Atiyeh, H. K. (2017). Syngas fermentation: a microbial conversion process of gaseous substrates to various products. Fermentation, 3(2), 28.
- Stoll, I. K., Boukis, N., & Sauer, J. (2020). Syngas fermentation to alcohols: reactor technology and application perspective. Chemie Ingenieur Technik, 92(1-2), 125-136.
- Sahoo, J., Patil, P., Verma, A., Lodh, A., Khanna, N., Prasad, R., & Fosso-Kankeu, E. (2021). Biochemical aspects of syngas fermentation. In Recent Developments in Microbial Technologies (pp. 395-424). Springer, Singapore.
Crediti immagini:
- Immagine in evidenza – https://www.ikft.kit.edu/english/695.php
- Fig. 1 – http://procone.org/applications.html
- Fig. 2 – https://www.ikft.kit.edu/english/695.php
- Fig. 3 – https://doi.org/10.3390/pr8121567
- Fig. 4 – https://doi.org/10.1016/j.apenergy.2016.11.084
- Fig. 5 – https://doi.org/10.3390/pr8121567