La nicotinamide adenin dinucleotide, semplificato NADH, è un coenzima idrosolubile naturalmente presente nell’organismo. Svolge un ruolo fondamentale nelle vie biochimiche che portano alla produzione di energia poiché fornisce un importante supporto nel funzionamento di alcuni enzimi andando incontro ad ossidazioni e riduzioni reversibili in molte reazioni di trasferimento di elettroni del metabolismo. L’associazione con un dato enzima è relativamente debole poiché il coenzima diffonde facilmente dalla superficie di un catalizzatore a quella di un altro, agendo, quindi, come trasportatore di elettroni da un metabolita ad un altro.
Scoperta e caratterizzazione del NADH
Il NADH fu scoperto nel 1906 da due biochimici britannici: Arthur Harden e William John Young, i quali, notarono che un estratto di lievito era in grado di accelerare la reazione di fermentazione alcolica. In particolare, scoprirono l’esistenza di due frazioni presenti all’interno delle cellule di lievito: una termosensibile e l’altra termoresistente. Dopo averle separate, si accorsero che la prima frazione non era in grado da sola di effettuare il processo fermentativo. Supposero, pertanto, l’esistenza di proteine responsabili della fermentazione nella frazione termosensibile e l’esistenza di cofattori o altre molecole che aiutassero il processo fermentativo nella frazione termoresistente. Solo diversi anni dopo, alcuni biochimici tedeschi isolarono la molecola del NADH dal lievito di birra e dagli eritrociti. Successivamente, nel 1957, il chimico scozzese Alexander R. Todd vinse il premio Nobel per la chimica con il merito di aver rappresentato la struttura del NAD.
Struttura molecolare
Chimicamente, il NADH è composto da due nucleotidi uniti insieme da un legame fosfoanidridico tra due gruppi fosforici. Le due basi azotate, che compongono i nucleotidi, sono l’adenina e la niacinammide. Quest’ultima, in particolare, deriva dalla niacina (vitamina B3) e svolge il ruolo principale nella molecola del NADH poiché dona/accetta atomi d’idrogeno implicati nelle razioni di ossidoriduzione.
Quando una molecola di substrato va incontro ad una ossidazione o deidrogenazione, perde due atomi di idrogeno. Di conseguenza, la forma ossidata del coenzima (NAD+) si trasforma nella forma ridotta (NADH) accettando uno ione idruro (costituito da un protone e due elettroni). Il secondo H+ rimosso dal substrato, viene invece rilasciato nel solvente acquoso.
La semi reazione è, quindi, la seguente: NAD+ + 2e¯ + 2H + –> NADH + H+
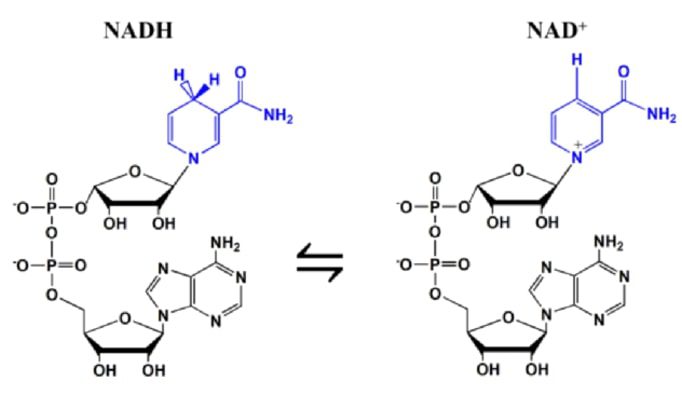
Si conoscono più di 200 ossidoreduttasi o deidrogenasi che catalizzano reazioni in cui il NAD+ accetta uno ione idruro da un substrato ridotto oppure in cui il NADH dona uno ione idruro ad un substrato ossidato. Ad esempio, l’enzima alcol deidrogenasi catalizza la prima reazione del catabolismo dell’etanolo in cui l’alcol viene ossidato ad acetaldeide.
CH₃CH₂OH + NAD+ –> CH₃CHO + NADH + H+
Integratori di NADH
Come già accennato, il NADH è un elemento chiave per la produzione di ATP poiché partecipa al trasferimento degli elettroni nelle reazioni del metabolismo energetico. I supplementi dietetici a base di NADH potrebbero, quindi, aiutare a ridurre la pressione arteriosa e i livelli di colesterolo nel sangue, nonché a fornire all’organismo un surplus di energia utile a combattere tutte quelle condizioni caratterizzate da carenza di energia ed affaticamento cronico.
Controindicazioni
Non esistono, ad oggi, studi che abbiano dimostrato che gli integratori alimentari a base di NADH possano causare effetti collaterali nella persona o interferire con farmaci o con il consumo di altre sostanze a patto che si seguano le istruzioni riportate sull’etichetta del prodotto. Tuttavia, sarebbe opportuno evitare l’assunzione in gravidanza o durante la fase di allattamento.
Fonti
- Nicotinammide adenina dinucleotide (NAD) (chimicamo.org)
- NADH (nicotinammide adenina dinucleotide) | Istituto Clinico Catanese – Humanitas Catania
- NAD+ metabolism: pathophysiologic mechanisms and therapeutic potential | Signal Transduction and Targeted Therapy (nature.com).
Fonti immagini
- Immagine in evidenza: https://images.fineartamerica.com/images-medium-large-5/nadh-dehydrogenase-molecule-artwork-science-photo-library.jpg
- Figura 1 – Structure of NADH and NAD + and the electrochemical oxidation process… | Download Scientific Diagram (researchgate.net)