La catena di trasporto degli elettroni ha sede nei mitocondri, e può essere descritta come la serie di complessi proteici grazie a cui avvengono le reazioni redox fondamentali per la vita.
I mitocondri nella produzione di energia
Tutte le cellule eucariotiche contengono organelli legati alla membrana con funzioni specializzate. I mitocondri sono organelli a doppia membrana che producono la maggior parte dell’energia di cui le cellule necessitano per crescere e riprodursi. Inoltre, molta di questa energia proviene da reazioni chimiche che avvengono nella membrana mitocondriale interna, che funge da barriera per le particelle cariche positivamente (protoni). Grazie a questa si ha il mantenimento di un gradiente di concentrazione in cui la membrana interna ha una concentrazione maggiore di protoni rispetto alla matrice. Questa membrana contiene anche l’enzima ATP sintasi, che utilizza il gradiente protonico come forza motrice per produrre molecole di ATP. Queste molecole di ATP poi, sono quelle che provvederanno a fornire l’energia necessaria alla maggioranza delle reazioni chimiche della cellula.
Più semplicemente, possiamo visualizzare la ATP sintasi come una turbina eolica che sfrutta l’energia cinetica del vento (gradiente protonico) per muoversi e infine produrre energia (molecole di ATP).
In questo contesto è chiaro che in assenza di gradiente protonico i mitocondri non sono in grado di produrre ATP, e così la cellula può rapidamente divenire carente di energia e morire. Per questo, la catena di trasporto degli elettroni che genera il gradiente protonico e lo mantiene nel tempo è fondamentale per la vita della cellula.
Organizzazione della catena di trasporto degli elettroni
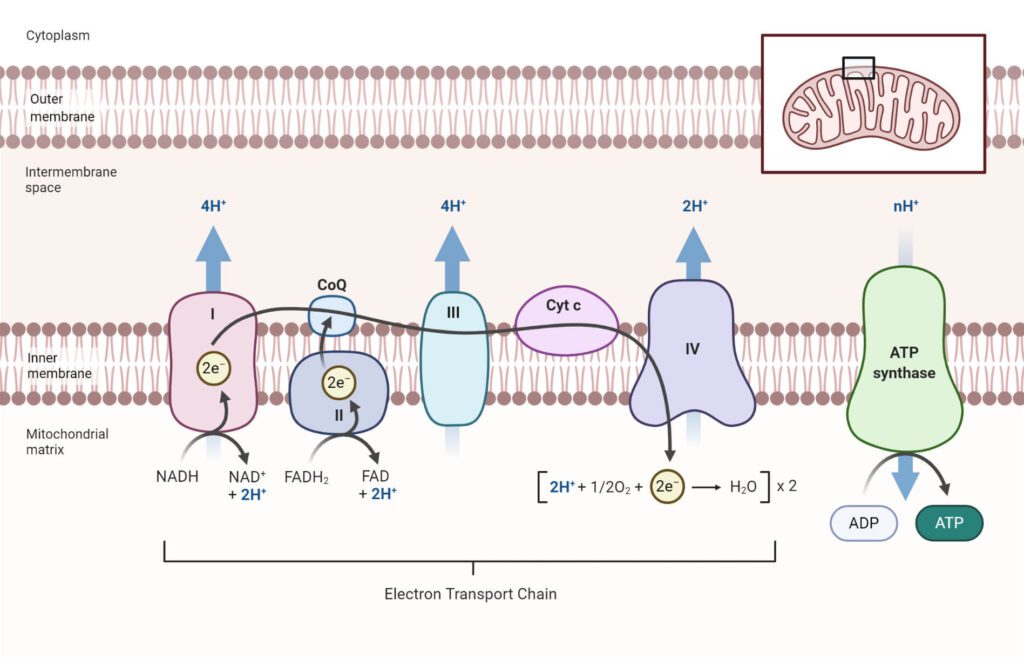
La catena di trasporto degli elettroni è composta da quattro complessi enzimatici legati alla membrana interna mitocondriale:
- complesso I (CI) – NADH deidrogenasi;
- complesso II (CII) – Succinato deidrogenasi;
- complesso III (CIII) – citocromo bc1;
- complesso IV (CIV) – citocromo c ossidasi;
questi, insieme al complesso V (o ATP sintasi) fanno parte del processo biochimico della fosforilazione ossidativa.

Gli step del trasporto degli elettroni
Da NADH a Coenzima Q
CI è il punto di entrata nella catena di trasporto degli elettroni. A partire dal NADH, questo enzima catalizza la riduzione del coenzima Q a QH2. Simultaneamente, trasferisce quattro protoni (H+) dalla matrice mitocondriale allo spazio intermembrana. Nello specifico di questa reazione, due elettroni vengono trasferiti dal NADH a una flavoproteina contenente il cofattore FMN. Poi, FMN così ridotto trasferisce gli elettroni uno ad uno a una catena di sette centri ferro-zolfo (Fe-S). Successivamente Il centro Fe-S N2, l’ultimo della catena, dona due elettroni al coenzima Q, riducendolo all’intermedio semichinone (QH·) e infine a ubichinolo (QH2).
Il coenzima Q può essere ridotto anche attraverso il CII, l’unico enzima del ciclo di Krebs (TCA cycle) legato alla membrana interna mitocondriale. Infatti, questo enzima catalizza l’ossidazione del succinato a fumarato con la concomitante riduzione dell’ubichinone a ubichinolo. In dettaglio, dal succinato gli elettroni passano attraverso una flavoproteina contenente il cofattore FAD e svariati centri Fe-S. Infine, gli elettroni sono trasferiti al coenzima Q, che viene così ridotto a QH2.
Da QH2 a citocromo c (Ciclo Q)
CIII accoppia il trasferimento degli elettroni da QH2 al citocromo c (proteina solubile debolmente associata alla membrana) con il trasferimento di protoni dalla matrice allo spazio intermembrana. Questa serie di reazioni prende il nome di ciclo Q, dal momento che si tratta di un trasferimento elettronico continuo e sequenziale. Nello specifico, questo ciclo regola il trasferimento di elettroni da un trasportatore a due elettroni (QH2) a dei trasportatori a un elettrone (i gruppi eme dei citocromi b e c). Il risultato netto è che QH2 viene ossidato a Q, mentre due molecole di citocromo c sono simultaneamente ridotte e i protoni risultanti trasferiti nello spazio intermembrana.
Da citocromo c a O2
Successivamente, Il citocromo c (ormai ridotto) che è una molecola fortemente solubile in acqua, si muove e trasferisce così un elettrone a uno dei centri bi-nucleari Cu2+ (centro di rame) dell’enzima CIV.
Nell’ultimo step della catena di trasporto degli elettroni, il CIV trasferisce le sue particelle cariche negativamente dal citocromo c all’ossigeno molecolare (O2). O2 in questo modo si riduce a una molecola d’acqua (H2O). In assenza di ossigeno, questo trasferimento elettronico viene interrotto e così anche la produzione di ATP a valle. Infatti, la ragione per cui respiriamo ossigeno è che in questo modo può essere utilizzato come accettore di elettroni finale nella catena di trasporto degli elettroni, e permettere la produzione di energia sottoforma di ATP.
Ogni volta che quattro elettroni sono donati al CIV, l’enzima preleva altrettanti H+ dalla matrice per convertire O2 in due molecole di H2O. Il complesso IV inoltre utilizza l’energia di questa reazione redox per pompare nello spazio intermembrana un protone per ogni elettrone che lo attraversa.
Resa della catena di trasporto degli elettroni
Nel suo insieme, la catena di trasporto degli elettroni a partire dal NADH genera la traslocazione di 10 ioni H+ dalla matrice allo spazio intermembrana. In questo processo, i complessi CI, CIII e CIV sono direttamente coinvolti nella traslocazione dei protoni. In particolare, per ogni molecola di NADH si producono 2.5 molecole di ATP. Infatti, i due gradienti (protonico ed elettronico) formano insieme la forza motrice protonica. Questa è proprio la forza che spinge ogni singolo protone attraverso il complesso V (CV), ovvero la ATP sintasi. In questo modo avviene la sintesi di ATP a partire dall’ADP e il fosfato inorganico (Pi).
In conclusione, a partire dai prodotti dal catabolismo ossidativo, grazie alla catena di trasporto degli elettroni, si produce la maggior parte dell’energia necessaria alla vita e alla riproduzione della cellula.
Fonti
- Zorova, Ljubava D et al. “Mitochondrial membrane potential.” Analytical biochemistry vol. 552 (2018).
- Vercellino, Irene, and Leonid A Sazanov. “The assembly, regulation and function of the mitochondrial respiratory chain.” Nature reviews. Molecular cell biology vol. 23,2 (2022).
- Guo, Runyu et al. “Structure and mechanism of mitochondrial electron transport chain.” Biomedical journal vol. 41,1 (2018).
Crediti immagini
- Immagine in evidenza: sciencedirect.com/science/article/abs/pii/S0925231219313384.
- Figura 1: creata con biorender.com
- Figura 2: pubmed.ncbi.nlm.nih.gov/34621061/