Perché colpire la membrana cellulare batterica con gli antibiotici?
La membrana cellulare batterica rappresenta un bersaglio terapeutico strategico nei confronti dei batteri patogeni.
Gli antibiotici rappresentano una terapia selettiva contro questi microrganismi ma, nel tempo, l’emergere di meccanismi di resistenza (AMR) ha considerevolmente ridotto la loro efficacia. Questo fenomeno è largamente diffuso sia per classi comuni come penicilline e cefalosporine, che per alcune più specifiche come i glicopeptidi.
La maggior parte di questi farmaci esercita la propria azione attraverso meccanismi selettivi nei confronti della cellula batterica quali: la sintesi della parete, la produzione di proteine o la replicazione del DNA.
In alcuni casi il bersaglio non è un enzima o una via metabolica, bensì una struttura fondamentale come la membrana cellulare.
Membrana cellulare batterica nei gram positivi e nei gram negativi
Non tutti i batteri, però, presentano la stessa organizzazione dell’involucro cellulare. Una maggior comprensione della membrana cellulare batterica deriva dalla tecnica proposta dal batteriologo danese Hans Christian Gram nel 1884. Le differenze strutturali più rilevanti, tra Gram positivi e Gram negativi, sono le seguenti:
Gram +
- Possiedono una sola membrana cellulare.
- Esternamente presentano una parete spessa formata da un’alta percentuale di peptidoglicano.
Gram –
- Possiedono due membrane, una citoplasmatica interna ed una esterna ricca di polisaccaridi (LPS).
- La parete di peptidoglicano è più sottile, ma è protetta all’interno dello spazio tra le due membrane.
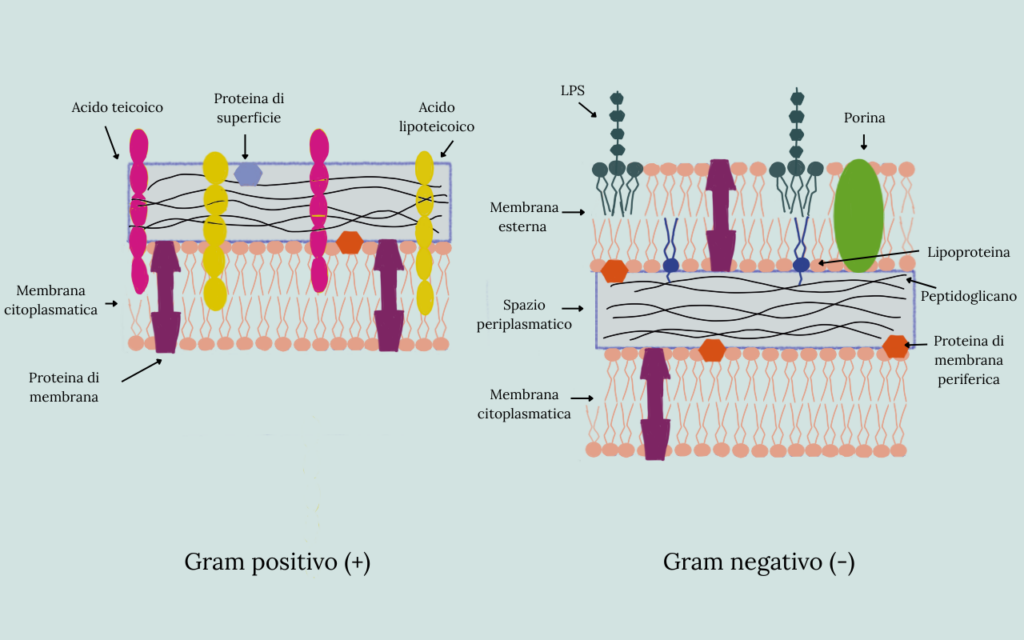
Le differenze strutturali influenzano l’accessibilità e la vulnerabilità della membrana cellulare batterica, determinando come alcuni antibiotici risultino efficaci solo contro specifici gruppi di batteri.
Perché la membrana cellulare batterica è un bersaglio efficace?
La membrana cellulare batterica è costituita da un doppio strato fosfolipidico semipermeabile che controlla il passaggio di ioni e nutrienti ospitando enzimi essenziali per il metabolismo energetico. La sua integrità è determinante per il mantenimento del potenziale di membrana e la sopravvivenza del batterio stesso.
A differenza di bersagli ancor più selettivi la membrana cellulare batterica è una struttura condivisa, seppur con alcune variazioni sulla composizione lipidica, anche dalle cellule dell’ospite. Per tale motivo alcuni di questi antibiotici esprimono un certo grado di tossicità che ne limita l’impiego clinico a situazioni particolari come le infezioni multiresistenti o la ricerca.
Antibiotici di membrana: quali sono e come agiscono
Le molecole antibiotiche ad azione diretta contro la membrana cellulare batterica hanno un bersaglio che non è un enzima specifico, ma una vera e propria entità strutturale.
La composizione della membrana è strettamente connessa ai meccanismi d’azione di questi antibiotici. In base alla struttura molecolare del singolo farmaco si attuano procedimenti diversi quali: alterazione della permeabilità di membrana attraverso la formazione di pori, variazione della struttura lipidica oppure depolarizzazione.
Il risultato è un’intensa e rapida azione battericida.
Polimixine
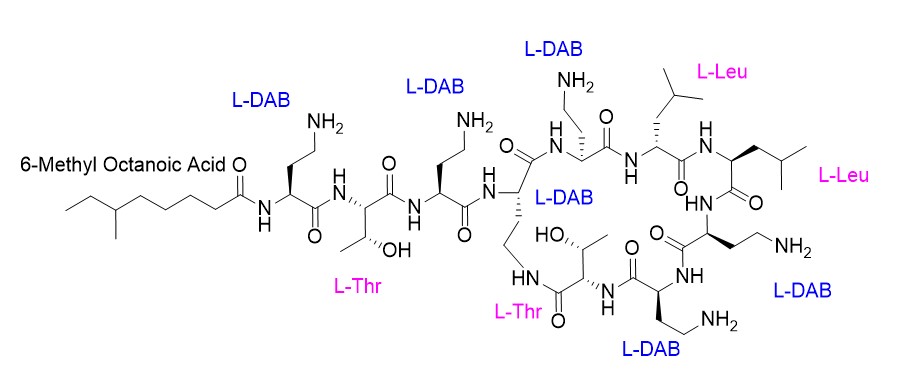
Questa classe di antibiotici è stata scoperta a metà degli anni ’40: la polimixina B nel 1947 e la polimixina E, anche detta colistina, nel 1949 quando venne isolata da Paenibacillus polymyxa var. colistinus.
Queste molecole sono attive principalmente nei confronti dei batteri gram negativi (-) in quanto operano un legame con i lipopolisaccaridi (LPS) della membrana esterna. L’interazione che si forma è di natura elettrostatica e provoca la dislocazione di ioni Ca2+ e Mg2+ responsabili dell’instabilità di tale membrana e della successiva penetrazione nello spazio periplasmatico. L’antibiotico porta alla disorganizzazione della membrana citoplasmatica che, infine, determina la perdita di contenuto cellulare e l’effetto battericida.
Tra i vari meccanismi di resistenza sviluppatisi uno dei più preoccupanti è quello legato al gene mcr (mobilized colistin resistance). Codificante per una fosfoetanolamina-transferasi, modifica il lipide A e compromette l’attacco della colistina; a differenza dei meccanismi di resistenza cromosomici “verticali” il gene mcr è plasmidico e può, quindi, trasferirsi orizzontalmente tra le varie specie batteriche con maggior rapidità.
Vengono utilizzate limitatamente contro batteri resistenti come Pseudomonas aeruginosa e Acinetobacter baumannii a causa della loro neurotossicità e nefrotossicità.
Daptomicina
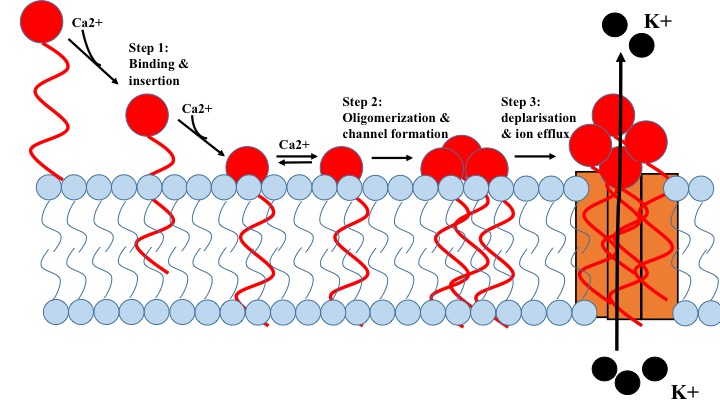
La daptomicina è un antibiotico scoperto nel 1983 ed approvato per uso clinico solo nel 2003. Identificato attraverso un campione di terreno del monte Ararat in Turchia deriva dalla caratterizzazione del ceppo batterico Streptomyces roseosporus.
La sua tossicità si riduce notevolmente con la somministrazione di un’unica dose giornaliera anziché con tre più piccole, mantenendo inalterata l’efficacia clinica. Il suo spettro d’azione è limitato ai gram positivi (+) e risulta utile nel trattamento di batteri multiresistenti come Enterococcus Faecalis, anche se di recente sta subendo meccanismi di resistenza sempre più frequenti.
La daptomicina necessita obbligatoriamente della presenza di ioni Ca2+ per completare il suo legame al fosfatidilglicerolo e svolgere l’attività battericida. Tale congiunzione determina un’aumentata permeabilità della membrana dove questa molecola, inserendosi, genera oligocomplessi determinanti:
- Depolarizzazione rapida.
- Perdita di potenziale di membrana.
Conseguenza diretta della perdita del potenziale di membrana è anche l’arresto della sintesi di DNA, RNA e proteine.
Studi recenti indicano che la daptomicina possa alterare i microdomini funzionali della membrana, delocalizzando proteine chiave per la sintesi della parete e la divisione cellulare.
Gramicidina
La gramicidina A (gA) è un peptide lineare componente del complesso delle gramicidine lineari. Questa miscela, prodotta da Bacillus brevis, è costituita da più isoforme strutturalmente correlate (indicate come gramicidina A, B e C). La gA è la frazione predominante e svolge l’azione battericida mediante due meccanismi:
- A dosaggi bassi (≤ 1 μM ) si inserisce nella membrana e attraverso la realizzazione di un canale, che consente il passaggio di cationi monovalenti (H+, Na+ e K+), è responsabile del collasso del gradiente elettrochimico e della perdita del potenziale di membrana (possibilmente con uno squilibrio del metabolismo dell’NADH e con la formazione di radicali liberi idrossilici).
- A dosaggi maggiori (≥5 μM) molte molecole si inseriscono nel doppio strato e, cambiando la disposizione dei fosfolipidi, l’organizzazione di membrana si perde generando un effetto battericida più intenso.
Gli ioni Ca²⁺ sono responsabili di un’azione inibente l’attività battericida, tale effetto si produce in modo significativo solo a basse concentrazioni di gA, ovvero quando il meccanismo prevalente è la formazione del canale ionico; mentre a concentrazioni più elevate la destabilizzazione strutturale della membrana rende l’inibizione meno efficace.
Le gramicidine vengono utilizzate come strumento terapeutico per infezioni superficiali, risultano al contrario troppo tossiche per uso sistemico.
Valinomicina
La valinomicina è stata isolata per la prima volta nel 1955 da Streptomyces fulvissimus. Nota da decenni, la sua tossicità spiccata la rende utile per uso sperimentale piuttosto che come alternativa clinica per infezioni batteriche.
Agisce principalmente contro i batteri gram positivi (+) dal momento che la membrana esterna dei gram negativi (-) riesce ad impedire selettivamente l’accesso intracellulare all’antibiotico.
Esercita la sua azione come ionoforo potassio-specifico determinando la dissipazione del gradiente ionico e la compromissione della sintesi proteica.
Limiti, resistenze e ruolo clinico attuale
Questi antibiotici restano molecole di impiego selezionato, nonostante il loro potente effetto battericida.
La comparsa di meccanismi di resistenza come: le modificazioni del lipopolisaccaride nei Gram negativi (-), che riduce l’affinità per le polimixine, o le alterazioni della composizione lipidica nei Gram positivi (+), che compromettono l’attività della daptomicina, ne hanno ulteriormente limitato l’utilizzo.
Si tratta quindi di farmaci preziosi da riservare a contesti clinici specifici dove il rapporto tra efficacia e sicurezza risulti favorevole.
Fonti
- Iss – batterio
- MSDmanuals – batteri e farmaci antibatterici
- UniFe – batteriologia delle infezioni
- MSDmanuals – polimixina B
- Britannica – antibiotic
- Ledger, E. V. K., Sabnis, A., & Edwards, A. M. (2022). Polymyxin and lipopeptide antibiotics: membrane-targeting drugs of last resort. Microbiology (Reading, England), 168(2), 001136. https://doi.org/10.1099/mic.0.001136
- Epand, Richard M et al. “Molecular mechanisms of membrane targeting antibiotics.” Biochimica et biophysica acta vol. 1858,5 (2016): 980-7. doi:10.1016/j.bbamem.2015.10.018
- Fang, Shang-Ting et al. “Effects of Calcium Ions on the Antimicrobial Activity of Gramicidin A.” Biomolecules vol. 12,12 1799. 1 Dec. 2022, doi:10.3390/biom12121799
- Huang, Shuhui et al. “The Nonribosomal Peptide Valinomycin: From Discovery to Bioactivity and Biosynthesis.” Microorganisms vol. 9,4 780. 8 Apr. 2021, doi:10.3390/microorganisms9040780
Immagini
- Immagine in evidenza – Di DFID – UK Department for International Development – A variety of different bacteria – testing for antimicrobial resistance, CC BY 2.0, https://commons.wikimedia.org/w/index.php?curid=96027057
- Figura 1 – Schema semplificato della struttura di batteri Gram positivi e Gram negativi. Rappresentazione grafica originale a scopo illustrativo.
- Figura 2 – Di Turner.mb007 – Opera propria, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=59835076
- Figura 3 – By Drakosam – Own work, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=49676714