Siamo quasi al termine del 2021 e siamo ancora nel pieno di una pandemia che ci costringe a varie restrizioni da ben due anni ormai, ossia quella causata dal COVID-19. Si fanno ancora speculazioni a riguardo di ciò che abbia causato la diffusione di questo virus. L’idea principale è che la trasmissione sia partita da specie animali con le quali l’uomo è entrato in contatto, infettandosi. Ma qual è l’animale che per eccellenza ad oggi provoca la diffusione della maggior parte di virus estremamente pericolosi per l’uomo? Le zanzare.

Un animale estremamente pericoloso per l’uomo
Le zanzare sono tra gli animali più letali al mondo e uccidono più esseri umani sulla terra di qualsiasi altro animale. Com’è possibile che accada una cosa del genere? Il motivo è semplice. Permettono la diffusione di un buon numero di virus estremamente dannosi per il genere umano. Il genere Aedes, ad esempio, induce la propagazione dei famigerati arbovirus, parola che deriva dall’inglese arthropod-borne viruses, che indica che la maggior parte di questi si sviluppa negli artropodi. Questi possono provocare diverse infezioni, quali:
- l’infezione da virus Zika, di cui il primo caso di infezione nell’uomo risale al 1968 in Nigeria, ma che poi è stata riscontrata anche in altri casi, tra il 2013 e il 2014, in Italia;
- la febbre gialla, diffusa principalmente tra Asia e Sud America;
- la dengue, la quale ha indotto numerose epidemie in Asia, Africa e Nord America;
- la Chikungunya, di cui il primo caso di infezione nell’uomo fu riscontrato nel 1963 in India, anche se questa patologia è stata in grado di generare una piccola epidemia pure in Emilia-Romagna, tra il 2004 e il 2005.
Attualmente il vaccino esiste solo per combattere il diffondersi di alcune di queste malattie. Per esempio, esiste quello contro la dengue. Nonostante, questo sia stato registrato in diversi paesi, però, non è ancora ampiamente utilizzato. Per la febbre gialla, invece, esiste un vaccino di vecchia data che viene utilizzato in tutto il mondo. Tuttavia, i fondi per la vaccinazione di routine sono limitati. Inoltre, per queste malattie non sono disponibili opzioni di profilassi, il che significa che la trasmissione non si interrompe durante la fase di infezione umana.
Le soluzioni attuate sino ad ora
La strategia predominante per controllare queste malattie devastanti è l’uso di insetticidi. Le zanzare, però, nel frattempo si sono evolute, sviluppando una forte resistenza a queste sostante. Approcci alternativi includono l’infezione da Wolbachia o l’uso di antibiotici, i quali però sono stati testati solo in luoghi ristretti in tutto il mondo.

Wolbachia spp. è un genere di alfa-proteobatteri. Esso è in grado di causare una serie di alterazioni nelle funzionalità riproduttive dell’ospite. In questo caso, quindi, impedisce agli insetti, portatori di virus, di riprodursi, ingrandire la popolazione e diffondere i vettori di malattie. Tuttavia, il lungo tempo necessario per ulteriori test induce a pensare che gli attuali approcci basati sugli insetticidi continueranno a svolgere un ruolo centrale per molti anni ancora.
Una recente scoperta utilizza Crispr/Cas9 per combattere Aedes aegypti
Per evitare l’uso continuo di insetticidi che come sappiamo ha un costo elevato non solo in termini economici, ma anche di salute ambientale, recentemente è stato proposto il sistema pgSIT. Questo meccanismo si basa sull’utilizzo delle Crispr/Cas9, che sappiamo bene essere un po’ una forma di “taglio e cucito”.
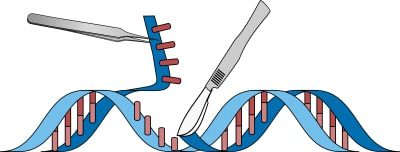
Infatti, esso si basa sull’impiego della proteina Cas9, una sorta di forbice molecolare in grado di tagliare un DNA bersaglio, generando modifiche al genoma di una cellula, sia questa animale, umana o vegetale. A seguito del taglio introdotto da Cas9, attraverso opportuni accorgimenti, è infatti possibile eliminare o sostituire delle specifiche sequenze. La programmazione del bersaglio di Cas9, inoltre, avviene attraverso una molecola di RNA, chiamata RNA guida.
Come agisce nello specifico il sistema pgSIT?
Il sistema pgSIT ha permesso di modificare il genoma di A. aegypti e di rendere i maschi della specie sterili e le femmine non in grado di volare e quindi a breve ciclo vitale. Dai risultati della ricerca, determinatasi nelle gabbie è venuto fuori che queste zanzare geneticamente modificate fossero in grado di sopprimere o sostituire totalmente la popolazione wilde-type. A quali fattori è dovuto ciò? Il fatto che le femmine geneticamente modificate non siano in grado di volare è un elemento estremamente importante. Esse, battendo le ali, sono in grado di emettere dei suoni che richiamano i maschi. In tal caso, quindi, questo meccanismo si annulla, riducendo la possibilità di accoppiamento. Inoltre, le femmine si rallentano nel muoversi e nel trovare fonti di sostentamento che gli consentano di sopravvivere.
I modelli matematici, infine, suggeriscono che il rilascio, su campo, di circa 100-200 o più uova di A. aegypti, caratterizzate dal sistema pgSIT, potrebbe determinare ottimi risultati come quelli ottenuti in laboratorio.
Fonti:
- Li, M., Yang, T., Bui, M. et al. Suppressing mosquito populations with precision guided sterile males. Nat Commun 12, 5374 (2021). https://doi.org/10.1038/s41467-021-25421-w
- https://www.fondazioneveronesi.it/magazine/articoli/lesperto-risponde/quali-infezioni-virali-possono-essere-trasmesse-dalle-zanzare
- https://www.unitn.it/ateneo/68544/cose-il-sistema-crisprcas9
Immagini:
- https://www.nea.gov.sg/corporate-functions/resources/research/wolbachia-aedes-mosquito-suppression-strategy/wolbachia-aedes-mosquito-suppression-strategy-how-it-works
- https://www.flickr.com/photos/iaea_imagebank/25819312343
- https://www.unitn.it/ateneo/68544/cose-il-sistema-crisprcas9