Da sempre, una delle maggiori problematiche in ambito clinico è sicuramente la reperibilità di organi e tessuti disponibili per il trapianto. La necessità di tali organi e tessuti supera infatti la loro disponibilità. Più di 100.000 pazienti si trovano nella lista d’attesa per un trapianto, e in media 22 persone muoiono ogni giorno in attesa che un organo o tessuto sia disponibile. Nell’ultimo decennio, l’ingegneria tissutale ha compiuto passi da gigante attraverso lo sviluppo di trapianti tissutali; tuttavia, ci sono ancora problemi significativi nell’applicazione clinica. Uno dei principali fattori che attualmente limitano l’applicazione clinica è la mancanza di una rete vascolare funzionante. La maggior parte delle attuali tecniche di bioingegneria non sono infatti ancora in grado di creare vasi di perfusione funzionanti. Inoltre, una corretta microvascolarizzazione non può essere realizzata utilizzando tecniche di biofabbricazione, come la stampa 3D. Di conseguenza, invece di tentare di progettare una rete vascolare, l’attenzione si è spostata verso diversi approcci grazie all’avvento di tecniche di decellularizzazione utilizzando, in questo caso, una foglia di spinacio.
Decellularizzazione
La decellularizzazione consiste nel denaturare le proteine del tessuto trattandolo con detergenti come l’SDS, il sodio dodecil solfato, e di eliminare tutte le cellule, preservando la matrice extracellulare e soprattutto una rete vascolare intatta. I tessuti e gli organi decellularizzati possono quindi essere ricellularizzati con cellule di un paziente per creare un innesto derivante dallo stesso individuo. Le analisi composizionali delle proteine, attraverso spettrometria di massa, hanno dimostrato differenze drastiche nella composizione di tessuti decellularizzati tra i diversi pazienti. I tessuti decellularizzati dei mammiferi non sono disponibili in grandi quantità e, anche quando disponibili, sono molto costosi. Inoltre, è necessaria una prolungata sperimentazione prima che interi organi decellularizzati possano essere considerati un’opzione nel campo medico. Perciò, bisogna cercare una risorsa di tessuti alternativa affinché il costo si abbassi. Le piante e gli animali sfruttano approcci abbastanza diversi per il trasporto di fluidi, sostanze chimiche e macromolecole, ma esistono sorprendenti similitudini tra i due tipi di strutture vascolari.
Materiali e metodi
Decellularizzazione delle piante
La vascolarizzazione delle piante segue la legge di Murray, e descrive il disegno di una rete ramificata ed affusolata simile a quella del sistema cardiovascolare umano. Le strutture all’interno del tessuto vegetale, come il tessuto umano, presentano proprietà meccaniche diverse che consentono varie funzioni. Le pareti cellulari delle piante sono composte da una varietà di polisaccaridi tra cui cellulosa, pectina ed emicellulosa. La cellulosa è biocompatibile ed ha dimostrato di promuovere la guarigione delle ferite. Inoltre, le impalcature di ingegneria dei tessuti cellulosici derivate da fette di mela decellularizzate hanno dimostrato la capacità di attaccamento e proliferazione delle cellule di mammifero e sono risultate biocompatibili se impiantate in vivo a livello sottocutaneo. Anche la pectina e l’emicellulosa sono state studiante come biomateriali per i tessuti ossei e per la guarigione delle ferite.
Analisi istologiche su foglie di spinacio
I campioni di foglie devono essere tagliati in quadratini di 1 cm, preferibilmente con il canale vascolare principale della foglia al centro del quadrato, mentre le radici ed i fusti saranno tagliati in pezzi di circa 1 cm di lunghezza. Successivamente, i campioni devono essere fissati, nel tempo di una notte, tramite un processore automatico di tessuto ATP-1 e poi incorporati in paraffina. I blocchi di paraffina vengono sezionati e colorati tramite tintura, per poi risciacquare tutto con acqua deionizzata per circa 5 minuti o fino a quando tutta la tintura risulta rimossa. Una volta deidratate le sezioni e immerse per 10s in un colorante definito “fast green FCF”, dovranno essere lavate in etanolo e poi nuovamente in xilene. Alla fine, i campioni possono essere visualizzati tramite microscopio.
Risultati
La struttura naturale delle piante superiori consente il trasporto di nutrienti attraverso xilema e floema a cellule distali. Per comprendere il potenziale di un’impalcatura tessutale vegetale, la decellularizzazione tramite perfusione è stata adattata per l’uso con foglie di spinacio. Queste foglie sono state utilizzate come modello grazie alla loro pronta disponibilità, al loro modello di rete vascolare e alla loro densità. Il giorno successivo all’inizio del processo di decellularizzazione, le foglie cominciano a perdere il loro colore verde a causa della perdita di clorofilla, che denota la perdita di cloroplasti dal tessuto fogliare (Fig.1).
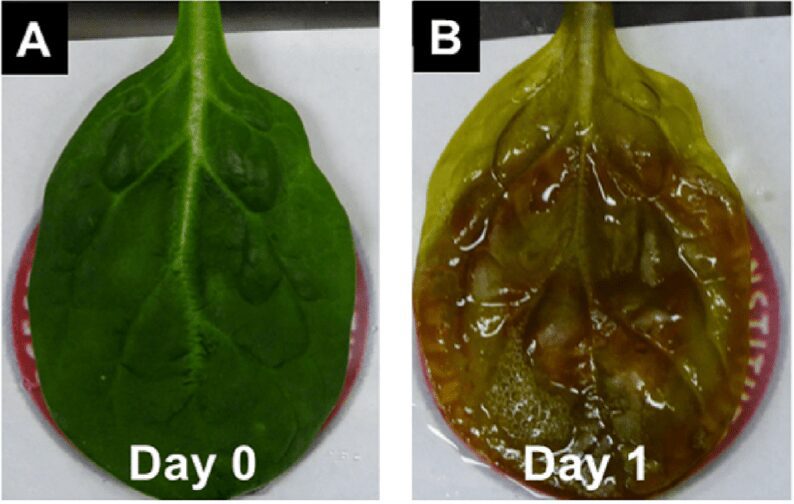
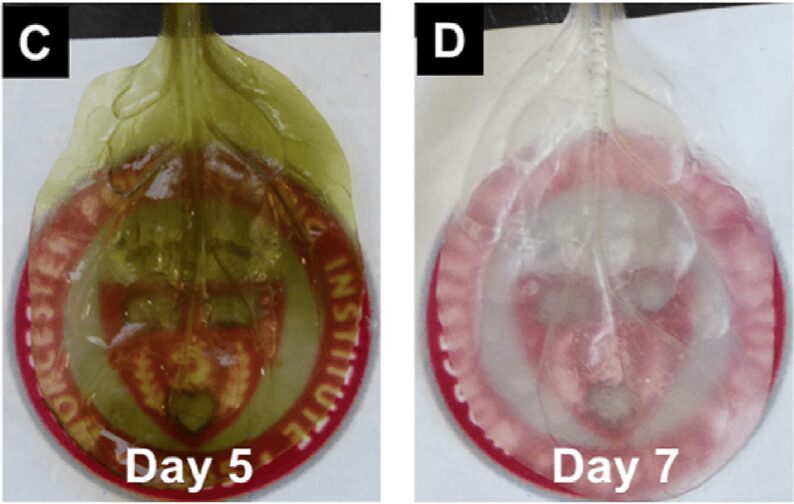
Il quinto giorno, le foglie diventano trasparenti con una tonalità di verde (Fig. 2 C). L’aggiunta di cloruro di sodio consente la rimozione di eventuali residui di clorofilla facendo risultare la foglia incolore e traslucida entro il settimo giorno (Fig. 2 D).
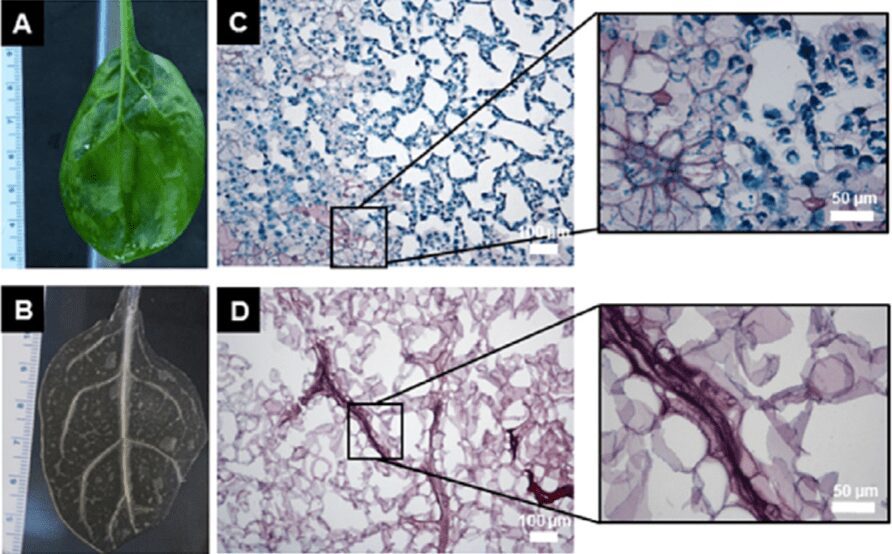
L’analisi istologica ci permette di identificare cellule con nuclei e cloroplasti in foglie native, nessuna delle quali è stata vista nelle loro controparti decellularizzate (Fig. 3). Invece, la lignina era presente sia prima che dopo il processo di decellularizzazione.
Caratterizzazione tramite SEM
Le foglie di spinaci decellularizzate hanno mantenuto lo stesso schema e la stessa densità delle reti vascolari osservate nelle foglie native (Fig. 4) riprese tramite miscroscopia elettronica a scansione (SEM), indicando che il processo di decellularizzazione non influisce sulle proprietà topografiche della superficie della foglia.

Le foglie decellularizzate contengono significativamente meno DNA e proteine rispetto alle foglie native. Questi dati dimostrano che il processo di decellularizzazione della pianta elimina quasi tutto il DNA e prodotti, classificando così il tessuto come decellularizzato. Rispetto alle foglie native, quelle decellularizzate presentano una apparente perdita di integrità meccanica. Nonostante ciò, rientrano nella gamma dei normali tessuti cardiaci umani decellularizzati utilizzabili. Oltre agli spinaci sono stati decellularizzati con successo anche i fusti di prezzemolo, suggerendo un potenziale diffuso per l’utilizzo di una varietà di specie vegetali.
Ulteriori test
Il grande vantaggio di usare cellule decellularizzate come base/impalcatura per i tessuti è il sistema vascolare innato. Perciò, i ricercatori hanno cercato di determinare se la vascolarizzazione della foglia rimanesse intatta e trasparente dopo il processo di decellularizzazione. Le foglie di spinacio decellularizzate sono state iniettate con il Ponceau Red attraverso una cannula e raggiungendo così tutto il sistema vascolare della foglia, con qualche piccola perdita. Affinché un tessuto vascolare ingegnerizzato sia accettato per processi clinici, il diametro di qualsiasi vaso deve permettere il passaggio del sangue. Per predire se questo sistema possa supportare il passaggio di cellule, la vascolarizzazione della foglia viene perfusa con un mezzo che possiede microsfere fluorescenti di diverso diametro. Questo metodo permette di compiere valutazioni sia per il diametro sia per l’apertura di un qualsiasi vaso.
Conclusioni
Esplorare l’ortogonalità dei vari regni offre un’opportunità unica di interfacciarsi con le differenze biologiche di ogni regno e imitare le caratteristiche peculiari. Questo approccio può essere sfruttato utilizzando paradigmi evoluti in un regno e offrire soluzioni a problemi di altri regni. Attualmente, è ancora poco noto come la vascolarizzazione vegetale sarà integrata con quella nativa umana o se ci sarà anche una risposta immunitaria.
Ad esempio, la cellulosa decellularizzata è biocompatibile e biodegradabile, ma non è chiara la risposta in vivo a questo tessuto vegetale. Quindi, saranno necessarie ulteriori indagini anche in questo senso.
L’utilizzo di piante per la formazione di tessuti ha molti benefici. La ricerca si sta muovendo verso una direzione più green e che ha a cuore l’ambiente, a causa dei cambiamenti climatici causati dall’uomo e l’esaurimento delle risorse naturali. Applicando i paradigmi di un regno ad un altro, potremmo finalmente riuscire ad affrontare la limitazione della perfusione esistente negli approcci tradizioni nel campo della medicina rigenerativa e della creazione dii tessuti. Tale ricerca fornisce risultati promettenti, ma, purtroppo, ci sono ancora molte domande senza risposta.
I commenti sono chiusi.