Caratteristiche virus epatite B
Il virus dell’epatite B (HBV) appartiene alla famiglia degli Hepadnaviridae. Sono virus a DNA dotati di envelope e prevalentemente epatotropi responsabili dell’insorgenza di patologie epatiche acute (epatite acuta, epatite fulminante), croniche (epatite cronica, cirrosi epatica) e neoplastica (epatocarcinoma primitivo). HBV è l’unico membro di questa famiglia che infetta l’uomo. Il virione maturo e completo ha un diametro di 42 nm e viene anche detto particella di Dane (fig.1). E’ costituito da un involucro esterno (envelope) di natura lipoproteica che racchiude un nucleocapside, di 30 nm, il quale a sua volta circonda il genoma virale rappresentato da un DNA circolare a doppia elica parzialmente incompleto. Oltre ad esso è presente la DNA polimerasi che per le sue proprietà funzionali è a tutti gli effetti una trascrittasi inversa (RT), con parziale omologia di sequenza con la RT dei retrovirus.

Oltre alla particella di Dane vengono prodotte altre particelle subvirali nelle cellule infettate con forma filamentosa di diametro intorno ai 40 nm e con forma sferica di 22 nm di diametro. Queste ultime non sono infettanti perché non possiedono il genoma ma solamente l’envelope con antigeni virali.
Genoma virus epatite B…
Il genoma del virus dell’epatite B come detto in precedenza è composto da una molecola di DNA di 3,2 kb (fig.2). E’ formata da due filamenti di diversa lunghezza il filamento breve S(+) che è circa il 50-80% della lunghezza di quello più esteso ed il filamento L(-). Il DNA possiede 4 open reading frame (ORF): la regione pre-S/S, la regione pre-C/C, la ORF P e la ORF X. La regione pre-S/S è composta da due sequenze dette pre-S1 e pre-S2 che precedono il gene S. Essendo presente un unico codone di stop comune e tre diversi codoni di inizio si vengono a formare durante la traduzione 3 diverse proteine dell’envelope. Queste proteine sono: la proteina large (L), la proteina middle (M) e la proteina small (S) detta anche antigene S o HBsAg.
Quindi l’involucro esterno del virus non è altro che un mosaico di queste 3 proteine. La proteina L è codificata dalle regioni pre-S1, pre-S2 e dal gene S ed è presente in forma glicosilata (gp42) e non glicosilata (p39). Svolge un ruolo importante sia nell’infezione che durante la formazione del virione poiché è implicata nel legame di HBV ai recettori cellulari e nell’assemblaggio delle proteine virali. La proteina M è codificata dalle regioni pre-S2 e dal gene S mentre la proteina S viene codificata dal gene S.
Tale proteina è denominata anche major perché è espressa sull’envelope in maggiore quantità rispetto alle altre. La regione pre-C/C codifica invece per due proteine, la proteina del core (HBcAg) e la proteina HBeAg. La prima è la costituente del capside icosaedrico del virus mentre la seconda non è un componente della particella virale ma è presente nel siero del soggetto infetto e quindi ha una funzione di marcatore di infettività. HBeAg prima di essere secreto subisce un ulteriore processo di maturazione, vengono idrolizzate la sequenza segnale e l’estremità C-terminale. La ORF P codifica per proteine non strutturali come la DNA polimerasi-RNA dipendente (RT) importante nella fase di replicazione del virus che produce un ibrido DNA-RNA legandosi covalentemente all’estremità 5’ del filamento di DNA (-). La regione X o ORF X codifica per la proteina HBX di 154 aa.
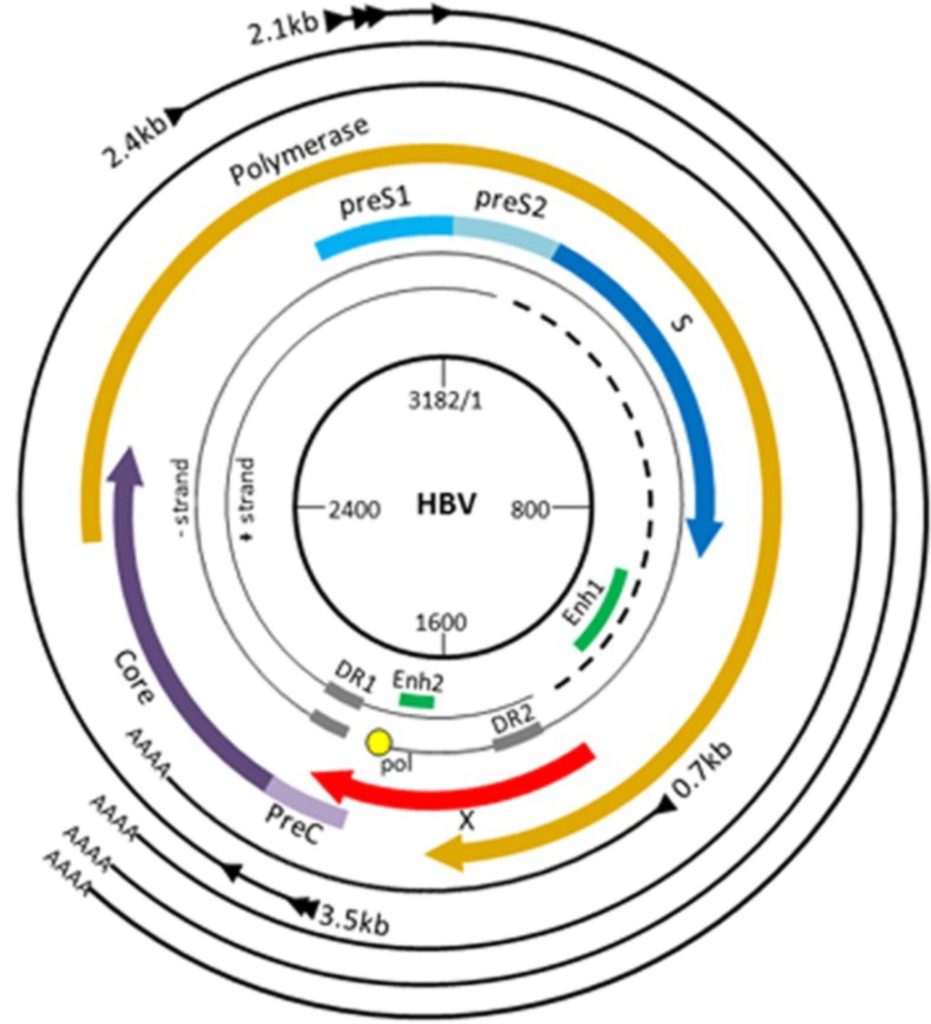
Sono presenti inoltre al terminale 5’ dei due filamenti due brevi sequenze ripetute denominate DR1 e DR2. Il ciclo di replicazione di HBV (fig.3) inizia con l’interazione delle proteine dell’envelope e i recettori specifici cellulari espressi sulla membrana degli epatociti. Al legame segue la fusione dell’envelope con la membrana cellulare ed una volta arrivato nel citoplasma viene direzionato al nucleo. Qui il genoma virale (dsDNA parzialmente incompleto) è convertito in DNA circolare a doppio filamento, si forma così una forma circolare covalentemente chiusa di DNA bicatenario (cccDNA) ad opera di enzimi cellulari.
A questo punto il cccDNA funge da stampo per la trascrizione di trascritti genomici e subgenomici, ad opera dell’enzima RNA polimerasi II della cellula ospite; questi vengono poi trasportati a livello citoplasmatico dove ha luogo la sintesi delle proteine funzionali e strutturali del virione.
Dai trascritti subgenomici come L mRNA, M/S mRNA, X mRNA vengono codificate le proteine dell’envelope e la proteina X, dall’mRNA preCore viene codificata la proteina pre-C alla quale dopo proteolisi dell’estremità C-terminale genera HBeAg. L’mRNA pregenomico invece codifica per la polimerasi virale e funge da stampo per la trascrittasi inversa. L’RNA pregenomico e la polimerasi vengono assemblate e incorporate con le proteine del core in modo da formare il nucleocapside.
In quest’ultimo, avviene la retrotrascrizione per cui si genera ad opera della RT un ibrido DNA-RNA che porta alla formazione del filamento L(-). Successivamente sullo stampo del filamento L(-) viene sintetizzato il filamento S(+) e ciò avviene solo dopo che l’mRNA pregenomico è stato degradato ad opera di una RNA H. Questo tipo di replicazione è asimmetrico poiché i due filamenti costituenti il DNA non sono generati contemporaneamente. Il nucleocapside, così costituito, viene internalizzato nel reticolo endoplasmico dove acquisisce le proteine dell’envelope, costituite dall’antigene di superficie virale e infine il virione maturo fuoriesce dalla cellula epatica.

Esistono diversi genotipi indicati con le lettere maiuscole e sono caratterizzati dall’avere lunghezze del genoma diverse perché presentano delezioni o inserzioni. Ad esempio, il genotipo B e C hanno una lunghezza di 3215 bp mentre il genotipo D 3182 bp, ciò è dovuto ad eventi di inserzione e delezione nel genoma.
Filogenesi
| Dominio | Acytota |
| Gruppo | VII (retrovirus a dsDNA) (HBV DNA) |
| Ordine | Non assegnato |
| Famiglia | Hepadnaviridae |
| Genere | Orthohepadnavirus |
| Specie | Hepatitis B Virus |
Patogenesi virus epatite B
L’infezione da HBV può dare luogo ad esiti diversi, strettamente correlati sia a fattori dell’ospite, quali l’età di acquisizione, il sesso e lo stato di immunocompetenza, sia alla biologia del virus e/o alla presenza di coinfezioni virali come HIV/HBV o altre cause di danno epatico (abuso di alcol). Tale infezione si associa ad epatite acuta, epatite cronica e carcinoma primitivo del fegato.
Il virus dell’epatite B (HBV) si trasmette per via parenterale, verticale e sessuale. Si è detto che il virus è epatotropo ma lo si ritrova anche a livello della saliva, nello sperma e nelle secrezioni vaginali. Il periodo di incubazione è variabile da 60 a 180 giorni. Nel 10% dei casi si sviluppa un’infezione acuta sintomatica mentre per il restante 90% l’infezione ha un decorso asintomatico. Raro è il decorso dell’infezione acuta ad epatite fulminante (1%), in questo caso si ha un’insufficienza epatica accompagnata ad encefalopatia. Nel caso di epatite acuta, la sintomatologia insorge con nausea, forti dolori addominali e muscolari, febbre ed un aumento delle transaminasi con incrementi da 3 a 5 volte i valori normali fino a 100 volte il range di normalità (il limite massimo di ALT a 25˚C è di 22 UI/L negli uomini e di 18 U/L nelle donne).
Dopo qualche giorno a causa della presenza di bilirubina nel siero, può comparire ittero (25-35% dei casi), con presenza di urine scure, feci chiare e colorazione giallastra di cute, mucose e congiuntive. La manifestazione dell’ittero è correlata con la presenza di un’elevata carica virale. L’infezione persistente da HBV si osserva in soggetti che, successivamente a un’infezione primaria non riescono a eliminare il virus. Ciò provoca il manifestarsi di un’epatite cronica che può evolvere in cirrosi epatica e carcinoma primitivo del fegato.
Metodi di identificazione
L’HBV non è direttamente citopatico ed il danno epatico deriva dalla reazione del sistema immunitario dell’ospite responsabile della necrosi delle cellule infette. Per l’inquadramento sierologico dell’infezione si ricercano i prodotti virali (gli antigeni, che riflettono la complessità strutturale del virus o il genoma) e gli anticorpi prodotti contro gli antigeni virali. Si distinguono: marcatori di infezione (HBsAg, anti-HBc, anti-HBe), di replica virale (HBV-DNA, HBeAg), di danno virus-indotto (IgM anti-HBc), di immunità (anti-HBs).
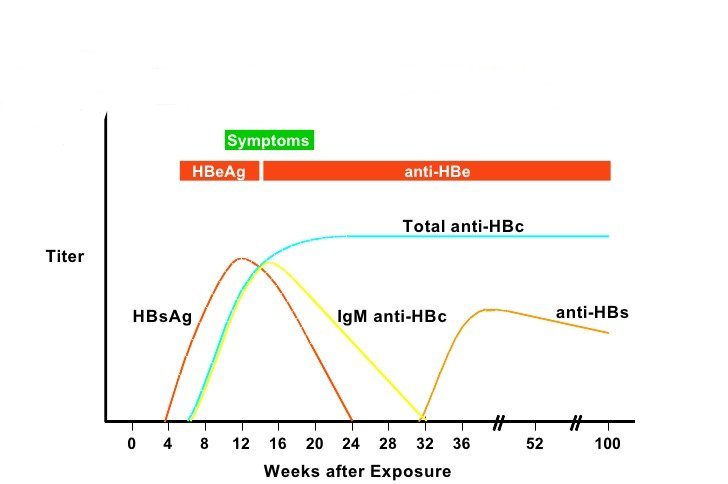
L’HBsAg resta il marcatore di infezione per eccellenza ed è determinabile da 1 a 10 settimane dall’infezione acuta e prima dell’insorgenza dei sintomi o dell’incremento delle transaminasi (fig.4). Nei pazienti che guariscono l’HBsAg diventa negativo dopo 4-6 mesi. La persistenza oltre 6 mesi indica la progressione della malattia nella forma cronica. L’anticorpo verso l’HBsAg (anti-HBs) appare in concomitanza con la scomparsa dell’HBsAg e frequentemente persiste, conferendo immunità duratura. L’HBeAg è un marcatore di replica virale e di infettività, associato ad alti titoli di HBV-DNA nel siero, malattia epatica attiva ed alto grado di infettività. Pazienti con infezione perinatale possono tuttavia essere HBeAg positivi ed avere basso grado di flogosi epatica e normali livelli di ALT. La sieroconversione da HBeAg ad anti-HBe e la negatività dell’HBV-DNA sierico indicano generalmente guarigione.
Terapia
Per quanto riguarda il trattamento dell’epatite cronica sono stati sviluppati negli anni farmaci in grado di ridurre o inibire la replicazione virale e monitorare il processo infiammatorio a livello epatico. Tra questi vi è la lamivudina, un farmaco appartenente alla classe degli analoghi nucleosidici della trascrittasi inversa. Questa molecola una volta fosforilata va a competere per l’incorporazione nelle sequenze di DNA virale andando così a bloccare il processo di sintesi del genoma virale ad opera della RT.
Vengono impiegati anche analoghi nucleotidici (Adefovir) che hanno la stessa funzione inibitrice della lamivudina. L’esistenza di un vaccino ha determinato una significativa diminuzione dell’incidenza dei casi di Epatite B, la via di somministrazione è intramuscolare e consiste di 3 dosi: la prima al III mese di età, la seconda al V mese e l’ultima all’XI mese. E’ un vaccino ricombinante ovvero costituito dalla proteina S (la proteina contro cui è diretta maggiormente la risposta anticorpale) clonata nel genoma di Saccharomyces cerevisiae e così fatta esprimere su larga scala in vitro.
Fonti
- T. Jake Liang, 2009, Hepatitis B: virus and disease.
- M.J. Bouchard e R. J. Schneider, 2004, The enigmatic X gene of Hepatitis B Virus.
- C. Wu, Y. Chen, L. Cao et all., 2018, Hepatitis B Virus infection: defective surface antigen expression and pathogenesis.
- J. Hoofnagle, 1994, Terapy of acute and chronic Hepatitis B.
I commenti sono chiusi.