Caratteristiche
Il virus Epstein Barr (EBV) anche detto Human Herpes Virus 4 (HHV-4) è un virus a DNA appartenente alla famiglia degli Herpes virus, responsabile della mononucleosi infettiva, a noi tutti nota con il nome di malattia del bacio.
L’EBV prende il nome dai suoi scopritori, il professor Michael Antony Epstein e la dottoressa Yvonne Barr. La scoperta accidentale dell’EBV e della sua associazione con la mononucleosi infettiva avvenne mentre i ricercatori analizzavano, al microscopio elettronico, una linea cellulare ottenuta da pazienti affetti da una particolare forma di linfoma delle zone malariche sub-sahariane, il così detto linfoma di Burkitt.
Nonostante i primi studi correlarono la presenza di questo virus al linfoma di Burkitt africano, in realtà il virus venne successivamente identificato nella paggior parte degli individui adulti sani e il suo ruolo nella patogenesi di questo tipo di linfoma divenne quindi sospetta. Ulteriori studi, associarono l’EBV con la patogenesi di una versione africana del linfoma di Burkitt nelle popolazioni endemiche della malaria e con la mononucleosi infettiva nel resto della popolazione. L’EBV è stato associato anche ad altri tipi d tumori maligni, come ad esempio il linfoma di Hodgking ed altri linfomi epiteliali, oltre che alla promozione della sclerosi multipla.
Un recente studio sierologico, ha infatti individuato un’interazione virale additiva della risposta immunitaria contro la glicoproteina virale IE1A ed EPV e l’insorgenza della sclerosi multipla, il cui potenziale ruolo promotore in questa patologia degenerativa era già noto dalla comunità scientifica.
Data la quasi esclusività dell’uomo come ospite principale del virus, dunque la difficoltà della sperimentazione animale per trattamenti antivirali, non esiste ancora nessun vaccino contro l’EBV.
Filogenesi
| Dominio | Acytota |
| Gruppo | Gruppo I (virus a dDNA) |
| Famiglia | Herpesviridae |
| Sottofamiglia | Gammaherpesvirinae |
| Genere | Lymphocryptovirus |
| Specie | Human herpesvirus 4 (HHV-4) |
Morfologia strutturale
L’EBV ha una forma sferoidiale ed un diametro complessivo di circa 122-180 nm. E’ costituito da una doppia membrana lipoproteica chiamata pericaspide esterno, che avvolge un nucleocapside icosaedrico interno dal diametro di circa 100 nm. Il genoma di EBV è costituito da un doppio filamento di DNA di 172 bp e 85 geni dei quali si differenziano 150 esoni e 12 introni. Le proteine codificate dal virus durante il suo periodo di latenza sono al massimo 9.
Patogenesi
L’EBV si trasmette attraverso lo scambio di fluidi, prevalentemente saliva, motivo per il quale l’infezione da esso causata è stata ribattezzata malattia del bacio. Il primo e principale target dell’EPV sono le tonsille, organoidi linfoidi, sede dei linfociti T e B. A livello delle tonsille, l’EBV attacca le cellule B e le cellule epiteliali. A questo livello, parliamo di infezione primaria, generalmente asintomatica. Dopo il primo attacco alle cellule B, il virus ha un periodo di incubazione di 2-6 settimane.
Il virus si replica quindi nelle cellule B e nelle cellule epiteliali, che possono essere trasmesse, attraverso la saliva, ad altre persone. Il riconoscimento di EBV parte delle cellule epiteliali avviene tramite un antigene virale, la glicoproteina gp350. A questo riconoscimento ne segue la fusione dell’envelope virale con la membrana cellulare dei linfociti B grazie all’interazione della gliproteina virale gp42 con le molecole MHC classe II.
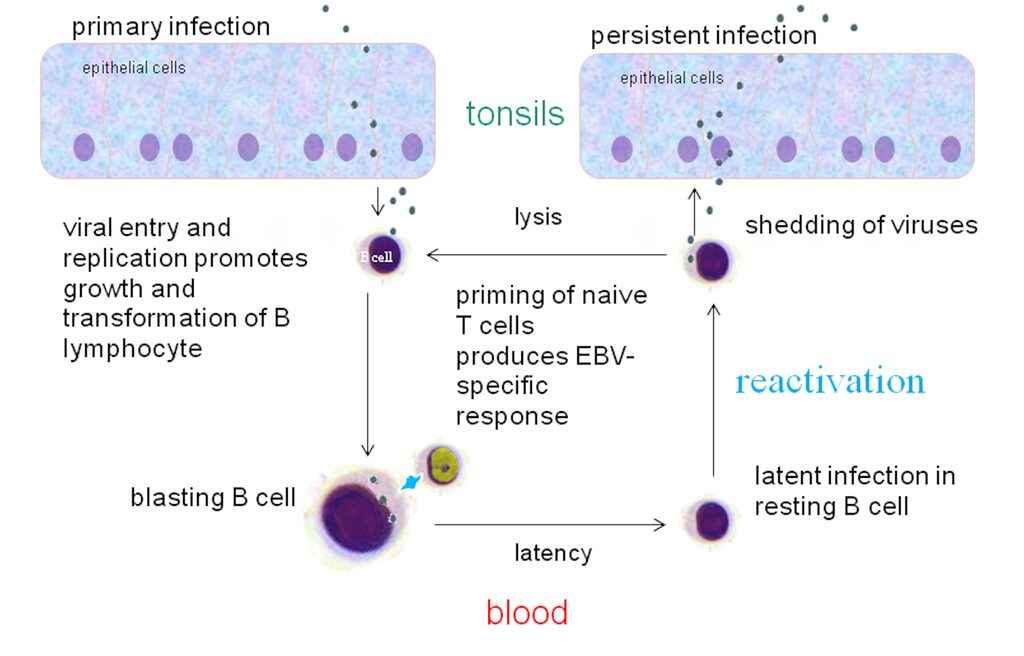
Una volta entrato nelle cellule B, l’EBV può entrare in tre fasi progressive di latenza. Dopo l’infezione primaria, il virus va incontro alla fase di latenza III, durante la quale si assiste alla risposta immunitaria delle cellule B infettate, con stimolazione delle cellule T di tipo CD8+ o linfociti citotossici. Durante questo processo di reazione del sistema immunitario, le cellule B si attivano e producono degli anticorpi contro EBV. L’entrata del virus in circolazione determina le forme più aggressive della mononucleosi infettiva, associate a stati febbrili e malessere generale. Durante la fase di latenza II dell’EBV, le cellule B differenziano in cellule B della memoria.
La riattivazione del virus avviene quando il virus passa dalla sua fase di latenza alla replicazione litica, che determina nuovamente la diffusione e replicazione del virus nelle cellule epiteliali.
Metodi di identificazione
Spesso l’infezione da EBV avviene durante l’infanzia e non causa alcun sintomo. La comparsa di sintomi aspecifici come la febbre, malessere generale, cefalea insieme a sintomi specifici quali infiammazione delle tonsille, dei gangli linfatici del collo, infiammazione del fegato ed eruzioni cutanee consentono di diagnosticare una probabile mononucleosi infettiva.
Il monotest è un test rapido per la mononucleosi che permette di identificare, con un’accuratezza del 71-90% , la presenza di anticorpi eterofili di EBV in un campione di sangue prelevato dal paziente.
Un ulteriore test, ancora più accurato, è in grado di identificare la presenza di anticorpi diretti contro EBV.
Terapia
Come per tutte le malattie infettive, la prevenzione consiste nella propria igiene personale e degli spazi con cui il virus potrebbe essere venuto a contatto. E’ inoltre importante evitare di condividere cibo, bevande, stoviglie e utensili con persone infette, anche nei giorni successivi alla manifestazione clinica dell’infezione.
Ad oggi non esiste un trattamento contro l’EBV, ed anche i comuni antivirali non sembra facciano effetto. Tuttavia, è comunque possibile curare la sintomatologia correlata alla sua infezione con riposo, farmaci analgesisci o antipiretici. In caso di rare complicanze e difficoltà respiratorie viene raccomandato anche l’uso di corticosteroidi.
Un team di ricercatori americani è inoltre impegnato nello sviluppo di un vaccino efficace contro l’EBV. I loro ultimi sforzi si sono concentrati sullo sviluppo di forme anticorpali in grado di attaccare gli antigeni virali che consento all’EBV di attaccare da un lato le cellule B del sistema immunitario e dall’altro, le cellule epiteliali quindi rispettivamente le glicoproteine gp42 e gp350 (Figura 2 e Figura 3).


I primi risultati ottenuti in modelli animali di scimmie hanno dato dei risultati positivi, ma ulteriori studi condotti nell’uomo sono necessari per confermare la loro efficacia.
Serena Galiè