Non esiste ancora una terapia in grado di eliminare completamente il virus dell’HIV dall’organismo di una persona sieropositiva. I farmaci antiretrovirali, pur controllando l’infezione, non funzionano sul DNA provirale, cioè sulle copie che si sono integrate nel genoma delle cellule infette. Il virus può rimanere latente in questo stato anche per anni, nascosto ai farmaci e alle cellule del sistema immunitario, e riattivarsi dopo la cessazione della terapia antiretrovirale – che il paziente è quindi costretto ad assumere per tutta la vita. Ma le cose potrebbero cambiare, grazie alle nuove terapie basate sull’editing del genoma che mirano proprio a eradicare questi bacini infettivi.
La “Food and Drug Administration” (FDA) ha autorizzato lo studio clinico di fase I/II per la terapia sperimentale EBT-101, progettata dalla biotech statunitense Excision BioTherapeutics in collaborazione con l’Università Statale di Milano. Il farmaco è basato sulla tecnologia dell’editing genomico CRISPR-Cas-9 per stanare il virus nascosto e asportare porzioni significative del genoma virale dalle cellule infette. L’inizio dello studio clinico è previsto entro la fine di quest’anno e permetterà di valutare la tollerabilità, sicurezza ed efficacia della terapia.
HIV, il virus nascosto
Il virus dell’immunodeficienza umana (human immunodeficiency virus, HIV) (Fig.1) è la causa della maggior parte delle infezioni al mondo. Secondo una stima di UNAIDS, nel 2020 le persone infettate dal virus erano 37,7 milioni, di cui la maggior parte in Africa e America Latina. In Italia il numero dei nuovi casi aumenta di circa 4000 ogni anno.

[Fonte: Wikipedia]
L’HIV infetta un tipo di globuli bianchi chiamati linfociti T CD4 o anche linfociti T helper. Questi hanno un ruolo centrale nella difesa dalle infezioni o dal cancro poiché “aiutano” e coordinano la risposta delle altre cellule immunitarie, come i linfociti B (produttori degli anticorpi) e i linfociti T CD8 (i “killer” delle cellule infette o cancerose). Conseguenza dell’infezione da HIV, quindi, è un progressivo indebolimento del sistema immunitario e negli stadi più avanzati lo sviluppo dell’AIDS (Sindrome da immunodeficienza acquisita) che rende la persona infettata dal virus suscettibile ad altre malattie o infezioni opportunistiche.
CRISPR contro l’HIV
Fino a qualche decennio fa, la diagnosi di sieropositività era una condanna a morte. Oggi, invece, una persona infettata dal virus può condurre una vita relativamente normale e non sviluppare mai l’AIDS. I farmaci antiretrovirali sono progettati per combattere i virus a RNA come l’HIV e ne bloccano la replicazione. Spesso funzionano così bene che la carica virale nell’organismo può scendere sotto un livello soglia e diventare addirittura “non rilevabile”. In questo caso anche le probabilità di contagiare un’altra persona sono quasi nulle.
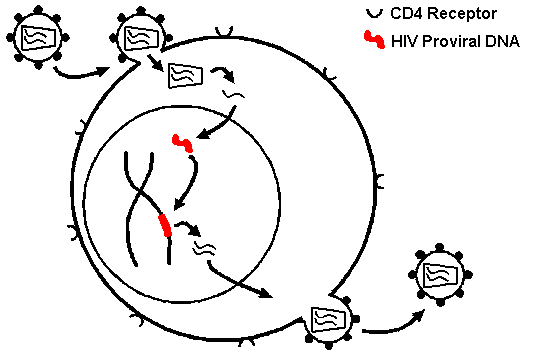
Questi farmaci consentono di tenere a bada l’infezione “attiva”, ma non quella “latente”. Diverse copie del genoma virale si integrano nel DNA delle cellule infette sottoforma di “provirus” (Fig.2) e sono inattaccabili dai farmaci e dal sistema immunitario. Il paziente è costretto ad assumere gli antiretrovirali per tutta la vita, perché qualora smettesse di prenderli, il DNA provirale potrebbe tornare attivo e riprendere l’infezione. L’obiettivo delle nuove terapie contro l’HIV è eliminare anche le copie integrate, senza distruggere le cellule infette o scatenare tempeste infiammatorie che danneggerebbero l’organismo. Il bisturi molecolare CRISPR-Cas-9 è lo strumento ideale, poiché consente di ritagliare sequenze specifiche di DNA, con una precisione di singolo nucleotide.
Il primo studio clinico
Il sistema funziona grazie a due RNA guida, che si legano a tre siti specifici sul genoma di HIV, e a un enzima, Cas9, che esegue un taglio di precisione “asportando porzioni significative del genoma di HIV e riducendo il rischio di una ‘escape’ virale”, come si legge nel comunicato stampa rilasciato dall’azienda biotech. EBT-101, questo il nome della terapia, ha ricevuto l’autorizzazione dall’FDA per lo studio clinico di fase I/II, dopo aver prodotto risultati soddisfacenti nella fase preclinica. Il farmaco sarebbe stato in grado di eradicare completamente l’infezione da HIV in molteplici modelli, da cellule primarie umane agli animali più semplici, fino ai primati non umani.
EBT-101 viene somministrato come trattamento singolo e utilizza un virus adeno-associato come “vettore”. In altre parola, enzima e RNA guida vengono “impacchettati” dentro un virus deprivato dei geni essenziali per la replicazione, che diventa un semplice veicolo di trasmissione. Non può infatti riprodursi nell’organismo (è reso innocuo) ma è ancora capace di trasferire il suo materiale genetico all’interno della cellula.
Le altre terapie avanzate
EBT-101 fa da apripista nel suo genere, ma sono già diversi anni che la ricerca contro questo virus si è spostata sulle terapie avanzate. Nel 2019, ad esempio, sono usciti due studi che hanno segnato una tappa fondamentale nella lotta all’HIV. Il primo è il caso di un paziente che ha ottenuto il trapianto di cellule staminali ematopoietiche manipolate con CRISPR per bloccare l’ingresso del virus. Il secondo descrive una tecnica chiamata LASER ART, basata sulla la combinazione di terapia antiretrovirale a rilascio prolungato e Crispr-Cas9, efficace negli studi preclinici per eliminare il virus dalle cellule in modelli murini.
Un’altra area di ricerca mira a utilizzare gli esosomi per trasportare farmaci innovativi nelle cellule infettate dall’HIV e per silenziare l’espressione dei geni del virus. Si tratta di vescicole sufficientemente piccole da muoversi liberamente nell’organismo, che le usa come “messaggeri” extracellulari, in grado di raggiungere cellule molto distanti tra loro. Diversi studi hanno messo in luce il potenziale degli esosomi per curare l’infezione da HIV. Di recente, gli esosomi hanno permesso di trasportare nelle cellule dei topi infetti una proteina in grado di impedire la replicazione del genoma virale.
Infine, tra le terapie avanzate in fase di sperimentazione contro l’HIV ci sono anche i CAR-T, che hanno già dimostrato la loro efficacia contro diversi tumori. Si tratta di linfociti T manipolati geneticamente per esprimere sulla superficie due recettori, che gli permettono di riconoscere rapidamente le cellule infette e di aumentare le loro funzioni immunitarie. L’uso di questa terapia, in combinazione con gli antiretrovirali, ha ridotto nei topi la percentuale di virus latente, il bacino dell’infezione.
Come cambierà la lotta all’HIV?
I progressi nella ricerca contro l’infezione da HIV hanno già trasformato questa malattia in una condizione cronica, poiché hanno permesso di tenere a bada il virus a tempo indefinito. Ma l’ingresso delle terapie avanzate potrebbe riuscire laddove tutti gli altri farmaci hanno fallito: eradicare completamente il virus, come mai è stato fatto in precedenza. La rivoluzione potrebbe richiedere ancora molti anni, poiché la maggior parte delle terapie sono ancora in fase di sperimentazione. Il primo studio clinico, che inizierà entro la fine di quest’anno, potrebbe aprire le porte a una nuova generazione di farmaci innovativi contro l’infezione da HIV.
Fonti:
Prasanta K. Dash, et al., 2019. Sequential LASER ART and CRISPR Treatments Eliminate HIV-1 in a Subset of Infected Humanized Mice. Nature.