È recentissima la notizia riguardante la scoperta del nuovo ceppo del virus dell’immunodeficienza umana (HIV). Lo staff dei laboratori di ricerca dell’azienda farmaceutica Abbott, in collaborazione con l’Università del Missouri, si è concentrato sul sequenziamento genico di campioni raccolti in Congo tra il 1983 ed il 2000: analizzando le sequenze genomiche dell’HIV-1 con la metodica NGS si è potuto confermare che, quello individuato, è classificabile come un nuovo ceppo virale appartenente al gruppo M (Figura 1).
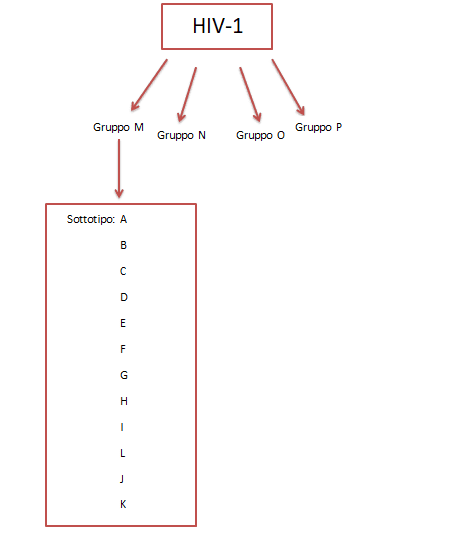
Figura 1 – Variabilità genetica del virus dell’HIV. Il virus HIV si distingue in HIV-1 e HIV-2, che sono i due gruppi principali. HIV-1 è ulteriormente suddiviso in gruppi, di cui il gruppo M è quello più diffuso tra gli esseri umani. Il gruppo M è a sua volta distinto in sottotipi virali a seconda della geolocalizzazione e di alcune caratteristiche genetiche.
HIV-1
Considerato la causa principale della pandemia di AIDS (sindrome da immunodeficienza acquista), dal momento che rappresenta la forma predominante del virus tra gli esseri umani, HIV-1 (Figura 2) sembra essersi originato in Africa centrale per poi diffondersi in tutto il mondo: è caratterizzato da variabilità genetica e da un’elevata virulenza e patogenicità, con le dovute differenze tra i diversi sottotipi e varianti ricombinanti, ovvero quelle forme virali originatesi da due sottotipi differenti dello stesso virus durante una co-infezione nel medesimo soggetto.
HIV-1, in base ad un’analisi filogenetica, è suddiviso in 4 distinti gruppi: M (Major), O (Outlier, eccezione), N (Non-M e Non-O) e P (Pending, in attesa di riformulazione). Il gruppo M è quello predominante nelle infezioni su scala globale e presenta, a sua volta, una notevole divergenza genetica, inizialmente individuata da ricerche sulle sequenze del solo gene env, ritenuto estremamente importante da studiare dal momento che codifica per la proteina gp120 che permette l’aggancio del virus ai linfociti T dando così origine all’infezione.

Figura 2 – Morfologia dell’HIV-1. Il virus è di forma sferica e circondato da doppia membrana: un pericapside o envelope ed un capside, sulla quale sono poggiate numerose proteine strutturali e di adesione. Nel core o nucleocapside conico della particella virale oltre al materiale genetico, due singoli filamenti di RNA associati a proteine basiche, sono presenti anche enzimi, tra i più importanti la trascrittasi inversa.
La tendenza a mutare
Si distinguono dunque almeno dieci cladi o sottotipi appartenenti al gruppo M, indicati con le lettere dell’alfabeto dalla A alla L, J e K. Alla base di questa variabilità genetica del virus vi è una bassa accuratezza della trascrittasi inversa, ovvero un’alta frequenza di errore da parte di questo enzima nell’aggiunta di nucleotidi per la sintesi di una nuova catena di DNA, causata a sua volta da un’elevata velocità di replicazione del virus stesso. Ad ogni ciclo replicativo si conta un numero enorme di mutazioni puntiformi, inserzioni e delezioni, molto spesso vantaggiose per il virus, poiché culminano nella genesi di nuove varianti virali.
La capacità di mutare frequentemente rappresenta l’arma più potente dell’HIV; difatti ciò permette al virus di nascondersi a lungo all’interno delle cellule infette, riuscendo così ad avviare numerosi cicli replicativi. Il fatto che il virus eluda facilmente le difese immunitarie dell’ospite rende difficili tutti gli interventi profilattici e terapeutici, nonché lo studio di possibili vaccini anti-virali.
HIV-2
Al pari del sierotipo HIV-1, il virus dell’HIV-2 è caratterizzato da una considerevole variabilità genetica e comprende 8 sottotipi, identificati ancora una volta con le lettere dell’alfabeto: dalla A alla H. Tuttavia gli studi su HIV-2 sono numericamente inferiori rispetto a quelli sul sierotipo HIV-1, poiché il virus in questione è considerato meno “pericoloso” dal momento che possiede una più bassa virulenza. Ciò implica che questa forma del virus determina un quadro clinico completamente differente: il periodo di latenza, ad esempio, è più esteso e la possibilità di contagiare un altro soggetto è inferiore.
Data la scarsa infettività, inoltre, il virus sembra rimanere confinato geograficamente in Africa Occidentale. Nonostante ciò i sottotipi A e B sono stati catalogati come ceppi a carattere pandemico ed individuati anche in Asia e Stati Uniti d’America, ovvero in quei Paesi in cui è stato possibile registrare un più alto tasso di immigrazione di soggetti provenienti dalle zone interessate dall’infezione da HIV-2.
La nuova variante virale
I sottotipi virali, detti anche ceppi o stipiti, altro non rappresentano che un’evoluzione, in senso stretto, del virus, che fa da minimo comune multiplo a tutti i sottotipi noti. Le varianti virali di una stessa specie dunque condividono alcune caratteristiche morfologiche, biologiche e filogenetiche ma possono distinguersi in base alla distribuzione geografica, alla modalità di insorgenza e di diffusione, alla patogenicità e al quadro sintomatologico correlato all’infezione che il virus determina.
Dell’HIV-1 gruppo M sottotipo L si è iniziato a parlare per la prima volta nel 1983, in Congo: dalle analisi preliminari si era notata una certa differenza tra quell’isolato e tutti gli altri stipiti già classificati. Lo stesso è stato segnalato di nuovo nel 1990, ancora una volta nella Repubblica Democratica del Congo. Nel 2001 infine, sempre in Congo, nel corso di uno studio sulla prevenzione della trasmissione verticale da madre a figlio dell’infezione da HIV, è stato prelevato materiale infetto difficile da analizzare perché insufficiente.
Tuttavia i ricercatori erano convinti dell’esistenza di una certa somiglianza genetica con i campioni precedentemente prelevati nello stesso Stato. Solo dopo 19 anni si sono sviluppate le tecnologie adeguate per sequenziare l’intero genoma di quel virus, rimasto congelato dal 2001, confermando l’esistenza di nuovo ceppo.
Nonostante il sottotipo virale sia in circolazione da molto tempo, per ora i casi sono limitati geograficamente e numericamente parlando. Questo lascia sottintendere che non si tratta di una variante caratterizzata da un elevato grado di infettività e virulenza e che quindi non esiste alcun pericolo di pandemia. Inoltre sembra che gli attuali trattamenti preventivi e farmacologici a disposizione per contenere l’infezione da HIV possono essere utili anche in questo caso, ma il tutto dovrà essere approfondito da ricerche future.
Un’attesa lunga 19 anni
Lo studio è stato pubblicato sul Journal of Acquired Immune Deficiency Syndromes ed è parte del programma di sorveglianza della Abbott, attivo da 25 anni, che si occupa specificamente dell’aggiornamento dei rilevamenti delle malattie infettive, per tenere traccia dei cambiamenti dei virus, in particolar modo dell’HIV e dell’epatite, in modo tale da continuare a garantire test diagnostici adeguati per lo screening del sangue.
Nel caso specifico dell’HIV molte ricerche nel corso degli anni sono state indirizzate sull’analisi dell’intero genoma virale, al fine di identificare tutte le varianti isolate. Si era notato, difatti, che l’elevato tasso di mortalità correlato a questo tipo di infezione era connesso al sierotipo HIV-1 e non a HIV-2, meno frequente e difficilmente a carattere pandemico e che, nonostante ciò, continuava ad emergere una notevole divergenza genetica tra gli isolati: la variabilità della popolazione virale HIV-1 genera ceppi connessi tra loro ma distinti, ognuno con proprie caratteristiche, in grado di rispondere in maniera differente alle terapie anti-virali che mirano ad impedire la replicazione del virus nell’organismo.
Dunque era, ed è tuttora, importante classificare in maniera corretta ogni sottotipo virale in modo tale da riuscire a limitare i danni, gestendo in maniera appropriata i diversi tipi di infezione: questo è possibile soltanto studiando il genoma completo di ogni nuovo ceppo e confrontando l’un l’altro.
Grazie alle nuove tecnologie si è smesso dunque di classificare i ceppi virali sulla base di sequenze genetiche parziali, in particolar modo erano ben conosciuti i geni strutturali gag ed env (Figura 3), e si sono così potute formulare, nel 1999, linee guida internazionali per la nomenclatura, che hanno portato ad una completa revisione della tassonomia di HIV.
Secondo le nuove direttive, inoltre, per confermare l’esistenza di un nuovo ceppo, è necessario indicare, analizzare ed accertare almeno tre distinti eventi non correlati epidemiologicamente tra loro. È per questo che ad oggi è corretto parlare del nuovo sottotipo L appartenente al gruppo M.

Figura 3 – Schematizzazione del genoma di HIV-1. Gag, pol ed env sono geni strutturali comuni alla famiglia Retroviridae che codificano per le proteine del nucleocapside. Le sequenze regolatorie tat e rev sono invece essenziali per la trascrizione e la replicazione. L’ultima classe di geni è rappresentata da sequenze accessorie: nef, vif, vpr, vpu, che ricoprono un importante ruolo nella replicazione virale in vitro e definiscono patogenicità e infettività del virus.
Il significato della ricerca
NGS, acronimo di Next Generation Sequencing è un sequenziamento di nuova generazione che facilita il confronto, simultaneamente, di diversi geni. Una tecnologia innovativa, dunque, che permette di caratterizzare la sequenza completa di grandi genomi in poco tempo, partendo da un’analisi in parallelo di milioni di frammenti di acido nucleico.
I nuovi strumenti tecnologici sono stati essenziali in questo studio specifico; difatti dato che il materiale virale estratto dal campione era scarso, è stato proprio necessario scegliere una metodica che permettesse anche l’amplificazione delle catene nucleotidiche.
I progressi tecnologici hanno dunque confermato che di sottotipi virali del gruppo M ne esistono almeno una decina: HIV è un virus che muta in continuazione e per questo sarebbe bene che la comunità scientifica riuscisse a monitorare l’evoluzione della sua variabilità genetica in modo tale da non trovarsi impreparata per una nuova eventuale pandemia.
Carla Caianiello
Fonti:
- Yamaguchi J., McArthur C., Vallari A., Sthreshley La., Cloherty Gavin A., Berg Michael G., Rodgers Mary A. (2019). Complete genome sequence of CG-0018a-01 establishes HIV-1 subtype L. Journal of Acquired Immune Deficiency Syndromes. Doi: 10.1097/QAI.0000000000002246
- Caramma I. ANDAMENTO DELLA PREVALENZA IN ITALIA DEI CEPPI NON-B DI HIV-1 NEGLI ULTIMI TRENTA ANNi. Tesi di dottorato di ricerca in Malattie Infettive XXIII ciclo. Università degli Studi di Milano. Facoltà di Medicina e Chirurgia, a.a 2009/2010 https://air.unimi.it/retrieve/handle/2434/150137/131490/phd_unimi_R07898.pdf
- https://edition.cnn.com/2019/11/06/health/hiv-new-strain-discovered/index.html
- https://nypost.com/2019/03/04/second-person-in-history-reportedly-cured-of-hiv/
- https://www.ilpost.it/2019/11/07/nuovo-ceppo-virus-hiv-aids/
- https://www.inail.it/cs/internet/comunicazione/pubblicazioni/catalogo-generale/la_biosicurezza_connessa_utilizzo_di_vettori_lentivirali.html
- https://it.wikipedia.org/wiki/HIV
- https://www.nbcnews.com/health/health-news/what-know-about-new-hiv-strain-n1078291
- https://www.quotidianosanita.it/scienza-e-farmaci/articolo.php?articolo_id=78547https://www.scientificamerican.com/article/first-new-hiv-strain-in-19-years-identified
Buongiorno, quindi una Persona che già ha HIV potrebbe essere a rischio di contrarre nuovi ceppi? O facendo una terapia con carica virale non rilevabile è immune a ricontrarre l’ HIV? Grazie