Caratteristiche
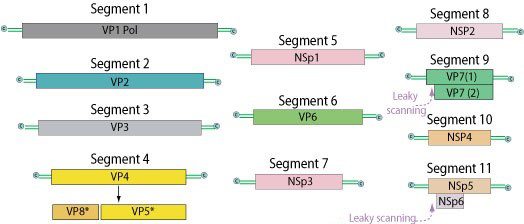
I Rotavirus, sono uno dei 15 generi appartenenti alla famiglia dei Reoviridae. Sono virus con un diametro di circa 70 nm, non possiedono l’envelope ma ben tre strutture capsidiche che circondano il genoma costituito da 11 segmenti di RNA bicatenario (dsRNA). Ciascun segmento codifica per una proteina (eccetto il frammento 11 che ne codifica due), in particolar modo vengono codificate 6 proteine strutturali e 6 di tipo funzionale (Fig.1).
Questi segmenti di RNA formano quattro gruppi diversi per dimensione sulla base dell’ordine dei pattern di migrazione elettroforetica. I pattern elettroforetici sono chiamati elettroferotipi e vengono riconosciuti quattro segmenti di dimensioni grandi, due di dimensioni medie, tre di piccole dimensioni e due con dimensioni ancor più piccole. Il segmento che migra più lentamente è noto come 1, mentre quello più rapido è definito 11 (fig.2).

Le proteine strutturali VP4 e VP7 costituiscono lo strato capsidico più esterno, la proteina VP6 oltre a comporre lo strato intermedio definisce anche la specificità di gruppo e sottogruppo dei rotavirus, mentre lo strato più interno è formato principalmente dalla proteina VP2 ed è associato a complessi proteici funzionali composti da VP1 e VP3. La VP1 è una RNA polimerasi-RNA dipendente ed è implicata nella sintesi del dsRNA mentre, la VP3 è una guanililtransferasi. Le proteine VP4 e VP7 fungono da antirecettori virali e mediano la fase di penetrazione del virus nella cellula ospite (fig.3). Il taglio della proteina VP4 nei due prodotti VP5 e VP8, rende maggiore l’infettività dei rotavirus, cioè facilita la penetrazione del virus nella cellula ospite.

Come detto in precedenza, in base alla variabilità genetica e specificità antigenica della proteina VP6, i rotavirus vengono classificati in 8 gruppi o specie indicati con le lettere maiuscole da A ad H. Il Rotavirus A è la specie che più frequentemente causa infezioni nell’uomo. VP6 determina anche la specificità di sottogruppo (SG). I rotavirus di gruppo A sono classificati pertanto nei 4 sottogruppi: SGI, SG II, SGI+II e SG non-I non-II in base alla reattività con anticorpi monoclonali SG-specifici. I rotavirus riconoscono diversi recettori cellulari tra cui l’acido sialico e le integrine. Ad esempio, VP5 lega tramite i residui Asp 308, Gly 309 e Glu 310 l’integrina α2β1.
Una volta avvenuto il legame al recettore e la penetrazione mediante endocitosi del virus, a livello del citoplasma inizia il processo di trascrizione che porta alla sintesi degli mRNA. Questi vengono tradotti nelle proteine virali e inoltre fungono da stampi per la sintesi del dsRNA ad opera della RNA polimerasi-RNA dipendente. Si formano così nuove particelle virali composte da proteine strutturali, funzionali e genoma che vengono rilasciate dalla cellula ospite in seguito alla lisi (fig.4). I rotavirus sono in grado di evadere dal sistema IFN dell’ospite. La NSP1 che si forma in seguito alla traduzione del suo mRNA è un antagonista di IFN in quanto induce la degradazione di fattori come IRF3 e IRF5 che sono invece implicati nell’attivazione di questa molecola.

Filogenesi
| Phylum | Duplornaviricota |
| Classe | Resentoviricetes |
| Ordine | Reovirales |
| Famiglia | Reoviridae |
| Sottofamiglia | Sedoreovirinae |
| Genere | Rotavirus |
| Specie | Rotavirus A-H |
Patogenesi
Questi virus sono trasmessi per via oro-fecale e sono gli agenti eziologici di gastroenterite acuta nei bambini. A livello dell’intestino tenue il virus si lega ai recettori superficiali degli enterociti e penetra in essi mediante endocitosi calcio-dipendente. La replicazione del virus ed il suo rilascio provocano la lisi delle cellule. Le manifestazioni cliniche sono diarrea, che può durare da 2 a 7 giorni, febbre e vomito.
La necrosi degli enterociti infettati concorre alla sintomatologia riducendo la digestione e l’assorbimento dei nutrienti, come conseguenza si ha un accumulo di disaccaridi nel lume intestinale e un aumento della pressione osmotica con richiamo di acqua. La NSP4 codificata dal segmento 10, funge da enterotossina virale in quanto è responsabile dell’aumento della concentrazione di Ca2+ intracellulare e ciò determina la fuoriuscita dalla cellula di ioni Na+, Cl– e acqua con diarrea secretoria e svolgendo così un ruolo patogenetico, infatti ad avvalorare quanto detto, se somministrata nei topi induce una profusa diarrea.
Le infezioni da rotavirus riguardano soggetti di tutte le età ma, negli adulti sono generalmente asintomatiche mentre è durante la prima infanzia che si osservano le manifestazioni cliniche sopra citate. La risposta immunitaria innata limita l’infezione da rotavirus, a questa si aggiunge la risposta immunitaria cellulare e umorale importante per il controllo della replicazione virale e nella protezione da successive reinfezioni. A circa 10 giorni dall’infezione si ha un picco di IgA specifiche che persistono per oltre 2 anni a concentrazioni decrescenti. Nelle reinfezioni invece si producono anticorpi crossreattivi verso più sierotipi e quindi un individuo per avere un’effettiva protezione duratura nel tempo deve venire in contatto con tale virus più di due volte.
Metodi di identificazione
La diagnosi di laboratorio si basa sulla ricerca del virus su campioni fecali o per mezzo di un tampone rettale. Il campione deve essere raccolto entro i primi 4 giorni dall’esordio clinico. Si può procedere con l’immunoelettromicroscopia che impiega anticorpi specifici per aggregare le particelle virali e consente di riconoscere i gruppi A, B e C che sono morfologicamente identici o effettuare il test ELISA come tecnica immunoenzimatica. La RT-PCR (altamente sensibile e specifica) consente invece di ricercare il genoma virale nelle feci.
Terapia
La diarrea provoca disidratazione e perdita importante di elettroliti e per questo la reidratazione per via orale è il trattamento di scelta per ovviare a tale problema. Nel 2006 sono stati brevettati due vaccini vivi attenuati da somministrare per via orale. Entrambi si sono dimostrati efficaci.
Si ringrazia Diego Piacentini per il contributo.
Fonti
- J.Matthijnssens, M. Ciarlet et all., 2008, Recommendations for the classification of group A Rotaviruses using all 11 genomic RNA segments.
- KL. Graham, Y. Takada, B.S. Coulson, 2006, Rotavirus spike protein VP5 binds α2β1 integrin on the cell surface and competes with virus for cell binding and infectivity.
- M. Barro & J.T. Patton, 2007, Rotavirus NSP1 inhibits expression of type I interferon by antagonizing the function of interferon regulatory factors IRF3, IRF5, and IRF7.
- http://viralzone.expasy.org/