Caratteristiche
Il virus della parotite (Mumps virus, MuV) (fig.1) è un virus dotato di envelope appartenente alla famiglia dei Paramyxoviridae, isolato nel 1934 da Goodpasture e Johnson.
I virioni presentano uno spiccato pleiomorfismo, possono infatti avere un diametro compreso tra i 100 e gli 600 nm. Il virus della parotite ha un genoma a RNA monocatenario non segmentato a polarità negativa di 15.384 nucleotidi, organizzato in 7 geni che codificano per 9 proteine sia di tipo strutturale che funzionale (fig.2).
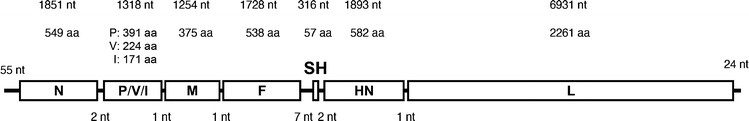
Queste sono:
- la proteina NP, strettamente associata all’RNA virale e che forma anche il nucleocapside elicoidale;
- la fosfoproteina P e la proteina L (large) giocano un ruolo importante nella fase di replicazione virale, infatti fungono da RNA polimerasi- RNA dipendente;
- la proteina V e la proteina SH (small hydrophobic) sono coinvolte nell’inibizione della produzione di IFN (interferone) e del suo signalling, garantendo così l’evasione del virus dalla risposta immunitaria dell’organismo ospite;
- la proteina I, funzione ad oggi poco conosciuta;
- la proteina M (matrice), circonda il nucleocapside ed è associata all’envelope e alle glicoproteine F e HN;
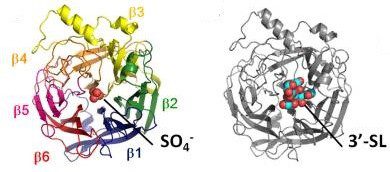
- la glicoproteina HN (fig.3) possiede attività emagglutinante e neuraminidasica; rappresenta l’antirecettore virale, riconosce e lega l’acido sialico (recettore) esposto sulla superficie delle membrane cellulari delle cellule bersaglio;
- la glicoproteina F, di fusione, media l’ingresso del virus nella cellula ospite.
Filogenesi
| Phylum | Negarnaviricota |
| Classe | Monjiviricetes |
| Ordine | Mononegavirales |
| Famiglia | Paramyxoviridae |
| Genere | Rubulavirus |
| Specie | Mumps Virus |
Patogenesi
L’uomo è l’unico serbatoio naturale del virus, del quale esiste un solo sierotipo. L’infezione ha inizio con una prima replicazione nelle cellule epiteliali delle vie aeree superiori, si espande quindi ai linfonodi locali, in cui si replica ulteriormente. Per mezzo del circolo linfatico il virus raggiunge gli organi del sistema reticoloendoteliale e a seguire dopo un’ulteriore fase di replicazione, si ha una fase viremica con la quale il virus raggiunge molti distretti: le parotidi, i testicoli, il pancreas ed il sistema nervoso centrale. La replicazione del virus nelle parotidi genera un’infiammazione locale e un caratteristico rigonfiamento di esse (fig.4).
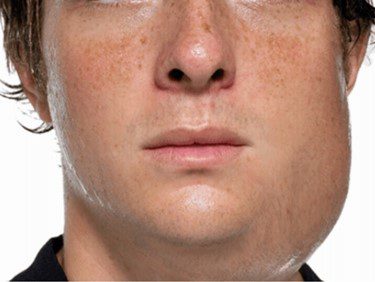
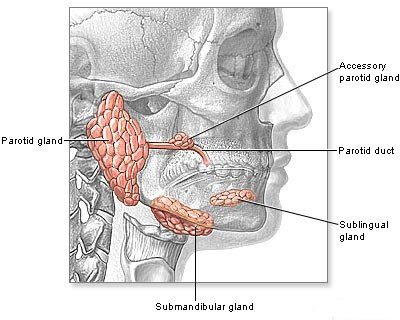
Oltre a tali ghiandole, possono essere interessate anche le ghiandole sottomandibolari e sublinguali (fig.5). Il periodo di incubazione è di circa 2/4 settimane e nelle forme sintomatiche il rigonfiamento di una o entrambi le parotidi ha una durata di circa 2 o 3 giorni, ma può prolungarsi in alcuni casi anche ad una settimana. Il 20-25% dei maschi sviluppa orchite, cioè l’ingrossamento di uno o entrambi i testicoli. Generalmente questo segno clinico si verifica tra i 5 e i 7 giorni dopo l’ingrossamento delle parotidi.
Oltre al dolore causato dalla mancanza dell’elasticità della tonaca albuginea (rivestimento composto da tessuto connettivo denso, fibre elastiche e cellule muscolari lisce che circonda il testicolo), questo disturbo è accompagnato da febbre e cefalea. Il virus della parotite è altamente neurotropico, il coinvolgimento del sistema nervoso centrale (SNC) è frequente ma clinicamente evidente solo nel 10% dei casi. In questi ultimi possono manifestarsi meningite asettica o encefalite (0,02-0,3% dei casi) dopo alcuni giorni dall’ingrossamento delle parotidi.
Metodi di identificazione
La diagnosi risulta necessaria in presenza di rigonfiamenti ghiandolari o nei casi in cui subentrano complicazioni come ad esempio la meningite. I campioni usati per l’indagine sono la saliva, tampone nasofaringeo, sedimento urinario e liquido cerebrospinale raccolti entro pochi giorni dalla comparsa dei sintomi. La ricerca di antigeni MuV viene effettuata con sistemi immunoenzimatici, gli acidi nucleici con metodi molecolari. Il metodo più utilizzato per la ricerca di anticorpi (presenza di IgM nelle prime fasi della malattia) è il test ELISA.
Terapia
Non esiste un trattamento specifico per la parotite, negli individui con orchite ad esempio, vengono impiegati farmaci antinfiammatori al fine di inibire i segni caratteristici del processo infiammatorio come dolore e gonfiore dell’area colpita.
Si impiega un vaccino vivo attenuato per evitare l’insorgenza della patologia; in Italia viene somministrato in combinazione con quelli per morbillo e rosolia, vaccino trivalente MPR (ceppi Jeryl Lynn o Urabe). Nei bambini la prima dose viene effettuata a partire dai 12 mesi compiuti e comunque entro i 15 mesi d’età. La seconda viene attualmente eseguita a 5-6 anni. Essendo un vaccino vivo attenuato, la vaccinazione non viene effettuata nei soggetti con deficit immunitario o a donne in gravidanza.
Si ringrazia Diego Piacentini per il contenuto
Fonti
- M. Brgles, M. Bonta, M. Šantak, B. Halassy, M. Marchetti-Deschmann, 2016, Identification of mumps virus protein and lipid composition by mass spectrometry.
- M. Kubota, K. Takeuchi et all., 2016, Trisaccharide containing α2,3-linked sialic acid is a receptor for mumps virus.
- S. Rubin, M. Eckhaus et all., 2015, Molecular biology pathogenesis and pathology of mumps virus.
- www.epicentro.iss.it