Incremento della popolazione mondiale e nuove necessità
Il costante incremento della popolazione mondiale, dovuto all’avanzamento tecnologico e all’incremento del welfare globale, sta suscitando nella comunità scientifica mondiale serie preoccupazioni inerenti alla disponibilità, all’uso e alla gestione delle risorse naturali ed alimentari del nostro pianeta.
Il consumo crescente di carne sta causando lo sviluppo di allevamenti sempre più intensivi con notevoli ripercussioni di natura ambientale, poiché una delle principali fonti di gas serra, ed in particolare di metano, è rappresentata proprio da allevamenti di bestiame.
Di contro, l’assunzione di proteine da parte dell’uomo è fondamentale per una corretta alimentazione. Per questi motivi, molti ricercatori da diversi anni stanno studiando e ottimizzando fonti proteiche alternative a quelle animali, come ad esempio le proteine prodotte da colture cellulari mediante processi fermentativi.
L’obiettivo di questo settore della ricerca è quello di migliorare il benessere degli animali e la sostenibilità ambientale degli allevamenti animali.
Un innovativo processo biotecnologico per la produzione di proteine
Un gruppo di ricercatori dell’Università di Tubinga, in Germania, guidati dal Prof. Largus Angenent, hanno messo a punto una piattaforma biotecnologica in grado di trasformare alcune risorse di scarto e il bio-idrogeno derivante da fonti rinnovabili, in proteine commestibili.
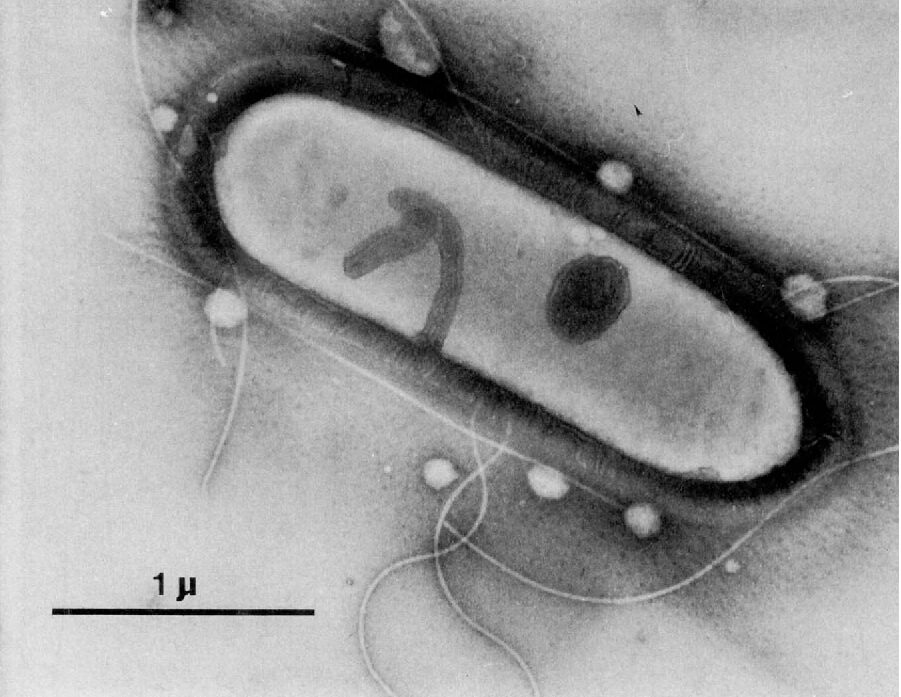
Il team di ricercatori ha ideato un processo che genera biomassa di lievito contenente una frazione proteica del 40-50% in peso. Si tratta di un bio-processo a due stadi che utilizza il batterio Clostridium ljungdahlii (Fig. 1) nel primo stadio per convertire idrogeno e anidride carbonica in acetato attraverso il pathway metabolico Wood-Ljungdahl di fissazione del carbonio (Fig. 2). Questo percorso biochimico è preferibile perché permette di non introdurre contemporaneamente ossigeno e idrogeno nel bioreattore, evitando, in questo modo, problemi di sicurezza.

Nel secondo stadio, una cultura pura di Saccharomyces cerevisiae (lievito di birra e panificazione) viene utilizzato in un secondo bioreattore per convertire, in presenza di ossigeno, l’acetato e l’ammoniaca in proteine di interesse alimentare (Fig. 3). L’ammoniaca utilizzata in questo secondo step potrebbe provenire da flussi di rifiuti industriali o addirittura dall’urina umana diluita in un’ottica di economia circolare, in cui lo scarto diventa risorsa.

L’aspetto innovativo
Nella letteratura scientifica sono già riportati processi biotecnologici in grado di produrre proteine di interesse alimentare, tuttavia, i processi già noti prevedono l’utilizzo dello zucchero (solitamente glucosio), come fonte di carbonio per la crescita dei microrganismi. Per cui la produzione di queste proteine sarebbe legata ancora all’agricoltura o più in generale allo sfruttamento di biomasse vegetali.
Con questo processo innovativo, invece, si potrebbe usare l’elettricità ottenuta da fonti rinnovabili (es. eolico e fotovoltaico) per effettuare l’elettrolisi dell’acqua, producendo l’ossigeno e l’idrogeno necessari per il bio-processo proposto. In questo modo, l’impatto ambientale e l’impronta di carbonio del processo di produzione delle proteine sarebbe notevolmente inferiore rispetto alla produzione di carne mediante gli allevamenti intensivi.
Ad oggi, l’unica azienda in grado di commercializzare proteine di origine microbica è la Quorn. Il processo messo a punto da questa azienda è caratterizzato da una produttività di 1.25 g/L/h. Per generare quantità industriali, il sistema a due stadi messo a punto da Angenent e colleghi dovrebbe essere 14 volte più produttivo, in quanto finora il team ha raggiunto solo una produttività di 0.07 g/L/h. Inoltre, un altro aspetto da ottimizzare consiste nel riciclaggio dell’anidride carbonica persa nella seconda fase, poiché solo il 25% del carbonio fissato nel primo step diventa biomassa nello step successivo.
L’impatto della ricerca
L’idea di produrre cibo a base di proteine di origine microbica ottenute da scarti potrebbe rivoluzionare il sistema produttivo del futuro in un’ottica di sostenibilità ambientale e tecnologica. Produrre cibo attraverso i microrganismi, insieme all’utilizzo di bio-carburanti e fonti energetiche rinnovabili e sostenibili, potrebbe essere una speranza per l’intero pianeta.
Nicola Di Fidio
Sitografia
- Katie Morrey (settembre 2019, ChemistryWorld). Microbes and renewable energy turn carbon dioxide into edible protein. Estrapolato da: https://www.chemistryworld.com/news/microbes-and-renewable-energy-turn-carbon-dioxide-into-edible-protein/3010920.article
Bibliografia
- Molitor, B., Mishra, A., & Angenent, L. T. (2019). Power-to-protein: converting renewable electric power and carbon dioxide into single cell protein with a two-stage bioprocess. Energy & Environmental Science.
Crediti immagini
- https://www.chemistryworld.com/news/microbes-and-renewable-energy-turn-carbon-dioxide-into-edible-protein/3010920.article
- https://www.semanticscholar.org/paper/Clostridium-ljungdahlii-sp.-nov.%2C-an-acetogenic-in-Tanner-Miller/a714870612ebd802c4839ac211a33010f9892bfd/figure/0
- https://en.wikipedia.org/wiki/Wood%E2%80%93Ljungdahl_pathway
I commenti sono chiusi.