Il microbiota intestinale e la terapia antitumorale
Il ruolo del microbiota intestinale nello sviluppo del cancro e nell’efficacia del suo trattamento è stato ampiamente confermato da diversi studi condotti, tanto in modelli animali come nell’uomo. In particolare, Akkermansia muciniphila sembra essere in prima linea nella risposta positiva all’immunoterapia anti-PD in pazienti affetti da melanoma. Tuttavia, il suo ruolo e quello di altri generi batterici in tumori maligni apparentemente non associati al tratto gastro-intestinale, è ancora poco conosciuto.
Delle nuove scoperte in questo ambito sono state appena pubblicate sulla prestigiosa rivista scientifica Nature communications, da parte di un gruppo di ricera della University of Western Ontario, in Canada. I ricercatori hanno dimostrato come la terapia di deprivazione androgenica, somministrata a pazienti affetti da cancro alla prostata, abbia un effetto diretto sulla composizione del microbiota intestinale, particolarmente sull’abbondanza di determinati generi batterici.
La terapia del tumore alla prostata
Il cancro alla prostata è una patologia maligna che interessa 1 uomo su 7 e che comporta un elevato tasso di morbilità nella popolazione oltre che un enorme carico finanziario per il sistema sanitario. In questi pazienti, tanto in presenza di metastasi come in caso di una cancro localizzato a elevato rischio, si effettua quella che in gergo viene chiamata “castrazione medica”, ossia una terapia ormonale di deprivazione di androgeni, tramite analoghi dell’ormone di rilascio delle gonadotropine o GnRH.
In caso di resistenza alla terapia ormonale, il trattamento prevede una terapia a base di abiraterone acetato (AA), un composto che agisce da antagonista del recettore degli androgeni. L’AA è scarsamente assorbito a livello intestinale e quasi del tutto escreto nelle feci. La prolungata residenza a livello del colon dell’AA acetato ha fatto accendere la lampadina ai ricercatori canadesi: il microbiota intestinale potrebbe usufruire di questo “rifiuto umano” a suo vantaggio.
Microbiota ed efficacia terapeutica in sperimentazione clinica
Il primo esperimento effettuato dai ricercatori per validare l’ipotesi del coinvolgimento del microbiota intestinale è stato valutare come, tanto i pazienti trattati con castrazione medica come quelli trattati con AA, fossero caratterizzati da una specifica firma microbiologica rispetto ai pazienti controllo non trattati. I risultati dimostrarono il particolare coinvolgimento dei generi batterici Akkermansia muciniphila e Corynebacterium.
Corynebacterium è un genere batterico noto per la sua capacità di metabolizzare il testosterone. E’ comunemente presente a livello di siti anatomici ricchi in androgeni, come ad esempio nel tratto urogenitale. La riduzione di Corynebacterium osservata nei pazienti trattati con entrambe le terapie inibitorie degli androgeni dimostra che la privazione degli androgeni circolanti in questi pazienti, induce in maniera indiretta la riduzione dei “batteri mangia testosterone”, nell’intestino.
Ulteriori esperimenti condotti in vitro hanno inoltre dimostrato l’inibizione selettiva del composto AA nei confronti di Corynebacterium e Akkermansia muciniphila. Il primo esperimento consisteva nella preparazione standardizzata di inoculi fecali selettivi provenienti da 8 pazienti controllo, in una coltura anaerobica durante 24 ore (Immagine 1). I risultati ottenuti hanno confermato quanto osservato in vivo: la terapia anti-androgeni facilita la crescita di Akkermansia muciniphila e ostacola la colonizzazione di Corynebacterium.
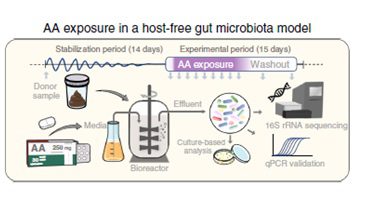
Dalla clinica alla biologia
Il secondo esperimento in vitro realizzato si è servito di un modello artificiale dell’intestino umano per osservare l’effetto di un determinato trattamento in una coltura poli-microbiologica standardizzata.
Anche in questo caso, i risultati ottenuti hanno confermato la promozione della crescita di Akkermansia muciniphila da parte dell’AA. Allo stesso tempo i generi Klesbiella, Biolophila, Oscillobacter, Hungatella erano più abbondanti dopo l’esposizione all’AA.
Evidentemente, dietro l’evidente funzione protettiva di Akkermansia muciniphila, si cela una rete di connessioni tra diversi generi batterici che collaborano tra di loro in maniera positiva o negativa per ottenere una risposta generale a livello metabolico. E’ interessante ad esempio osservare che l’azione di Akkermansia muciniphila sembra essere negativamente associata a generi batterici produttori di butirrato, normalmente considerati benefici per la salute metabolica dell’ospite.
Uno sguardo d’insieme pertanto, che propone nuove conferme e interessanti osservazioni sulla rete di connessioni tra ceppi batterici diversi che si nasconde dietro alla dichiarazione di responsabilità del nostro amato microbiota intestinale.
Dalla biologia all’attivazione del metabolismo batterico
Una volta identificato il protagonismo di Akkermansia muciniphila nei pazienti trattati con AA i ricercatori si sono avventurati a descriverne il ruolo metabolico attraverso la costruzione di un modello di predizione. I risultati ottenuti hanno rivelato l’aumentata attivazione delle vie metaboliche associate al ciclo del gliossilato e della vitamina K2, entrambe di origine batterica. La sintesi del succinato e dell’acetato tramite l’attivazione del ciclo del gliossilato e, contemporaneamente, la sintesi microbiologica della vitamina K2, forniscono una spiegazione funzionale del coinvolgimento di Akkermansia muciniphila nell’esito del trattamento contro il cancro.
I ricercatori suggeriscono che elevate concentrazioni di acetato a livello del colon potrebbero accelerare la crescita di Akkermansia muciniphila agendo come una fonte diretta di energia oltre che innescare l’espressione di geni coinvolti nella degradazione della mucina, per cui questo batterio è particolarmente esperto. Allo stesso tempo, gli studiosi propongono un’alimentazione crociata nei confronti della famiglia batterica Enterobacteriaceae, la cui crescita sembrerebbe essere stimolata dal metabolismo di batteri degradanti la mucina, come Akkermansia muciniphila.
Insomma, abbiamo davanti un quadro generale del tipo “o tutto o niente”: una scena variopinta con una cascata di eventi imprescindibili in cui ogni singolo attore svolge il suo ruolo fondamentale. Gli attori ce li abbiamo, gli eventi anche. Signori, la scenetta è pronta per essere rappresentata nel prossimo show: il trattamento del cancro.
Serena Galiè
Fonti
- Daisley, B.A., Chanyi, R.M., Abdur-Rashid, K. et al. Abiraterone acetate preferentially enriches for the gut commensal Akkermansia muciniphila in castrate-resistant prostate cancer patients. Nat Commun 11, 4822 (2020). https://doi.org/10.1038/s41467-020-18649-5
- https://www.eurekalert.org/pub_releases/2020-09/lhri-gmm092920.php