Premessa
La prevalenza dei disordini cardio-metabolici (obesità, diabete di tipo 2 e malattie cardiovascolari) è in progressiva crescita in tutto il mondo ed è una delle prime cause di mortalità globale. Nella patogenesi di tali disordini sono implicati sia fattori genetici che fattori ambientali.
Considerato il ruolo attribuito ai valori aumentati di colesterolemia nella genesi delle alterazioni che possono determinare le patologie cardiovascolari e visto il crescente interesse sul ruolo del microbiota intestinale nell’origine delle patologie dell’apparato vascolare, si sta cercando di indagare e comprendere quale sia la correlazione tra microbiota intestinale e dislipidemie con particolare riguardo al metabolismo del colesterolo.
Di recente, il microbiota intestinale e i suoi metaboliti sono entrati a pieno titolo tra i possibili target per cercare di controllare i livelli di colesterolo ematico e, di conseguenza, migliorare la funzionalità vascolare e ridurre il rischio di aterogenesi. Trimetilammina-N-ossido (TMAO), per esempio, che è uno dei prodotti batterici, ha mostrato di indurre aterosclerosi in modelli animali
Gli acidi grassi a catena corta (SCFAs), quali l’acido propionico, l’acido butirrico, l’acido acetico, sono tra i metaboliti batterici (i cosiddetti postbiotici) che hanno dimostrato di esercitare benefici diversi sulla salute: modulano la funzione del sistema immunitario, controllano la proliferazione cellulare e le riserve energetiche.
In questo articolo si propone di fare il punto sulle conoscenze attuali riguardanti il rapporto tra propionato e dislipidemie.
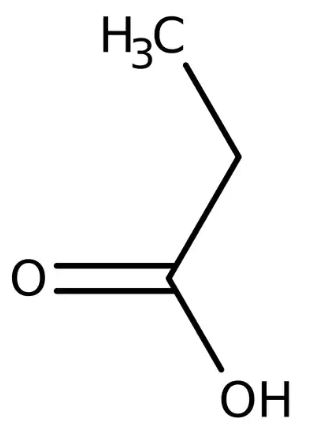
Propionato e assorbimento del colesterolo
L’assorbimento del colesterolo alimentare avviene a livello dell’intestino tenue, soprattutto nel duodeno e nel digiuno del tubo digerente. La molecola del propionato (Fig. 1), prodotto dai batteri presenti nell’intestino, mediatore immunitario, potrebbe influenzare il metabolismo del colesterolo intestinale agendo sul suo trasportatore epiteliale, influenzando cioè l’espressione del trasportatore (una proteina transmembrana) del colesterolo noto come NPC1L1 un trasportatore attivo che veicola la molecola dal lume intestinale all’enterocita.
L’acido propionico, in particolare, è risultato implicato nel controllo dell’immunità mediata dai linfociti T (T-cells) e, perciò, nel decorso di patologie autoimmuni, promuovendo la differenziazione verso le cellule T regolatorie (Tregs). L’acido propionico ha poi mostrato benefici anche nel caso dell’ipertensione. È infatti ormai noto come l’assunzione di fibre prebiotiche, che stimolano la produzione di SCFA da parte del microbiota intestinale, svolga un effetto benefico sulla salute cardiovascolare e, nello specifico, in grado di contrastare le dislipidemie.
Acido propionico e rischio cardiovascolare
I ricercatori hanno studiato come l’acido propionico possa regolare i livelli di lipoproteine in modelli murini modificati che non esprimono le apolipoproteine E (apoE-/-), che sono trasportatori plasmatici di colesterolo, e in pazienti con ipercolesterolemia.
Iniziando dal controllo dei livelli di lipidi plasmatici in vivo, dopo eventuale intervento antibiotico per la deplezione batterica, dieta standard o ad alto contenuto di grassi per 6 settimane, si è osservato che nel gruppo con microbiota soppresso i livelli di VLDL e LDL totali sono risultati maggiori della controparte non trattata con antibiotici indipendentemente dalla dieta, supportando il ruolo generale del microbiota; l’aumento dei livelli di colesterolo è risultato associato a un parallelo aumento di lesioni aterosclerotiche; il supplemento esogeno di acido propionico (200 mg/kg) ha, di contro, prevenuto l’aumento di VLDL e LDL correlato a dieta ricca di grassi soprattutto nel gruppo pre-trattato con antibiotici, suggerendo come l’acido propionico possa compensare modulando l’espressione Niemann-Pick C1-like protein 1(NPC1L1), principale trasportatore transmembrana del colesterolo nonché responsabile del suo assorbimento.
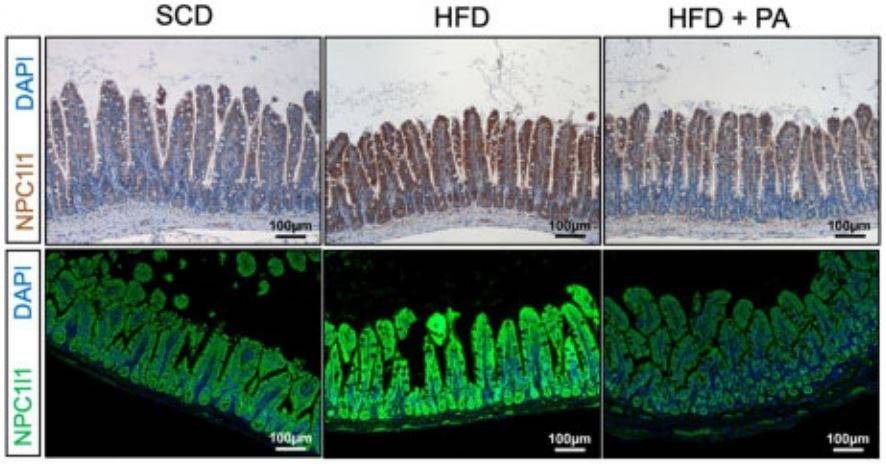
Il dato interessante è un aumento della concentrazione di NPC1L1 nelle sezioni istologiche intestinali di modelli murini apoE-/- alimentati con alto contenuto di grassi rispetto alla dieta standard. Tale accumulo è stato tuttavia contrastato dal supplemento con acido propionico (Fig. 2).
I livelli plasmatici di stigmasteroli e sitosteroli (usati come indicatori di assorbimento intestinale) hanno mostrato un aumento in seguito ad alti contenuti di grassi, situazione anche in questo caso mitigata dall’acido propionico.
Acido propionico e sistema immunitario
In uno studio specifico di quest’anno, pubblicato su European Heart Journal, Haghikia A. ed altri suoi colleghi hanno esplorato i meccanismi d’azione dell’acido propionico anche dal punto di vista immunitario. Precedenti studi hanno infatti dimostrato come sia, per esempio, attivamente coinvolto nel controllo del metabolismo sistemico dei linfociti T intestinali. Anche in questo caso, il supplemento di acido propionico ha indotto un aumento di cellule Treg e interleuchine-10 (IL-10 una citochina ad azione antinfiammatoria) nell’intestino tenue. Nessuna altra alterazione è stata invece registrata in relazione ad altre cellule immunitarie quali Th1 o Th17, monociti, IL-6, TNF-alfa.
L’acido propionico è in grado di regolare indirettamente l’assorbimento di colesterolo agendo su NPC1L1 attraverso IL-10. Le evidenze osservate in vivo sono state testate su un campione di 62 pazienti con ipercolesterolemia constatando una tendenza analoga. In particolare il trattamento con acido propionico per otto settimane ha ridotto significativamente i livelli sierici di lipoproteine LDL e colesterolo totale rispetto al gruppo con placebo, ha supportato lo sviluppo fenotipico di cellule T periferiche con un aumento di Treg senza però alterare i livelli di linfociti Th17 e Th1. Quindi, una dieta ricca di grassi e colesterolo provoca uno squilibrio delle cellule immunitarie nel microambiente dell’intestino tenue, con ridotte frequenze delle cellule Tregs e concentrazioni di IL-10.
I livelli alterati delle cellule Tregs vengono corretti dall’integrazione di propionato esogeno, che modula l’espressione di NPC1L1 e la densità della membrana, con una conseguente riduzione dell’assorbimento del colesterolo, portando così ad una ridotta aterogenesi.
La figura 3 rappresenta schematicamente l’azione dell’acido propionico verso l’aumento del colesterolo e l’aterosclerosi.

Conclusioni
Lo studio riportato sottolinea il ruolo dell’acido propionico prodotto della fermentazione batterica nel diminuire l’assorbimento del colesterolo intestinale attraverso un pathway immunitario, illustrando così un ruolo chiave nella prevenzione e nel controllo delle dislipidemie. Il supplemento orale di acido propionico ha dimostrato, anche a livello clinico, di migliorare i livelli delle lipoproteine LDL e HDL contribuendo quindi alla salute cardiovascolare.
Tra i principali fattori coinvolti, e sui quali l’acido propionico va ad agire, vi sono il trasportare NPC1L1 ed il mediatore IL-10. Questo ci porta a dedurre che una alimentazione più ricca di fibre ad azione prebiotica che stimolino la produzione di SCFA ha, quindi, tutte le carte in regola per diventare una strategia di modulazione nutrizionale del microbiota con la finalità di prevenire le patologie cardiovascolari.
Il microbiota intestinale, pertanto, con i suoi metaboliti come l’acido propionico, potrebbe essere uno strumento di grande potenzialità terapeutica per il controllo delle dislipidemie.
Fonti
- Haghikia A., Zimmermann F., Schumann P. et al. “Propionate attenuates atherosclerosis by immune-dependent regulation of intestinal cholesterol metabolism” European Heart Journal, Volume 43, Issue 6, 7 February 2022, Pages 518–533
- https://www.fishersci.it/shop/products/propionic-acid-99-pure-acros-organics/10634622
- Immagine in evidenza: https://media.istockphoto.com/photos/human-heart-with-blocked-arteries-picture
Salve, ho il livello de LDL alto 4,4. Ho prova abbassarlo con là Berberina e l’alimentazione, ma non è sceso. Dove posso acquistare l’acido propionico? Grazie
Salve Nina, la berberina non agisce tanto sulle LDL, agisce più che altro sull’insulino-resistenza (e sulla motilità intestinale, il microbiota…).
L’acido propionico lo produce già il suo microbiota, potrebbe valutare la presenza di ceppi produttori di propionato con un test del microbiota colonico e qualora non ci fosse una produzione sufficiente cercare di modulare.