Caratteristiche
Providencia stuartii è un batterio gram negativo anaerobio facoltativo, appartenente alla famiglia delle Enterobacteriaceae, di forma bastoncellare, mobile per la presenza di flagelli, catalasi positivo, ossidasi negativo, non fermentante il lattosio e non in grado di produrre forme di resistenza quali le spore. P. stuartii rientra tra i patogeni opportunisti in grado di causare infezioni correlate all’assistenza (ICA), comunemente localizzato nel suolo, nell’acqua e nelle acque reflue. Ad oggi, si conoscono 8 specie di Providencia sp, quali: P. alcalifaciens, P. vermicola, P. sneebia, P. burhodogranaeriae, P. heimbachae, P. rustigianii, P. rettgeri e P. stuartii, la specie di più frequente riscontro nell’uomo causa di infezioni urinarie correlate a catetere. Le specie P. rettgeri e la P. alcalifaciens sono invece associate a manifestazioni gastroenteriche, tra cui la diarrea del viaggiatore, forti dolori addominali, coliche e diarrea persistente.
P. stuartii, secondo la classificazione OMS, rientra nel secondo livello dei gruppi di rischio e può essere lavorato in laboratori di biosicurezza BSL-2.
Filogenesi
| Dominio | Prokaryota |
| Regno | Bacteria |
| Phylum | Pseudomonadota |
| Ordine | Enterobacterales |
| Famiglia | Enterobacteriaceae |
| Genere | Providencia |
| Specie | P. stuartii |
Morfologia delle colonie
P. stuartii cresce bene in condizioni di laboratori standard, in terreni arricchiti ed incubati a 37 °C, in agar nutriente e/o brodo nutriente. Il terreno di elezione è il MacConkey Agar, dove le colonie dopo incubazione a 24 ore appariranno piccole, leggermente irregolari e incolori (Fig.1). La crescita può essere visibile anche su terreni particolarmente arricchiti, come il Simmons Citrate Agar utilizzato per la differenziazione delle Enterobacteriaceae, il cui principio si basa sull’utilizzo del citrato: è un terreno a becco di clarino la cui provetta non inoculata presenta un colore standard verde, ed il suo viraggio nel colore blu indica la crescita dell’agente patogeno e l’utilizzo del citrato come unica fonte di carbonio (Fig.2).
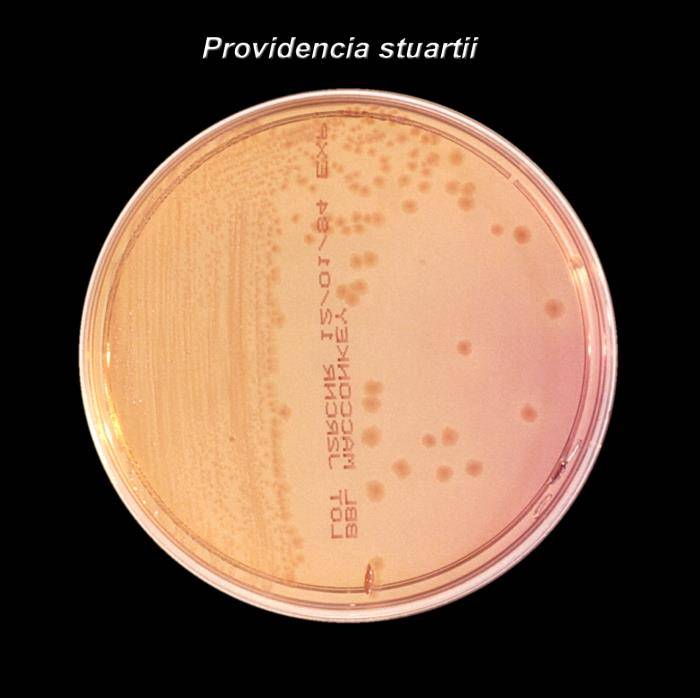

Altri terreni arricchiti il cui utilizzo può essere di supporto nella ricerca di P. stuartii sono l’HiCrome Mueller Hinton, raccomandato per la differenziazione cromogenica di microrganismi e per la determinazione della sensibilità di quest’ultimi agli antibiotici, dove le colonie appaiono piccole e generalmente di colore marrone. L’utilizzo di questo terreno in particolare è estremamente utile nello screening dei patogeni causa di infezioni urinarie, differenziati in base al colore in cui contemporaneamente è possibile discriminare la sensibilità agli antimicrobici (Fig.3).
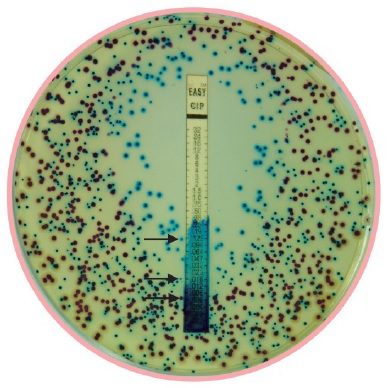
Infine, un ulteriore terreno utilizzabile per la ricerca di P. stuartii è l’Urea Agar Base, anch’esso a becco di clarino il cui principio, a differenza del Simmons, si basa sulla produzione dell’enzima ureasi, la cui positività è data dal viraggio del colore del terreno dal giallo al rosa acceso.
Patogenesi
P. stuartii è l’agente patogeno di più frequente riscontro nell’uomo, in particolare nelle infezioni ospedaliere urinarie associate all’utilizzo prolungato del caterere: questo espone le persone anziane ad un rischio maggiore di infezione da Providencia, responsabile per il 9% delle UTI. Non di rado è presente una co-infezione con Proteus mirabilis, con un aggravamento del quadro clinico del paziente. P. stuartii produce ureasi batterica, un importante fattore di virulenza associato alla formazione di calcoli urinari, pielonefrite acuta ed ostruzione di cateteri urinari permanenti / a lungo termine. Nei pazienti anziani la mortalità può essere purtroppo molto alta, specie in chi presenta altre comorbidità. Oltre che dalle urine, può essere isolato anche da altri materiali biologici, come feci e sangue.
Questa specie batterica è inoltre responsabile della cosiddetta sindrome della sacca urinaria viola o sindrome delle urine viola, generalmente asintomatica ma caratterizzata appunto dalla colorazione violacea delle urine. La sintomatologia dell’infezione da P. stuartii può essere simile ad altre infezioni batteriche, per cui è essenziale la diagnosi differenziale. Sintomi riscontrati sono febbre, letargia, vomito, urine maleodoranti, urgenza urinaria, ematuria, oliguria e poliuria – questi tre in particolare riscontrati quasi sempre.
La sepsi è ovviamente di origine urinaria ed è associata, all’esame obiettivo, a tachicardia, ipotensione e febbre.
Metodi di identificazione
I metodi di identificazione per la ricerca di P. stuartii prevedono l’utilizzo di tecniche di microbiologia standard, come esami colturali su terreni specifici (MacConkey, Simmons, etc), isolamento, colorazione di Gram e identificazione batterica con MALDI-TOF con successivo antibiogramma.
L’antibiogramma, sia con tecniche manuali che con metodiche automatizzate è di estrema importanza per impostare al più presto una specifica terapia antibiotica in particolare nei pazienti anziani e/o immunocompromessi, data la resistenza a più antimicrobici di questo agente patogeno.
Terapia
La terapia di maggiore utilizzo per le infezioni urinarie e le batteriemie da P.stuartii prevede in prima linea le cefalosporine, come ceftriaxone, cefotaxime, cefepime, cefixima, sostituibili in caso di allergia con i betalattamici. Un’altra alternativa è rappresentata dagli aminoglicosidi, a meno che dall’antibiogramma il patogeno non ne sia espressamente resistente.
Per evitare infezioni a monte da Providencia, è fondamentale attuare una buona prevenzione anche e soprattutto in ambito ospedaliero. Imprescindibile è il corretto lavaggio delle mani degli operatori a contatto con il paziente, la cura appropriata e frequente dei cateteri urinari e la rimozione degli stessi quando non più necessari nonché il loro utilizzo solo in condizioni strettamente richieste e/o urgenti.
Priscilla Caputi
Fonti
- Kenneth J. Ryan, C. George Ray. Sherris, Microbiologia Medica. The McGraw Hill Companies, 2017. Edizione Mediche Scientifiche Internazionali.
- Koneman’s. Testo – Atlante di Microbiologia diagnostica. 3 volumi, Antonio Delfino Editore, 6 edizione 2008, 7 edizione 2019.
- Viaggi B., Tascini C., Rossolini GM. Enterobacterales multiresistenti, dal laboratorio alla clinica. Edizioni Medico Scientifiche, Pavia, 2018.
- Kurmasheva, N., Vorobiev, V., Sharipova, M., Efremova, T., & Mardanova, A. (2018). The potential virulence factors of Providencia stuartii: motility, adherence, and invasion. BioMed Research International, 2018.
- Warren, J. W. (1986). Providencia stuartii: a common cause of antibiotic-resistant bacteriuria in patients with long-term indwelling catheters. Reviews of infectious diseases, 8(1), 61-67.
- Wie, S. H. (2015). Clinical significance of Providencia bacteremia or bacteriuria. The Korean journal of internal medicine, 30(2), 167.
- https://microbewiki.kenyon.edu/index.php/Providencia_stuartii
- https://www.microbiologiaitalia.it/didattica/livelli-di-biosicurezza/
- https://www.microbiologiaitalia.it/terreni-di-coltura/urea-broth-base-terreno-di-christensen/
- https://www.microbiologiaitalia.it/terreni-di-coltura/macconkey-agar/
- https://www.microbiologiaitalia.it/batteriologia/maldi-toff-nuova-frontiera-alla-lotta-microbica-in-clinica/
- https://www.microbiologiaitalia.it/microscopia/colorazione-di-gram-distinguere-e-classificare-i-batteri/
- https://www.ncbi.nlm.nih.gov/Taxonomy/Browser/wwwtax.cgi?mode=Info&id=588
- https://microbiologie-clinique.com/simmons-citrate-agar.html
- http://www.kje01.com.tw/wp-content/uploads/2018/10/M2010-HiCrome%E2%84%A2-Mueller-Hinton-Agar-2.pdf
- https://phil.cdc.gov/
- http://www.biolifeitaliana.it/
Crediti immagini
- Immagine in evidenza: https://alchetron.com/Providencia-stuartii
- Figura 1: CDC, Public Health Imagine Library (PHIL)
- Fig. 2: https://microbiologie-clinique.com/simmons-citrate-agar.html
- Fig. 3: https://ridacom.com/en/products/view/7125