Il microbioma è la prima barriera per inibire possibili infezioni. Buoni o non, i batteri intestinali sono pur sempre microrganismi e come tali dovrebbero essere riconosciuti dal sistema immunitario per essere eliminati. Molti studi non hanno trovato risposte per lungo tempo, fin quando un gruppo di ricercatori non ha correlato la presenza di alcuni fagi alla resistenza antibiotica.
Resistenza antibiotica e batteriofagi
Per spiegare lo sviluppo della resistenza del batterio agli antibiotici, si deve far riferimento alla loro interazione con i batteriofagi. Considerando lo scambio di materiale genetico dal fago al batterio, l’Università Nazionale di Singapore e l’Università di Glasgow hanno incentrato le loro ricerche sul meccanismo di replicazione del fago. Infatti, lo studio ha portato alla scoperta di un nuovo meccanismo di scambio del genoma, definito “trasduzione laterale”.
Generalmente, il virus fago infetta la cellula ospite batterica e replica il genoma per poter liberare la maggior quantità di particelle virali possibili. Nel caso di una “trasduzione generalizzata” il batteriofago inietta il genoma nella cellula ospite per replicare il maggior numero di particelle virali. Di conseguenza, la cellula ospite “scoppia” per liberare i virioni.
Per contro, la “trasduzione specializzata” avviene per inserimento del DNA nel genoma batterico. Solo in presenza di stimoli esterni, la cellula ospite replica il genoma del virus e le particelle virali vengono liberate.
Inizialmente, i ricercatori credevano che l’integrazione di frammenti di DNA virale nel genoma batterico fosse un evento occasionale. Lo studio sulla resistenza dello Staphylococcus aureus ha attestato come l’integrazione del genoma virale sia molto frequente. Difatti, prima dell’escissione il genoma virale si integra nel genoma batterico e la “copiatura” della sequenza virale porta con sé anche parti del genoma dell’ospite.
In questo modo, la cellula ospite trasferisce porzioni di genoma ad altri batteri. Questo meccanismo comporta la rapida trasmissione della resistenza ai farmaci.
Un buon esempio: Pseudomonas aeruginosa e resistenza antibiotica
Negli ultimi due anni i casi isolati da infezioni invasive da P. aeruginosa sono diminuiti, anche se i ceppi batterici continuano a presentare resistenza alla maggior parte degli antibiotici. La multi-resistenza è da attribuire alla capacità selettiva che impedisce ai comuni farmaci di penetrare la membrana esterna della cellula.
In particolare, antibiotici come i beta-lattamici (cefalosporine, ceftazidime e cefepime) e carbapenemi associati a inibitori delle beta-lattamasi, piperacillina-tazobactam, sono potenzialmente efficaci, anche se la resistenza a queste classi di farmaci aumenta con il passare degli anni.

D’altra parte, ultimi studi hanno valutato come la presenza dei batteriofagi incentivi la gravità delle infezioni da P. aeruginosa per inserimento del genoma virale nel cromosoma batterico. Proprio questo meccanismo di replicazione “nasconde” il batterio dall’attacco del sistema immunitario.
Il tè verde nella resistenza antibiotica
Molti fitocomplessi e principi attivi vegetali vengono testati per ridurre le resistenze antibiotiche in riferimento ai loro usi millenari. Un esempio è proprio la catechina del tè verde, epigallocatechin gallato (EGCG), presente in maggiore quantità nelle foglie. Proprio quest’ultima è stata testata in azione sinergica ai comuni antibiotici nelle infezioni nasocomiali.

Pseudomonas aeruginosa
A questo proposito, uno studio pubblicato sul Journal of Medicine ha rivelato l’effetto positivo della catechina sull’attività di uno specifico antibiotico attivo contro P. aeruginosa. L’antibiotico in questione è l’aztreonam e il team che ha condotto lo studio ne ha valutato l’attività farmacologica in associazione a epigallocatechin gallato (EGCG).

Un team dell’Università del Surray ha condotto studi in vitro su pelle umana infettata dal batterio ed ha valutato l’efficacia farmacologica dell’aztreonam associato ad EGCG. Allo stesso modo, ulteriori studi sono stati condotti in vivo sulle larve di Galleria Mellonella infettate da batteri.
In entrambi i casi, la presenza di Epigallocatechin gallato ha aumentato notevolmente la permeabilità dell’antibiotico aztreonam, con minimi effetti collaterali.
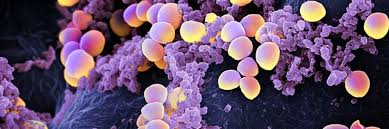
Staphylococcus aureus
Lo stesso vale per il batterio multi-resistente S. aureus. L’associazione di EGCG ai più comuni beta-lettamici e, in particolare, alla oxitetraciclina, ha dato notevoli risultati farmacologici con minimi effetti collaterali.
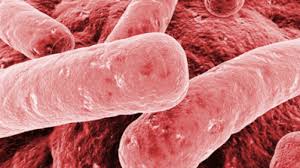
Klebisiella Pneumoniae
Non meno importante il risultato dell’attività sinergica di EGCG ed antibiotico su colonie batteriche di K. pneumoniae. Gli studi sono stati condotti prendendo in esame gli antibiotici clinicamente importanti: ciprofloxacina, gentamicina e tetraciclina.
Allo stesso tempo, dopo uno screening fenotipico, le colonie di K. pneumoniae isolate sono state unicamente quelle che presentavano una maggiore attività della beta-lattamasi e carbapenemasi. Proprio la sinergia di EGCG, coadiuvata da acido caffeico, migliorava l’attività farmacologica dei comuni antibiotici utilizzati contro i ceppi più resistenti.
Nuove strategie
Da questi presupposti, gli obiettivi sono molteplici. Molecole di origine vegetale stanno aprendo la strada ad un nuovo approccio, modulando l’attività di molti farmaci per effetto sinergico. Per contro, studi di valutazione dell’attività del fago in combinazione ad altri batteri, potrebbe dare miglioramenti nel target farmacologico.
Infatti, sia l’azione del fago che l’azione di molecole vegetali potrebbe essere sviluppata a vantaggio di un possibile trattamento per infezioni resistenti e, in aggiunta, per una migliore conoscenza del microbioma e dei batteri che lo popolano.
Bibliografia
- Bellino S., D’Ancona P., Iacchini S., Monaco M., Pantosti A., Pezzotti P., Dipartimento Malattie Infettive, ISS, Iannazzo S., Ministero della Salute, Antibiotico-resistenza, https://www.epicentro.iss.it/antibiotico-resistenza/ar-iss-rapporto-pseudomonas-aeruginosa
- Le Scienze, 2018, https://www.lescienze.it/news/2018/10/15/news/batteriofagi_trasduzione_trasferimento_resistenza_batteri_antibiotici-4153527/
- Febvre H. P. et al., 2019, Nutrients, PHAGE Study: Effects of Supplemental Bacteriophage Intake on Inflammation and Gut Microbiota in Healthy Adults, Review
- Bettis J. et al., 2019, Restoring the activity of the antibiotic aztreonam using the polyphenol epigallocatechin gallate (EGCG) against multidrug-resistant clinical isolates of Pseudomonas aeruginosa, Research Article
- https://notiziescientifiche.it/sostanza-nel-te-verde-utile-nelleliminare-batteri-resistenti-ad-antibiotici/
- Toffolo R., Tè verde (EGCG) nelle infezioni e nell’antibiotico resistenza, https://www.farmacistidivulgatori.it/ptta-portfolio/te-verde-egcg-nelle-infezioni-e-nellantibiotico-resistenza/
- Novy P. et al., 2013, Synergistic interactions of epigallocatechin gallate and oxytetracycline against various drug resistant Staphylococcus aureus strains in vitro, Research article
- Dey D. et al., 2015, Polyphenolic Secondary Metabolites Synergize the Activity of Commercial Antibiotics against Clinical Isolates of β-Lactamase-producing Klebsiella pneumoniae, Research article