Una sorpresa scientifica di fine anno per una delle più emergenti problematiche nella salute pubblica: combattere gli indistruttibili, una classe di batteri antibiotico resistenti denominati ESKAPE (guarda caso, una omatopea della parola escape, in italiano fuga) cioè coloro che sfuggono ai comuni trattamenti.
Una nuova scoperta per la lotta all’antibiotico-resistenza
La scoperta è stata appena pubblicata sulla prestigiosa rivista scientifica Nature da parte di un gruppo di ricerca del Winstar Institute, a Philadelphia (USA), il quale ha presentato una nuova classe di composti chimici in grado di svolgere una duplice azione: uccidere batteri “intrattabili” e stimolare la risposta immunitaria dell’ospite.
Il fenomeno dell’antibiotico-resistenza è stato ormai dichiarato una minaccia globale per la salute pubblica da parte dell’organizzazione mondiale della salute (WHO) e si stima che, entro il 2050, le infezioni antibiotico-resistenti causeranno trilioni di morti e un onere cumulativo attorno ai 100 miliardi per l’economia mondiale.
La lista di batteri resistenti a tutti i trattamenti antibiotici disponibili cresce in maniera esponenziale, contariamente all’offerta di nuovi farmaci, il che si traduce in un’estenuante corsa, da parte della comunità scientifica, alla ricerca di nuove classi di antibiotici in grado di far fronte a questa crisi sanitaria.
In prima linea per questo ambizioso obiettivo c’è il gruppo di ricerca del Vaccine & Immunotherapy Center ideato da Farokh Dotiwala. La nuova generazione di antibiotici presentata dai ricercatori è stata battezzata con il nome di DAIAs (dall’inglese antibiotici immunitari a duplice azione).
DAIA: una classe di antibiotici raffinati
Gli antibiotici normalmente agiscono contro funzioni batteriche vitali, incluse la sintesi di acidi nucleici e proteine, la costruzione della membrana cellulare e determinate vie metaboliche. In risposta, i batteri hanno però sviluppato dei meccanismi in grado di evadere l’efficacia antibiotica, mutando le componenti su cui essi agiscono.
Con gli antibiotici DAIA, si presenta la possibilità di far fronte all’infezione batterica potenziando il sistema immunitario, simultaneamente ad un attacco diretto, per impedire ai batteri Gram-negativi di sviluppare resistenza.
Il bersaglio scelto dai ricercatori per questa nuova classe di antibiotici è una via metabolica chiamata metil-D-eritrol fosfato (MEP) o via del non-mevalonato. Quest’ultimo è responsabile, nei batteri Gram-negativi, nei micobatteri e negli Apicomplexa, della biosintesi degli isoprenoidi, delle molecole essenziali per la loro sopravvivenza. In particolare, l’enzima responsabile della loro sintesi, nonchè target dei nuovi antibiotici, è chiamto IspH.
I nuovi inibitori di IspH
I nuovi inibitori di IspH, a differenza dei comuni antibiotici appartenenti a questa classe, sono capaci di penetrare efficientemente la membrana batterica. Infatti, grazie ad uno studio di docking molecolare, i ricercatori sono stati in grado di raffinare la liberazione di concentrazioni nanomolari del farmaco all’interno dei batteri e provocarne la morte per apoptosi (Fig. 1).
Gli esperimenti effettuati in vitro dal team di ricerca ne hanno dimostrato l’efficacia nei confronti di vari isolati clinici multi-resistenti quali i generi Acinetobacter, Pseudomonas, Klebsiella, Enterobacter, Vibrio, Shigella, Salmonella, Yersinia, Mycobacterium e Bacillus.
L’enzima IspH è allo stesso tempo in grado di attivare le cellule umane citotossiche T a concentrazioni molto basse, quindi dare avvio ad una risposta immunitaria da parte dell’ospite. Contemporaneamente, I composti studiati, si sono dimostrati sicuri e non tossici per le cellule umane, prive dell’enzima IspH.
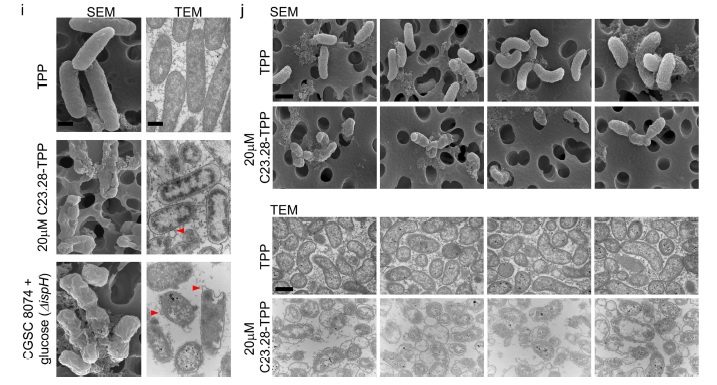
Un’arma a duplica azione per l’antibiotico resistenza
Riteniamo che questa innovativa strategia DAIA possa rappresentare un potenziale punto di riferimento nella lotta mondiale contro l’antibiotico-ressitenza, creando una sinergia tra la capacità di uccisione diretta degli antibiotici e il potere naturale del sistema immunitario.
Così dichiara Farokh Dotiwala, l’autore principale della pubblicazione su Nature.
Farokh Dotiwala è un assistente professore del Wistar Institute impegnato nella ricerca contro l’antibiotico-resistenza. A lui si deve la scoperta del meccanismo di microptosi, il processo di apoptosi programmata dei microrganismi da parte del nostro sistema immunitario. Questo meccanismo, attivato dalle cellule T, porta alla secrezione di perforine, che perforano le membrane delle cellule infettate, granulisine che entrano all’interno delle cellule batteriche ed infine di granzimi, che innescano una cascata enzimatica in grado di uccidere il batterio.
Dato che i batteri non sviluppano resistenza nei confronti di microptosi, Dotiwala ha deciso di dedicare la sua ricerca allo sviluppo di nuove strategie terapeutiche che sfruttino questo meccansimo di difesa immunitaria. E possiamo dire che gli sforzi compiuti stanno ottenendo ottimi risultati.
Serena Galiè
Fonti
- Singh, K.S., Sharma, R., Reddy, P.A.N. et al. IspH inhibitors kill Gram-negative bacteria and mobilize immune clearance. Nature (2020). https://doi.org/10.1038/s41586-020-03074-x
- https://www.sciencedaily.com/releases/2020/12/201223125759.html
- https://wistar.org/news/press-releases/wistar-receives-support-more-55m-private-foundations-and-funding-agencies
- Dotiwala F et al., Killer lymphocytes use granulysin, perforin and granzymes to kill intracellular parasites. Nat Med. 2016 Feb;22(2):210-6. doi: 10.1038/nm.4023.