L’adenosintrifosfato (o ATP) è la principale fonte energetica usata delle cellule. Sfortunatamente, essa non si trova libera in natura ma deve essere prodotta a seguito di un lungo processo che ha come passaggio chiave quello attraverso l‘ATP sintasi, un macchinario molecolare presente nei mitocondri senza il quale la sintesi di ATP non sarebbe possibile. In questo articolo andremo ad scoprire la struttura, il funzionamento e cosa comporta un malfunzionamento dell’ATP sintasi.
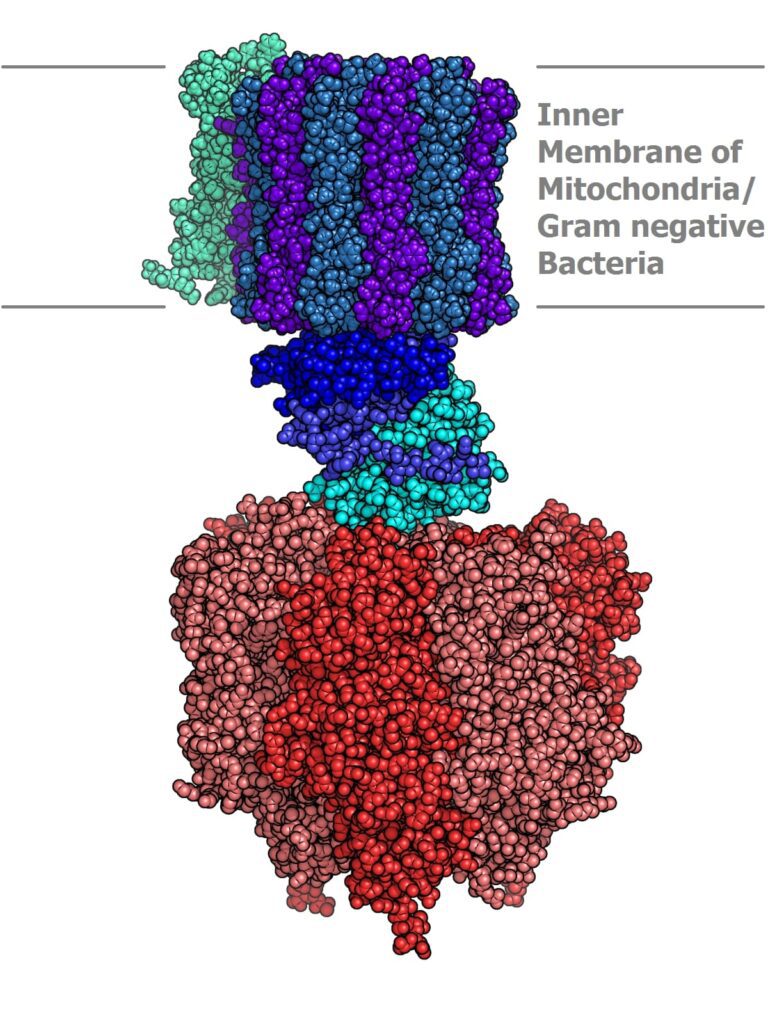
Struttura dell’ATP sintasi
L’ATP sintasi è formata da due subunità denominate F0 ed F1. La subunità F1 protende verso la matrice mitocondriale mentre F0 ha una natura principalmente idrofobica. In particlare, in Homo sapiens il segmento F1 è composto da tre subunità alfa, tre beta, una gamma, una delta e una epsilon. Il segmento F0 dell’ATP sintasi, è invece legato alla membrana mitocondriale ed è costituito da una struttura circolare composta da vari monomeri (detta c-ring), dalle subunità a, b ,d, F6 e dall’OSCP (oligomycin sensitivity-conferring protein).
A livello evolutivo le due subunità sembrano essersi evolute indipendentemente una dall’altra, tuttavia la loro associazione sembra essere avvenuta in epoche molto antiche data l’importanza che l’ATP riveste per le cellule. Studi molecolari hanno rilevato come la subunità F1 sia simile alla DNA elicasi mentre la subunità F0 mostra una notevole similarità funzionale al meccanismo che aziona i flagelli.
La sintesi di ATP da parte dell’ATP sintasi
Il processo di sintesi dell’ATP è già stato ampiamente descritto in altri articoli, pertanto in questo paragrafo ci soffermeremo sul ruolo centrale dell’ATP sintasi. Due, infatti, sono i fattori che permettono la sintesi di ATP
- la presenza di un gradiente protonico presente nei mitocondri tra la membrana interna e lo spazio intermembrana
- la conformazione molecolare dell’ATP sintasi
Il gradiente protonico permette ai protoni di fluire dallo spazio intermembrana alla membrana interna mitocondriale in un passaggio obbligato attraverso la subunità F0 dell’ATP sintasi. Questo passaggio attraverso il c-ring innesca una serie di cambiamenti conformazionali che si propagano per tutta la proteina fino ad arrivare alla subunità F1, dove avviene la sintesi di ATP a partite da ADP e fosfato inorganico. Infatti, queste rotazioni generano un cambiamento conformazionale a livello della subunità beta che, in base a quale stato del ciclo catalitico si trova, può legare ADP e fosfato inorganico, legare ATP neosintetizzato o rilasciare la molecola di ATP neosintetizzata.
Mutazioni sui geni dell’ATP sintasi
Da quanto detto sopra risulta evidente l’importanza dell’ATP sintasi per il metabolismo cellulare ed è facile comprendere come delle mutazioni nei geni di questa proteina portino a delle conseguenze cliniche piuttosto serie. Al giorno d’oggi le principali mutazioni sono presenti sui geni mitocondriali MT-ATP6 e MT-ATP8. La mutazione m.8993T>G sul gene MT-ATP6 è considerata una delle più serie e porta alla NARP, una patologia mitocondriale associata a neuropatia, atassia (controllo dei muscoli difficoltoso) e alla retinopatia pigmentosa. A livello biochimico si assiste a una marcata riduzione di sintesi di ATP e a una diminuzione del livello di funzionalità dell’ATP sintasi. Le mutazioni interessano il c-ring ed essendo esso il “motore” dell’ATP sintasi, un suo malfunzionamento causa il fenotipo sopra descritto.
L’altro sito di mutazione ampiamente studiato si trova sul gene mitocondriale MT-ATP8 e le mutazioni portano a problematiche cardiache, neurologiche, e di movimento.
Terapie
Esistono diversi terapie dirette a migliorare la vita dei pazienti che presentano mutazioni nella sequenza dei geni che codificano per l’ATP sintasi. Considerando che nei soggetti si ha un accumulo di specie reattive dell’ossigeno (ROS), molecole come l’N-acetilcisteina (NAC) sono risultate efficaci in studi in vitro. Oltre ai più classici approcci farmacologici, la terapia genica sembra essere un approccio promettente. Tra le varie opzioni di terapia, esiste la possibilità di esprimere un gene wild type (ossia perfettamente funzionante) che sintetizza le proteine che compongono l’ATP sintasi non nel mitocondrio, ma bensì nel nucleo della cellula. Un’altra opzione possibile è quella di usare delle nucleasi per rimuovere il gene mutante e riprestinare la funzionalità del gene wild type.
Fonti
- Jonckheere AI, Smeitink JA, Rodenburg RJ. Mitochondrial ATP synthase: architecture, function and pathology
- David L Nelson Michael M Cox, I principi di biochimica di Lehninger – Settima edizione. A cura di Edon Melloni. ISBN: 9788808920690
- https://en.wikipedia.org/wiki/ATP_synthase
Crediti immagini
- Immagine di copertina e figura 1: https://it.wikipedia.org/wiki/ATPasi_trasportante_H%2B_tra_due_settori#/media/File:Atp_synthase.PNG