Caratteristiche generali
L’insieme di tutte le reazioni chimiche che mantengono in vita la cellula, permettendole di interagire con l’ambiente esterno, costituisce il metabolismo (dal greco μεταβολή, cambiamento). Le vie metaboliche consentono, quindi, la crescita e la riproduzione dei microrganismi. La capacità di adattarsi alle condizioni esterne rappresenta un punto di forza fondamentale per le cellule batteriche. Difatti, è proprio grazie a tale attitudine, e quindi grazie alla varietà di vie metaboliche possibili, che le specie batteriche possono sopravvivere in un ampio range di condizioni diverse.
Tutte le vie metaboliche sfruttate dalle cellule microbiche si ritrovano a far parte di una rete, un network appunto, di pathway, metaboliti ed enzimi interconnessi e interdipendenti (Fig.1).
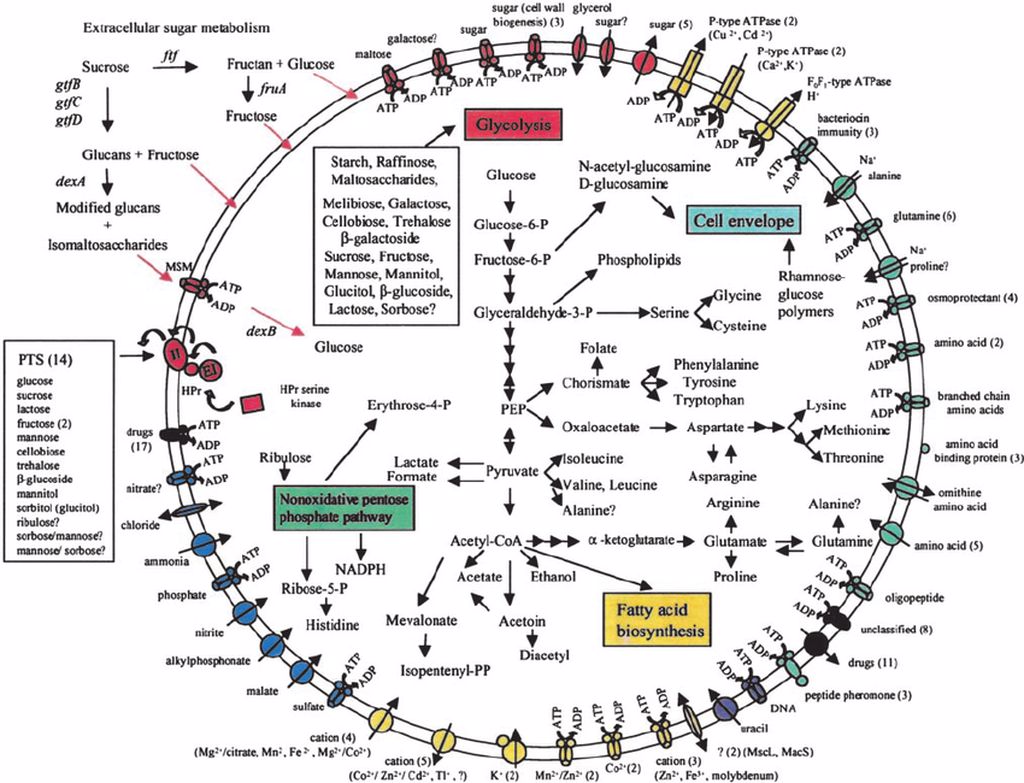
Qualunque sia il loro scopo, i pathway metabolici possono essere distinti in: lineari, dove ogni enzima usa il prodotto dello step precedente; ciclici, nei quali si vanno a rigenerare le molecole di partenza; a spirale, dove gli enzimi non riescono a discriminare tra uno specifico substrato ed un altro formato durante la reazione.
Metabolismo energetico
Le cellule microbiche utilizzano il metabolismo energetico, o catabolismo, per ricavare energia a partire da molecole complesse, che vengono scisse in componenti monomeriche più semplici. Grazie alla rottura dei legami presenti nelle molecole si riesce a liberare energia chimica. Le reazioni che costituiscono il metabolismo energetico sono dette reazioni esoergoniche. Il metabolismo batterico di tipo energetico può compiersi con tre diverse modalità: fermentazione, respirazione e fotosintesi. Fermentazione e respirazione condividono una fase iniziale di metabolismo del glucosio, ovvero la via metabolica della glicolisi, dove lo zucchero viene convertito in acido piruvico, con conseguente rilascio di energia. In realtà, la glicolisi può essere sostituita in alcuni casi dalla via di Entner – Douderoff, usata da alcuni Gram-negativi, o dalla via dei pentoso-fosfati, tipica invece dei batteri acidolattici.
Fermentazione
La fermentazione rappresenta il meccanismo catabolico più semplice, in cui i composti organici coinvolti svolgono la duplice funzione di donatori e di accettori di elettroni. Come già detto, questa avviene a partire dal prodotto della glicolisi, l’acido piruvico. Alcune delle fermentazioni che distinguiamo in base al prodotto finale sono:
- lattica, produce lattato ed è tipica dei lattobacilli;
- alcolica, produce etanolo;
- propionica, genera propionato ed è tipica dei batteri propionici (ad esempio Propionibacterium acnes);
- butirrica, produce butirrato ed è tipica dei batteri dei genere Clostridium;
- acetica, genera acetato ed è tipica dei batteri acetici;
Respirazione
La via catabolica della respirazione può, invece, avvenire secondo due meccanismi, in relazione alla presenza di ossigeno: respirazione aerobica e anaerobica. In entrambi in casi, i composti organici o inorganici fungono da donatori di elettroni. Il ruolo di accettore finale di elettroni è a carico dell’ossigeno molecolare, nel caso del processo aerobico, oppure a carico di un composto inorganico, nel caso del processo anaerobico.
Nella respirazione aerobica, il piruvato prodotto dalla glicolisi entra nel ciclo di Krebs sotto forma di acetil-CoA, dove vengono sintetizzati elementi fondamentali per l’ultimo step della respirazione ma anche precursori necessari ai processi biosintetici. Il meccanismo finale prevede la fosforilazione ossidativa, in cui gli elettroni arrivano all’ossigeno tramite una catena di trasporto e si ha la massima produzione di energia.
La respirazione anaerobica vede principalmente l’utilizzo di solfati, nitrati e carbonati come accettori finali di elettroni. Un catabolismo di questo tipo si ritrova in batteri denitrificanti, batteri solfato-riduttori e batteri metanogeni. Esempi di respirazione anaerobica sono infatti la denitrificazione, la riduzione degli ioni solfato e la metanogenesi.
Fotosintesi
Infine, la fotosintesi è il meccanismo catabolico più raro ed implica l’utilizzo della luce come fonte di energia. La via ha inizio con l’assorbimento della luce grazie alla presenza di pigmenti all’interno della cellula e la successiva trasformazione dell’energia luminosa in energia chimica di legame, grazie alla sintesi di molecole energetiche. Il meccanismo è prettamente anaerobico e si parla infatti di fotosintesi anossigenica. I batteri fotosintetici, per lo più anaerobi obbligati e anaerobi facoltativi, mettono in atto questo tipo di processo. Nel caso in cui vi sia produzione di ossigeno, si parla di fotosintesi ossigenica, accostata per semplicità a quella delle piante e tipica dei cianobatteri.
Metabolismo biosintetico
Le cellule microbiche sfruttano il metabolismo biosintetico, o anabolismo, per produrre molecole di grandi dimensioni, a partire da bulding blocks più piccoli. Nelle vie anaboliche si vanno a produrre macromolecole e costituenti della biomassa, attraverso una serie di reazioni di polimerizzazione che richiedono energia. L’idrolisi di molecole energetiche, come l’ATP, permette di ricavare tale energia. In questo caso si parla di reazioni endoergoniche. Le vie di biosintesi dei microrganismi seguono la classificazione delle biomolecole che compongono il materiale organico, di conseguenza si hanno meccanismi di sintesi di: nucleotidi, amminoacidi, acidi grassi e zuccheri. Infine, anche il processo di fissazione dell’azoto può essere considerato come un ulteriore pathway anabolico, poiché vede la formazione di ammoniaca a partire dall’azoto gassoso. Tale ammoniaca viene poi utilizzata dalla cellula per la biosintesi di molecole azotate, come nucleotidi e amminoacidi.
Biosintesi di nucleotidi
I nucleotidi hanno un ruolo molto importante nella cellula. Diversamente da quanto si potrebbe pensare questi non vanno a costituire soltanto gli acidi nucleici, ma sono i precursori di un’ampia varietà di molecole. I nucleotidi, ad esempio, sono i componenti di alcune molecole energetiche, ma anche di cofattori di ossidoriduzione, intermedi attivati e messaggeri cellulari. Il processo di sintesi viene distinto nella formazione della componente zuccherina e nella formazione della base azotata. In relazione, poi, alla natura della base azotata esistono due tipi di meccanismi: un meccanismo raffinato, per le purine, e un meccanismo semplice, per le pirimidine.
Le purine (adenina e guanina) sono sintetizzate a partire dall’acido inosinico, che funge da precursore, mentre le pirimidine (timina, citosina e uracile) si formano tutte da una molecola di uridilato.
Biosintesi di amminoacidi
A differenza dei mammiferi, le cellule batteriche sono in grado di sintetizzare tutti e 20 gli amminoacidi. I precursori di queste vie biosintetiche sono generalmente metaboliti e molecole prodotti durante le vie cataboliche principali. I pathway anabolici che producono amminoacidi si dividono in 5 famiglie, in relazione alla molecola che funge da precursore:
- alfa-chetoglutarato, da cui si ottengono glutammato, glutamina, prolina e arginina;
- aspartato, da cui si ottengono aspartato, asparagina, lisina, metionina, treonina e isoleucina;
- fosfoenolpiruvato, da cui si ottengono gli aromatici fenilanalina, tirosina e triptofano;
- piruvato, da cui si ottengono alanina, valina e leucina;
- 3-fosfoglicerato, da cui si ottengono serina, glicina e cisteina.
Infine, un pathway biosintetico separato, che parte invece dal fosforibosilpirofosfato, permette di produrre istidina.
Biosintesi di acidi grassi
I lipidi costituiscono una componente importante delle membrane citoplasmatiche e della membrana esterna dei Gram-negativi. Questi possono essere utilizzati anche come fonte di carbonio ed energia. I principali componenti dei lipidi microbici sono gli acidi grassi, sintetizzati tramite l’inserimento di singole coppie di atomi di carbonio ad opera dell’enzima ACP. Il meccanismo anabolico è differente a seconda che si tratti di acidi grassi saturi o insaturi e lineari o ramificati. Gli acidi grassi prodotti vengono poi assemblati in lipidi tramite l’esterificazione degli atomi di carbonio del glicerolo.
Biosintesi di zuccheri
Gli zuccheri, soprattutto in forma di polisaccaridi, rappresentano dei costituenti importanti della parete cellulare dei microrganismi. Inoltre, tali molecole vengono utilizzate dalla cellula come riserva di carbonio ed energia. Generalmente, i polisaccaridi sono sintetizzati a partire da forme attivate di glucosio, come UDPG o APDG. Se la cellula non cresce in presenza di glucosio questo deve essere sintetizzato tramite la via anabolica di gluconeogenesi, che ripercorre all’indietro la via della glicolisi, producendo glucosio a partire da fosfoenolpiruvato.
Categorie nutrizionali
Il metabolismo microbico può essere suddiviso in tre livelli, a seconda delle diverse esigenze delle cellule. In base a come ottengono il carbonio per sintetizzare biomassa, distinguiamo batteri autotrofi (dalla CO2), batteri eterotrofi (da composti organici) e batteri mixotrofi (da entrambi). In base a come ottengono equivalenti riducenti necessari all’anabolismo, distinguiamo batteri litotrofi (da composti inorganici) e batteri organotrofi (da composti organici). Infine, in base a come ottengono energia per vivere e crescere, distinguiamo batteri chemiotrofi (da composti chimici) e batteri fototrofi (dalla luce).
Nelle diverse nicchie ecologiche si potranno ritrovare, quindi, molto categorie nutrizionali differenti:
- Batteri chemolitoautotrofi, ottengono energia dall’ossidazione di composti inorganici e fissano l’anidride carbonica. Ad esempio, i batteri nitrificanti, i batteri solfuro-ossidanti o quelli che ossidano il ferro.
- Batteri fotolitoautotrofi, ottengono energia dalla luce e fissano l’anidride carbonica. Ad esempio, i cianobatteri.
- Batteri chemolitoeterotrofi, ottengono carbonio da composti organici ed ottengono energia dall’ossidazione di composti inorganici. Ad esempio, i batteri nitrificanti o i batteri idrogeno-ossidanti.
- Batteri chemoorganoeterotrofi, ottengono energia, carbonio e equivalenti riducenti dai composti organici. Si tratta della categoria nutrizionale più diffusa e questa comprende Escherichia coli, Pseudomonas spp e Bacillus spp.
- Batteri fosfoorganotrofi, ottengono energia dalla luce ed ossidano composti organici. Ad esempio, Rhodobater e Rhodospirillum.
Ruolo degli enzimi nel metabolismo
Nella vasta rete del metabolismo microbico, un ruolo fondamentale è svolto dagli enzimi. Si tratta di molecole di origine proteica, utilizzate come catalizzatori biologici, poiché capaci di accelerare le reazioni chimiche all’interno delle vie metaboliche. L’azione dei catalizzatori biologici permette di trasformare una sostanza di partenza, il substrato, in un’altra sostanza, il prodotto, attraverso un meccanismo che vede la formazione temporanea di un complesso intermedio, definito complesso enzima-substrato. Il meccanismo di azione degli enzimi (Fig.2) è consentito dalla presenza del sito attivo, una “tasca” nella struttura tridimensionale della proteina, all’interno del quale il substrato penetra per essere successivamente trasformato in prodotto. Proprio grazie alla presenza delle molecole enzimatiche le reazioni che costituiscono le vie metaboliche possono avvenire in tempi compatibili con le necessità della cellula.
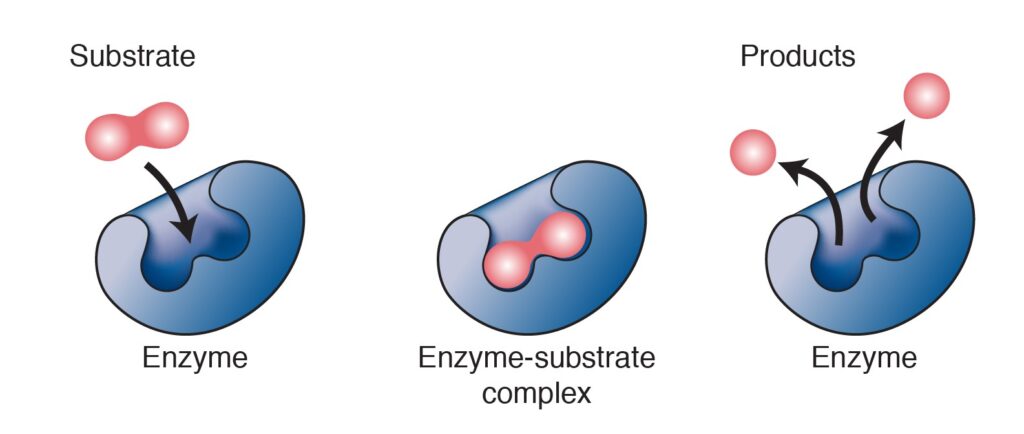
Inoltre, ogni enzima coinvolto in una via metabolica corrisponde ad un possibile punto di controllo per quella specifica pathway. Il meccanismo di regolazione può coinvolgere gli enzimi allosterici, dove un legame reversibile con uno o più modulatori, generalmente metaboliti o piccole molecole, va a modificarne l’attività. Ma in realtà, il meccanismo più frequente nelle cellule batteriche è quello di controllo trascrizionale. Questo regola direttamente il numero degli enzimi espressi dalla cellula ed è maggiormente efficace in risposta a variazioni meno repentine e più durature nel tempo.
Molecole chiave del metabolismo
Oltre agli enzimi, esiste una serie di molecole necessarie e fondamentali in ambito metabolico: le molecole energetiche e i cofattori accettori di elettroni.
L’ATP (adenosina trifosfato) è una molecola formata da una base azotata, l’adenina, uno zucchero pentoso, il ribosio, e da tre gruppi fosfato (Fig. 3). Questa costituisce una vera e propria moneta di scambio utilizzata nei pathway metabolici. Nelle reazioni anaboliche l’ATP viene idrolizzata ad ADP + P per liberare l’energia necessaria alla sintesi. In quelle cataboliche, invece, le molecole di ATP vengono sintetizzate per immagazzinare l’energia liberata dalla degradazione delle macromolecole.

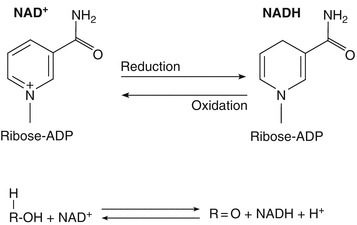
I cofattori sono molecole necessarie agli enzimi per esplicare la loro attività catalitica. Nel caso specifico dei cofattori accettori di elettroni, detti cofattori di ossidoriduzione, si fa riferimento a specifiche molecole che costituiscono il potere riducente della cellula. I cofattori di ossidoriduzione più noti sono NAD (nicotinammide adenin dinucleotide) e FAD (flavin adenin dinucleotide). Durante un reazione chimica, queste molecole, presenti in forma ossidata, vengono modificate chimicamente e passano alle forme ridotte NADH e FADH2 (Fig.4). I cofattori redox permettono il trasporto di elettroni nella cellula, determinando l’immagazzinamento dell’energia derivante dalle reazioni chimiche in cui sono coinvolti. Per completare il ciclo catalitico e utilizzare in modo controllato tale energia, i due cofattori devono ritornare alla forma originaria e ciò può avvenire anche a carico di un enzima diverso. Altri cofattori di ossidoriduzione importanti sono il NADP e il FMN.
Fonti
- Madigan, Martinko, Stahl, Bender, Buckley. Brock. Biologia dei microrganismi. Pearson. ISBN: 9788891900944
- Ajdić D, McShan WM, McLaughlin RE, Savić G, Chang J, Carson MB, Primeaux C, Tian R, Kenton S, Jia H, Lin S, Qian Y, Li S, Zhu H, Najar F, Lai H, White J, Roe BA, Ferretti JJ. Genome sequence of Streptococcus mutans UA159, a cariogenic dental pathogen. Proc Natl Acad Sci U S A. 2002 Oct 29;99(22):14434-9. doi: 10.1073/pnas.172501299. Epub 2002 Oct 23. PMID: 12397186; PMCID: PMC137901.
- Enzyme (genome.gov)
- Carrà S. (2018) Devils, Ratchets and Biomolecular Motors. In: Stepping Stones to Synthetic Biology. The Frontiers Collection. Springer, Cham. https://doi.org/10.1007/978-3-319-95459-2_1
- Ziegler M. (2013) Nicotinamide Adenine Dinucleotide (NAD). In: Roberts G.C.K. (eds) Encyclopedia of Biophysics. Springer, Berlin, Heidelberg. https://doi.org/10.1007/978-3-642-16712-6_42
Fonti immagini
- Figura 1 – Ajdić D, McShan WM, McLaughlin RE, Savić G, Chang J, Carson MB, Primeaux C, Tian R, Kenton S, Jia H, Lin S, Qian Y, Li S, Zhu H, Najar F, Lai H, White J, Roe BA, Ferretti JJ. Genome sequence of Streptococcus mutans UA159, a cariogenic dental pathogen. Proc Natl Acad Sci U S A. 2002 Oct 29;99(22):14434-9. doi: 10.1073/pnas.172501299. Epub 2002 Oct 23. PMID: 12397186; PMCID: PMC137901.
- Immagine 2 – Enzyme (genome.gov)
- Figura 3 – Ziegler M. (2013) Nicotinamide Adenine Dinucleotide (NAD). In: Roberts G.C.K. (eds) Encyclopedia of Biophysics. Springer, Berlin, Heidelberg. https://doi.org/10.1007/978-3-642-16712-6_42
- Immagine 4 – Ziegler M. (2013) Nicotinamide Adenine Dinucleotide (NAD). In: Roberts G.C.K. (eds) Encyclopedia of Biophysics. Springer, Berlin, Heidelberg. https://doi.org/10.1007/978-3-642-16712-6_42