“Allarme rosso, ripeto, allarme rosso. Soggetto non ben identificato si aggira nelle nostre linee di sicurezza, richiediamo rinforzi.”. Sirene iniziano ad echeggiare, i pannelli di controllo si mobilitano, i volontari vengono buttati giù dalle brande ed ancora un po’ intorpiditi dall’apparente riposo si preparano agli armamenti.
Qualcuno non ha mai affrontato alcun nemico, qualcuno invece è un veterano e di esperienza ne ha da vendere. Non sanno cosa esattamente li aspetterà, ma una cosa è certa: la vittoria deve essere loro. Loro sono nati per difendere ciò che li circonda, un qualcosa di prezioso: l’UOMO.
Sulla scia del film “Inside-Out”, se potessimo immaginare come funzioni l’intricato mondo dentro di noi in una situazione di potenziale pericolo, la scena appena descritta potrebbe essere un buon inizio. Se fossimo poi inoltre i registi di questa opera, non potremo che affidare la prima battuta di questo incipit a loro, i nostri primi agenti di sicurezza: I macrofagi.
Identikit di un macrofago
I macrofagi sono cellule fagocitiche localizzate in modo costitutivo nei tessuti deputati a reagire rapidamente in seguito all’ingresso di microbi. Essi fanno parte del plotone dell’immunità innata, quel ramo del sistema immunitario che per primo entra in gioco per la nostra difesa.
Questo plotone è caratterizzato da meccanismi di difesa pre-esistenti all’infezione e proprio per questo non è dotato di specificità ma di rapidità di azione. In alcuni casi l’immunità innata può bastare per scampare il pericolo. Però nella maggior parte di questi rappresenta un metodo geniale per temporeggiare, limitare il raggio di azione del nemico, attendendo che i rinforzi, dotati di armi pesanti (immunità adattiva), arrivino per eradicarlo.
Macrofagi non si è, ci si diventa.
I macrofagi prendono origine da una cellula staminale ematopoietica che intraprende il percorso verso la linea differenziativa mieloide a livello del midollo osseo (Figura 1). Questo precursore sotto pressione di elementi come il fattore stimolante le colonie di monociti (M-CSF), tende a differenziarsi in monoblasto. Questo poi seguendo il processo differenziativo raggiungerà lo stadio di monocita.
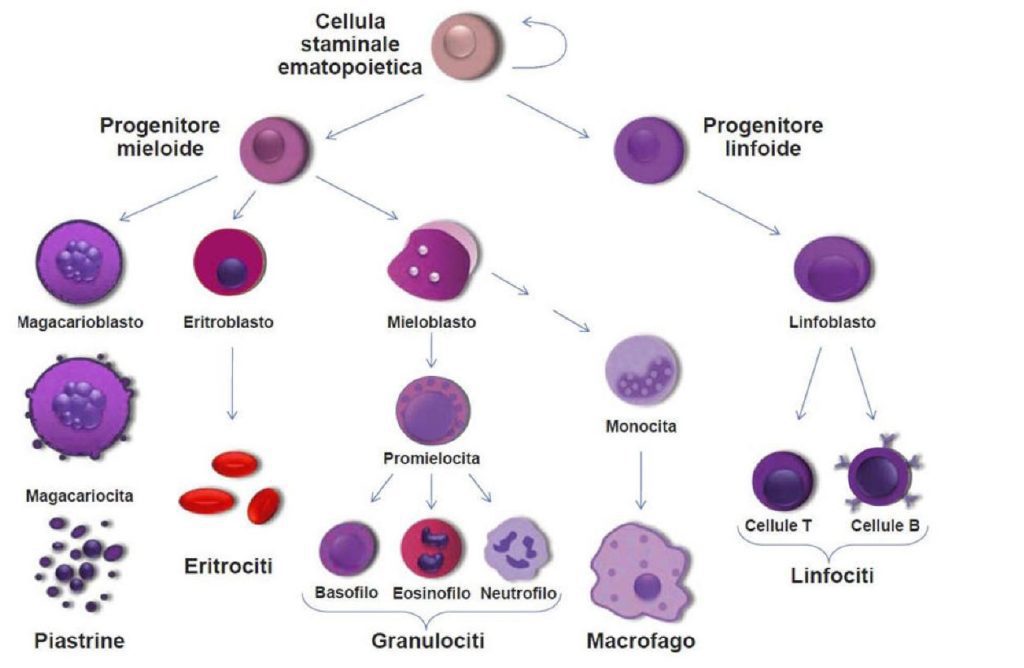
Una volta raggiunto questa fase, il monocita viene riversato nel torrente circolatorio. I monociti in circolo sono circa 500-1000/mm3, hanno un diametro di 10-15 micron, un nucleo a fagiolo ed un citoplasma contenente lisosomi, vacuoli fagocitici e filamenti di citoscheletro.
Classificazione dei monociti
I monociti sono eterogenei e si possono suddividere in due sottotipi classificabili per marcatori di membrana e cinetica di migrazione nei tessuti:
- monociti infiammatori: così definiti in quanto saranno reclutati dal sangue ai tessuti in caso di infezione/infiammazione
- monociti che daranno origine ai macrofagi residenti nei tessuti.
Quest’ultimo sottotipo entrerà nei tessuti, dove, sotto azione di fattori locali, effettuerà il suo ultimo step differenziativo acquisendo caratteristiche citomorfologiche differenti in base alla sede colonizzata, diventando macrofagi (Figura 2).
La loro presenza in tessuti diversi è definita da nomi che ne determinano la localizzazione specifica. Infatti i macrofagi che per esempio rivestono i sinusoidi vascolari del fegato prendono il nome di cellule di Kupffer, quelli presenti nel sistema nervoso centrale sono identificati come cellule della microglia, nelle vie aree polmonari vengono definiti macrofagi alveolari e così via.
Rispetto al monocita, il macrofago appare dimensionalmente più grande, presenta un nucleo pressochè rotondeggiante, un citoplasma ricco di lisosomi e reticolo endoplasmatico rugoso e apparato di Golgi molto sviluppati, per le funzioni che vedremo successivamente.

Classificazione dei macrofagi
Queste cellule, come agenti appostati, colonizzano maggiormente le zone dove è possibile avere una maggior probabilità di incontrare qualche estraneo e bloccarne il passaggio. Essi si suddividono in due tipologie:
- i macrofagi residenti: quiescienti, adesi alla matrice extracellulare tramite prolungamenti citoplasmatici che ne conferiscono una struttura stellata, sono i veri e proprio agenti appostati, silenziosi, fissi, attenti e scrutatori.
- I macrofagi attivati: attivati da processi infiammatori o infezioni, grazie ad un rimodellamento citoscheletrico acquisiscono capacità di movimento ameboide, per partire all’inseguimento, e sono caratterizzati da una spiccata capacità fagocitaria, per arrestare l’intruso.
Ruolo dei macrofagi
Quali armi sono a disposizione di queste cellule? i macrofagi presentano diverse ed importanti funzioni sia nell’immunità innata che adattativa.
1- FAGOCITOSI:
La principale funzione dei macrofagi è quella di ingerire i microbi. Per permettere questa funzionalità questi agenti, come altre cellule fagocitiche, sono dotati di recettori di membrana in grado di riconoscere i microbi.
Stiamo parlando ad esempio dei recettori scavenger, le lectine di tipo C o i recettori del mannosio. Tutti questi fanno parte dei Pattern Recognition Receptors (PRR), recettori dell’immunità innata, in grado di riconoscere profili molecolari estranei.
Ma sulla superficie di queste cellule possiamo trovare anche recettori a più alta affinità in grado di riconoscere alcune opsonine come ad esempio gli anticorpi.
Non appena un microbo o un suo frammento si lega ad uno di questi recettori, la regione della membrana plasmatica adiacente ad esso subisce un riarrangiamento tale da formare una protrusione che si espanderà fino a raggiungere le dimensioni necessarie a racchiudere l’agente estraneo. Questa vescicola che si viene a formare viene definita Fagosoma (Figura 3).
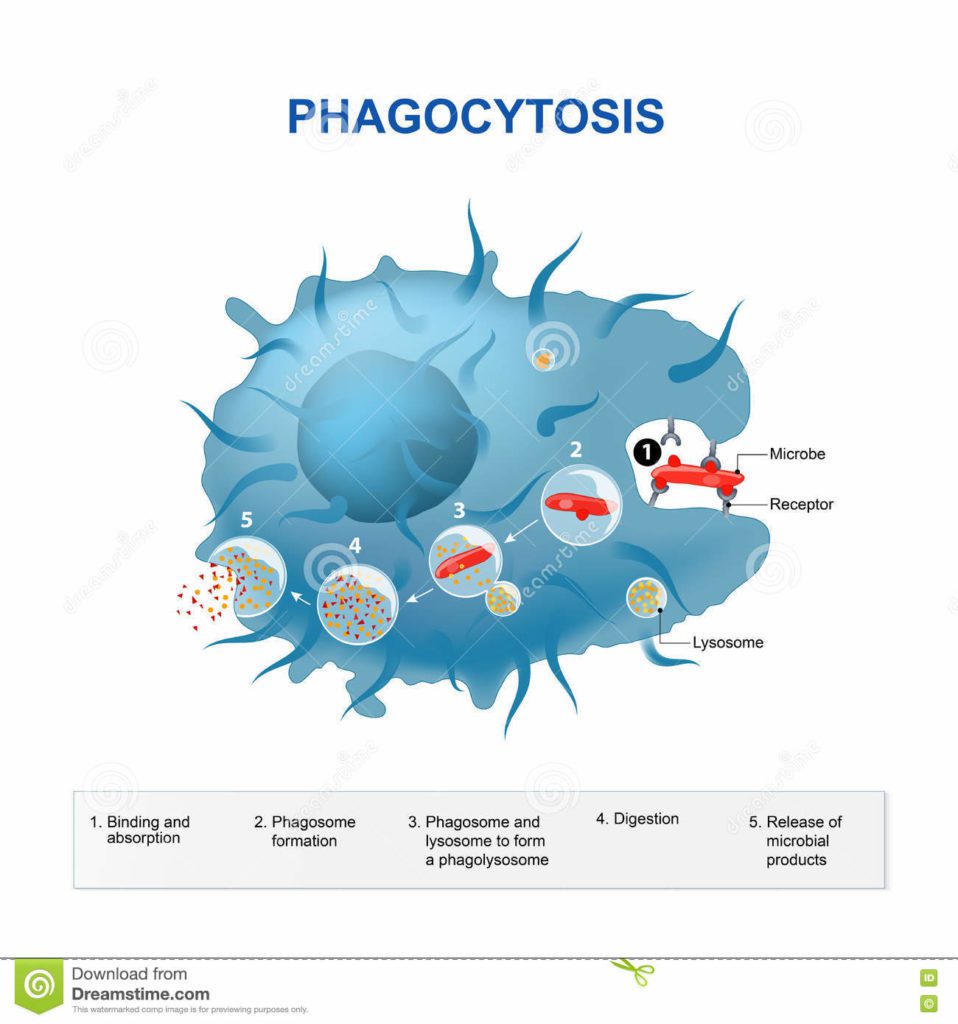
Il fagosoma viene internalizzato nella cellula, dove nel frattempo sono state attivate tutte le vie di segnalazione atte alla produzione di sostanze microbicide, qui va a fondersi con i lisosomi, formando i fagolisosomi, in cui si concentra la maggior parte dei meccanismi microbicidi.
Questi meccanismi possono essere:
- Produzione di specie reattive dell’ossigeno (ROS) in grado di uccidere l’agente estraneo e favorire, all’interno del fagolisosoma, delle condizioni adatte per l’azione degli enzimi proteolitici.
- Produzione di monossido di azoto (NO) che può combinarsi con il superossido di idrogeno o il perossido, per produrre perossinitrito, un radicale altamente nocivo per i microbi.
- Enzimi proteolitici in grado di andare a degradare l’agente patogeno.
2- RISOLUZIONE DEL PROCESSO INFIAMMATORIO:
Ingeriscono e degradano le cellule morte derivanti da un processo infettivo o un danno sterile al tessuto e sono anche in grado di riconoscere e fagocitare le cellule apoptotiche prima che queste possano rilasciare il loro contenuto e determinare un processo infiammatorio.
3- PRODUZIONE DI CITOCHINE:
I macrofagi sono anche capaci di produrre queste preziose molecole, che sono in grado di legarsi e attivare recettori espressi da altri tipi cellulari, come i leucociti, che quindi verranno coinvolti nel processo di difesa. Per esempio, le citochine rilasciate dai macrofagi (IL-1, IL-8, IL-6) sono in grado di legarsi a livello dell’endotelio vascolare per facilitare il reclutamento dei monociti e neutrofili nei siti di infezione, amplificando così la risposta protettiva.
4- PRESENTAZIONE DELL’ANTIGENE:
I macrofagi sono dotati del complesso maggiore di istocompatibilità di classe 2 (MHC II), un recettore di membrana in grado di esporre frammenti di microrganismi extracellulari che vengono captati e metabolizzati nella cellula.
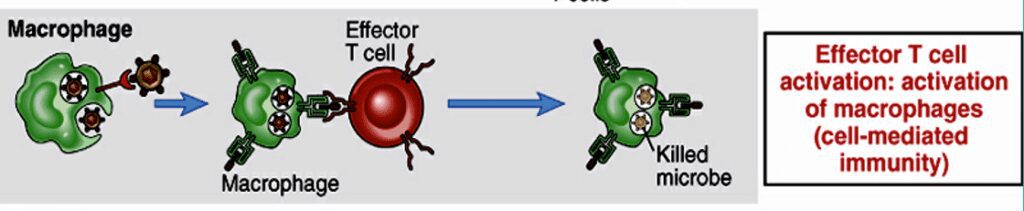
L’MHC II, caricato del frammento estraneo, è in grado di andarsi a legare al recettore dei linfociti T (TCR), il legame permette l’attivazione di quest’ultima classe cellulare e quindi della risposta immunitaria adattativa.
5- RIPARAZIONE TISSUTALE:
Queste cellule sono anche coinvolte nel rimodellamento di tessuti danneggiati stimolando l’angiogenesi e la sintesi della matrice extracellulare ricca in collageno, tramite produzione di TGF-β e IL-10.
Attivazione classica ed alternativa
Come è possibile che queste cellule riescano ad avere un ventaglio così ampio di funzioni?
Tutto dipende dall’ambiente circostante. Diversi stimoli portano i monociti/macrofagi a differenziarsi in sotto-popolazioni funzionalmente distinte.
L’attivazione “Classica” prevede che i macrofagi, identificati con l’acronimo M1, siano stimolati da componenti microbiche e dalle citochine (maggiormente dall’ INF-γ), assumendo maggiormente l’azione microbicida.
L’attivazione “Alternativa” indotta soprattutto dalla produzione di IL-4 e IL-13 prodotte dai linfociti Th2, neutrofili ed altri tipi cellulari invece favorisce l’attivazione di macrofagi (M2) con attività antifiammatorie, spiccate capacità di riparazione tissutale e nei processi fibrotici.
In condizioni patologiche
Cosa potrebbe succedere se i nostri agenti in appostamento venissero fatti lavorare eccessivamente?
Un’eccessiva attivazione di queste cellule può danneggiare i tessuti dell’ospite attraverso la liberazione di tutte quelle sostanze microbicide che essi sono in grado di produrre. Una volta riversate all’esterno, queste sostanze non hanno la capacità di distinguere ciò che è self da ciò che non lo è. Il risultano nocive ovviamente anche per le cellule circostanti, provocando così un danno tissutale.
Nelle infiammazioni croniche, può succedere che i macrofagi, insieme ad altre cellule del sistema immunitario, tendano ad accumularsi. Si forma una sorta di struttura capsulare (granuloma) intorno al sito di infiammazione.
Insomma, questi agenti sono ben addestrati, ma fanno pur sempre parte di un esercito molto più ampio, se salta un pannello di controllo, il sistema va in tilt.
Il Macrofago nella ricerca scientifica
Proprio per le loro molteplici attività e caratteristiche, i macrofagi ad oggi sono sotto l’obiettivo di diverse ricerche scientifiche, stanno diventando dei buoni alleati anche in laboratorio.
A questo proposito si stanno svolgendo delle ricerche per poter utilizzare i macrofagi M2 come target anti-aterosclerosi, per aumentare la capacità di rimodellamento tissutale. Proprio per questa capacità infatti sono molti gli studi che prevedono il loro utilizzo nella medicina rigenerativa.
Si ipotizza che i macrofagi siano un elemento importante da tenere in considerazione nei casi di obesità. Si è notato, infatti, che soggetti obesi presentano un numero maggiore di queste cellule. Questo potrebbe spiegare il loro stato di infiammazione cronica ed oltre tutto il maggior rischio di riscontrare tumori. In aggiunta, ricerche scientifiche mostrano come i macrofagi potrebbero essere implicati nell’omeostasi cardiaca e anche nel mantenimento di una buona conduzione elettrica a livello dello stesso.
Queste sentinelle del sistema immunitario non smettono mai di stupirci. Forse tra non troppo tempo, , non sarebbe sorprendente se alle molteplici funzioni precedentemente elencate se ne aggiungessero di nuove.
Quello che è certo oggi, è che grazie anche a loro, in questo momento, sì, anche in questo momento in cui voi state comodamente leggendo questo articolo, in totale relax, magari sul divano di casa vostra, loro sono sempre lì, attivi, pronti a proteggervi e comunicare con i nostri pannelli di controllo. E Magari se vi concentrate bene potete quasi udire quell’impercettibile vocina che fa: “Tutto ok, Huston, pericolo scampato.”
Ilaria Bellini
Fonti
- “Immunologia cellulare e molecolare” Abul K. Abbas et al. Elsevier.
- Figura 3: https://www.google.com
- https://www.biopills.net
Grazie Dottoressa!! Mi è stata molto utile questa sua spiegazione, fatta davvero benissimo
e aggiungo che ho apprezzato anche la vena simpatica, che non guasta mai, anzi!!