Lieviti oleaginosi
I lieviti oleaginosi sono microrganismi in grado di accumulare elevate quantità di lipidi all’interno delle proprie cellule. La concentrazione di bio-olio intracellulare può variare dal 20% fino al 70% in peso della massa cellulare secca.
L’olio di origine microbica o “single cell oil” rappresenta una promettente alternativa sostenibile agli oli vegetali per applicazioni energetiche e industriali come, ad esempio, la produzione di biodiesel, bioplastiche, biosurfattanti, intermedi chimici e farmaceutici e mangimi per animali.
L’uso di trigliceridi ottenuti da microrganismi oleaginosi (lieviti, batteri e microalghe) per scopi non alimentari permetterebbe di destinare gli oli vegetali edibili esclusivamente alla filiera alimentare evitando, quindi, una competizione di natura etica “food-feed-fuel”, soprattutto nei Paesi in via di sviluppo.
Inoltre, la produzione di un bio-olio di nuova generazione mediante processi fermentativi assicurerebbe una indipendenza dall’alternarsi delle stagioni e dall’estensione del terreno. Due fattori che, invece, influenzano notevolmente la produzione degli oli vegetali tradizionali ottenuti mediante spremitura meccanica dei semi di coltivazioni oleaginose (es. palma, colza, girasole).
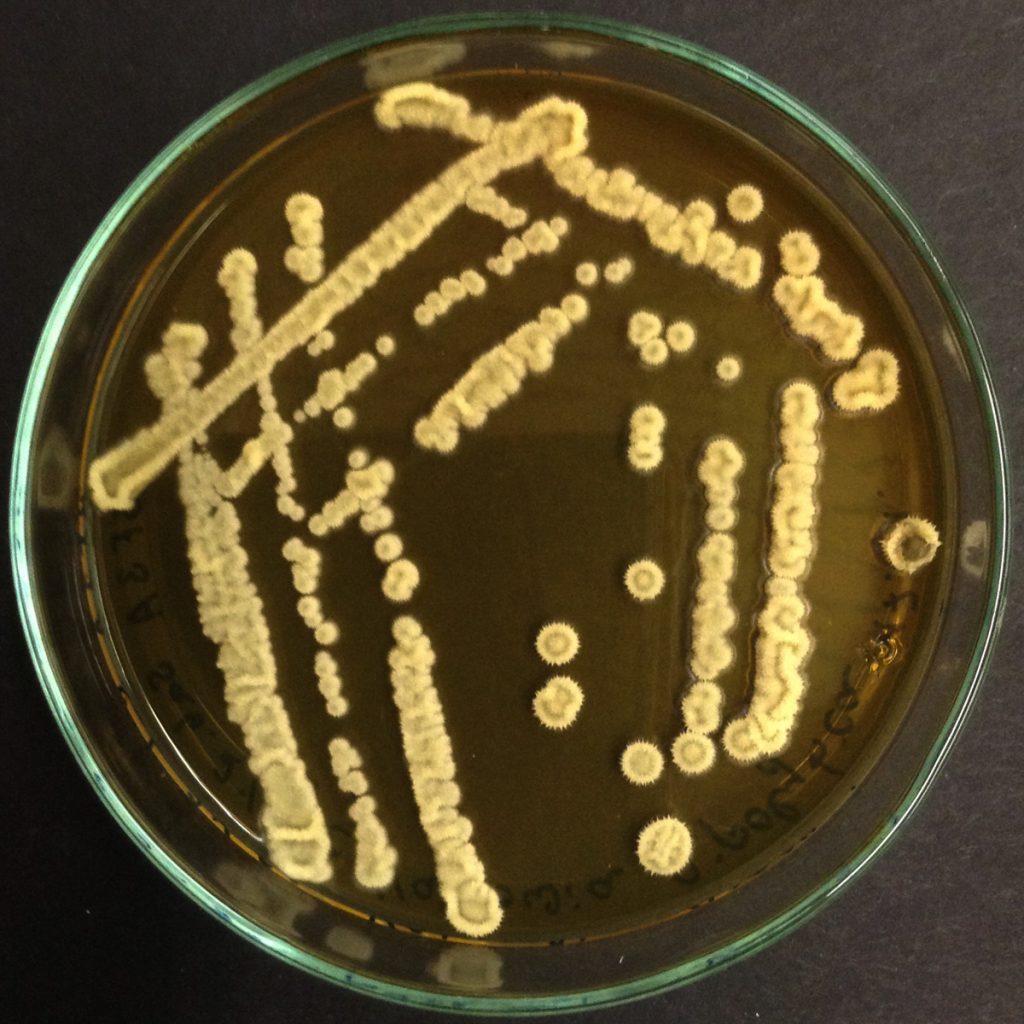
Tra i lieviti oleaginosi, le specie più studiate nella letteratura scientifica sono Yarrowia lipolytica (Fig. 1), Cutaneotrichosporon oleaginosus, Lipomyces starkeyi e Rhodotorula glutinis.
La lipogenesi
L’accumulo di lipidi o “lipogenesi” nei lieviti oleaginosi si verifica quando un nutriente nel mezzo di coltura (ad esempio azoto o fosforo) diventa limitante mentre la fonte di carbonio è presente in eccesso.
La limitazione di azoto è la condizione più efficiente per indurre la lipogenesi. Durante la fase di crescita cellulare, l’azoto è necessario per la sintesi di proteine e acidi nucleici mentre il flusso di carbonio è distribuito tra processi energetici e anabolici cedevoli carboidrati, lipidi, acidi nucleici e proteine. Quando l’azoto viene limitato, il tasso di crescita rallenta e la sintesi di proteine e acidi nucleici tende a cessare.
Nelle specie non oleaginose, l’eccesso di carbonio rimane inutilizzato o viene convertito in polisaccaridi di riserva, mentre, in specie oleaginose, esso è preferenzialmente incanalato verso la sintesi lipidica, provocando l’accumulo di trigliceridi all’interno di corpi lipidici intracellulari (Fig. 2).

Il percorso biochimico di biosintesi lipidica non è molto diverso tra organismi eucarioti e non differisce tra funghi oleaginosi e non oleaginosi (Fig. 3).
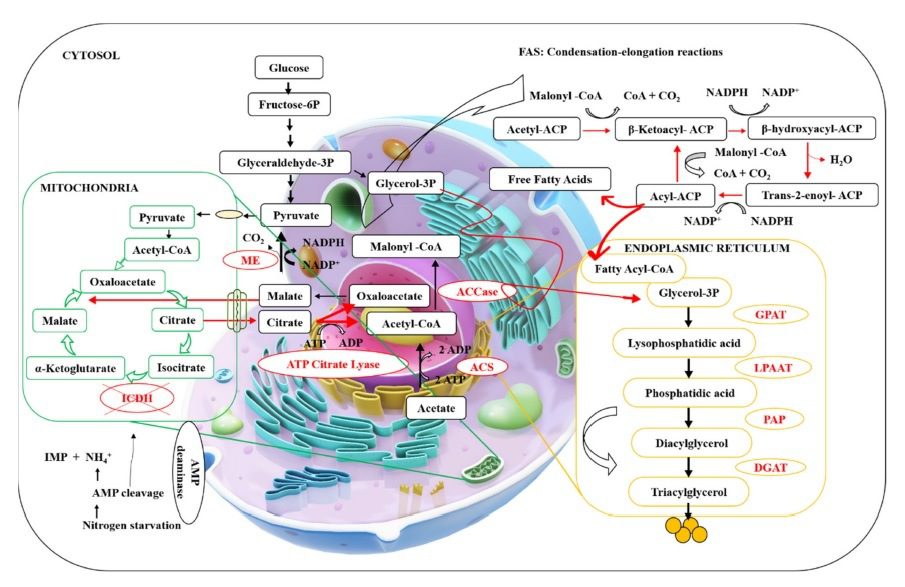
La capacità di accumulare grandi quantità di lipidi dipende soprattutto dalla regolazione, dalla via biosintetica e dalla fornitura di precursori, rappresentati da acetil-CoA, malonil-CoA e glicerolo-3-fosfato, e di NADPH come cofattore.
La maggior parte delle informazioni sono state ottenute dal lievito modello Saccharomyces cerevisiae, che non accumula lipidi, e dal lievito Yarrowia lipolytica, che rappresenta un organismo modello per la produzione di bio-olio ed è adatto per la manipolazione genetica.
In caso di necessità energetiche, i lipidi di riserva vengono mobilitati da questo comparto e catabolizzati ad opera di enzimi, quali triacileglicerolo lipasi e steril-estere idrolasi.
La necessità di substrati di scarto per la produzione di bio-olio
Ad oggi, la produzione di bio-oli microbici avviene esclusivamente su scala laboratorio e non esistono ancora impianti industriali in grado di assicurarne una produzione su scala commerciale.
Una delle motivazioni del parziale sviluppo di questo processo biotecnologico consiste nell’ancora mancato raggiungimento di una piena sostenibilità economica a causa della competizione rispetto agli oli tradizionali ottenuti da fonti vegetali ma soprattutto da fonti fossili.
Per questo motivo, al fine di rendere economicamente competitivi gli oli di origine microbica e favorirne una produzione su larga scala è necessario ridurne i costi di produzione attraverso l’utilizzo di materie prime, ossia fonti di carbonio, di scarto come i rifiuti agro-industriali.
Le molecole di scarto ottenibili da processi già presenti su scala industriale e utilizzabili come substrato per la fermentazione dei lieviti oleaginosi sono numerose. Tra di esse troviamo gli acidi organici volatili, come acido acetico, acido propionico e acido butirrico, il glicerolo grezzo, l’N-acetilglucosammina e gli zuccheri di seconda generazione ottenuti da biomasse (glucosio, xilosio, arabinosio) (Fig. 4).

Cutaneotrichosporon oleaginosus come biocatalizzatore per conversione di scarti in risorse
Gli acidi organici volatili rappresentano uno dei principali sottoprodotti dei processi industriali di digestione anaerobica. Il glicerolo grezzo è il principale sottoprodotto della produzione di biodiesel tradizionale, ottenuto mediante la reazione di trans-esterificazione dei trigliceridi estratti dalle piante oleaginose. L’N-acetilglucosammina è uno degli scarti derivanti dalla lavorazione dei crostacei in quanto tale molecola rappresenta l’unità di base della chitina, ossia il polimero che costituisce l’esoscheletro di insetti e artropodi.
Infine, gli zuccheri di seconda generazione sono ottenuti da biomasse lignocellulosiche di scarto derivanti da processi agro-industriali (es. lavorazione del cardo, della paglia, della pannocchia) dalla manutenzione del verde pubblico e delle colture edibili o dall’industria della carta (es. carta non riciclabile e acque reflue ricche di cellulosa).
Cutaneotrichosporon oleaginosus (Fig. 5) è una delle specie più studiate e più promettenti tra quelle appartenenti alla categoria dei lieviti oleaginosi. Nel corso degli ultimi quindici anni, la tassonomia di questa specie ha subito varie modifiche. Tale microrganismo è noto anche col nome di Apiotrichum curvatum, Cryptococcus curvatus, Trichosporon cutaneum e Trichosporon oleaginosus.
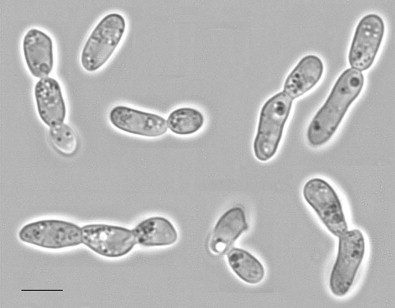
Tale microrganismo è in grado di accumulare bio-olio fino al 60% del proprio peso cellulare. Inoltre, esso è caratterizzato da una crescita rapida e da una buona resistenza agli inibitori della crescita (es. furfurale, 5-idrossimetilfurfurale, metanolo, siringaldeide, guaiacolo) presenti spesso nei rifiuti utilizzati come substrato di fermentazione.
Tuttavia, la sua abilità principale è quella di essere in grado di convertire tutte le molecole di scarto citate in precedenza in bio-olio di nuova generazione attraverso la lipogenesi.
Punti di debolezza del bio-olio e prospettive future
Sebbene la produzione di single cell oil sia un processo biotecnologico di grande interesse sia per la ricerca sia per l’industria, le sfide scientifiche e tecnologiche da affrontare, così come gli ostacoli da risolvere, sono ancora diverse.
La prima criticità legata alla conversione dei rifiuti in biodiesel, biosurfattanti, biopolimeri, mangimi, intermedi chimici, ecc. consiste nell’elevata complessità chimica dei substrati di scarto. La presenza di inibitori della crescita e/o di elevate concentrazioni di azoto e/o fosforo limita l’attività catalitica del C. oleaginosus causando, spesso, un drastico calo della produttività di olio e della resa di processo.
Una seconda importante criticità è legata ai metodi di estrazione del bio-olio dalle cellule di lievito. A differenza di molte molecole ottenute per via fermentativa su scala industriale, come ad esempio l’etanolo, l’acido lattico, l’acido citrico, i trigliceridi non vengono secreti nel mezzo di coltura ma vengono accumulati all’interno delle cellule, all’interno dei corpi lipidici.
Pertanto, il recupero dei lipidi richiede la lisi della membrana cellulare e dei corpi lipidici. Attualmente, il metodo più utilizzato su scala laboratorio prevede una lisi chimica mediante acido cloridrico in temperatura seguita dall’estrazione dell’olio mediante due solventi organici: cloroformio e metanolo.
Purtroppo, si tratta di reagenti estremamente tossici sia per l’uomo, sia per l’ambiente e gli animali. Metodi e solventi green alternativi sono stati identificati e testati ma spesso, purtroppo, presentano delle rese di estrazione più basse rispetto al metodo convenzionale non sostenibile.
Tutto ciò ha significative ripercussioni sulla sostenibilità economica e ambientale di questo innovativo modello di bioraffineria.
Per questi motivi, è necessario continuare a svolgere attività di ricerca e sviluppo per perfezionare questo processo e renderlo idoneo per lo scale-up, assicurando una produzione rispettosa della natura e delle generazioni future.
Nicola Di Fidio
Sitografia:
- Nicola Di Fidio (11 aprile 2018, Microbiologia Italia). Dalle raffinerie alle bioraffinerie grazie a batteri, lieviti e microalghe. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/dalle-raffinerie-alle-bioraffinerie-grazie-a-batteri-lieviti-e-microalghe/
- Nicola Di Fidio (10 settembre 2019, Microbiologia Italia). Biodiesel e β-carotenoidi di nuova generazione prodotti da glicerolo industriale di scarto per via biotecnologica. Estrapolato da: https://www.microbiologiaitalia.it/micologia/biodiesel-e-beta-carotenoidi-di-nuova-generazione-da-glicerolo-industriale-di-scarto/
- Nicola Di Fidio (11 agosto 2017, Microbiologia Italia). Biodiesel da scarti vegetali grazie ai lieviti oleaginosi. Estrapolato da: https://www.microbiologiaitalia.it/micologia/biodiesel-da-scarti-vegetali-grazie-ai-lieviti-oleaginosi/
- Nicola Di Fidio (25 marzo 2020, Microbiologia Italia). Carta non riciclabile in biocarburanti: un nuovo schema di bioraffineria ed economia circolare. Estrapolato da: https://www.microbiologiaitalia.it/micologia/carta-non-riciclabile-in-biocarburanti-un-nuovo-schema-di-bioraffineria-ed-economia-circolare/
- Nicola Di Fidio (13 gennaio 2021, Microbiologia Italia). Lipomyces starkeyi: una cell factory per la produzione di biodiesel di nuova generazione da canne giganti infestanti. Estrapolato da: https://www.microbiologiaitalia.it/micologia/lipomyces-starkeyi-una-cell-factory-per-la-produzione-di-biodiesel-di-nuova-generazione-da-canne-giganti-infestanti/
Bibliografia:
- Di Fidio, N., Liuzzi, F., Mastrolitti, S., Albergo, R., De Bari, I. (2019). Single cell oil production from undetoxified Arundo donax L. hydrolysate by Cutaneotrichosporon curvatus.
- Caporusso, A., Capece, A., De Bari, I. (2021). Oleaginous Yeasts as Cell Factories for the Sustainable Production of Microbial Lipids by the Valorization of Agri-Food Wastes. Fermentation, 7(2), 50.
- Annamalai, N., Sivakumar, N., Oleskowicz-Popiel, P. (2018). Enhanced production of microbial lipids from waste office paper by the oleaginous yeast Cryptococcus curvatus. Fuel, 217, 420-426.
- Ryu, B. G., Kim, J., Kim, K., Choi, Y. E., Han, J. I., Yang, J. W. (2013). High-cell-density cultivation of oleaginous yeast Cryptococcus curvatus for biodiesel production using organic waste from the brewery industry. Bioresource technology, 135, 357-364.
- Chatterjee, S., Mohan, S. V. (2018). Microbial lipid production by Cryptococcus curvatus from vegetable waste hydrolysate. Bioresource technology, 254, 284-289.
- Seo, Y. H., Lee, I., Jeon, S. H., Han, J. I. (2014). Efficient conversion from cheese whey to lipid using Cryptococcus curvatus. Biochemical engineering journal, 90, 149-153.
Crediti immagini:
- Immagine in evidenza e Fig. 4 – Nicola Di Fidio
- Fig. 1 – https://commons.wikimedia.org/wiki/File:Yarrowia_lipolytica_Wuerze_colonies_46.jpg
- Fig. 2 – Czabany, T., Athenstaedt, K., Daum, G. (2007). Synthesis, storage and degradation of neutral lipids in yeast. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids, 1771(3), 299-309.
- Fig. 3 – Caporusso, A., Capece, A., De Bari, I. (2021). Oleaginous Yeasts as Cell Factories for the Sustainable Production of Microbial Lipids by the Valorization of Agri-Food Wastes. Fermentation, 7(2), 50.
- Fig. 5 – https://www.sciencedirect.com/topics/immunology-and-microbiology/cryptococcus-curvatus