Definizione ed epidemiologia
La candidosi invasiva (IC) è un infezione sistemica da Candida e include la candidemia (“Candida bloodstream infection”), la candidosi disseminata con coinvolgimento di organi interni (“deep-seated candidiasis”), l’endocardite e la meningite da Candida. Negli USA la candidemia costituisce l’8-10% delle “bloodstrem infections“, in Europa il 2-3%. Circa il 30% delle candidemie si verifica in terapia intensiva. La gestione del paziente con candidosi invasiva è estremamente complessa anche perché nella maggior parte dei casi i pazienti sono soggetti fragili con molte comorbidità. La candidosi invasiva presenta una mortalità del 40-50%.
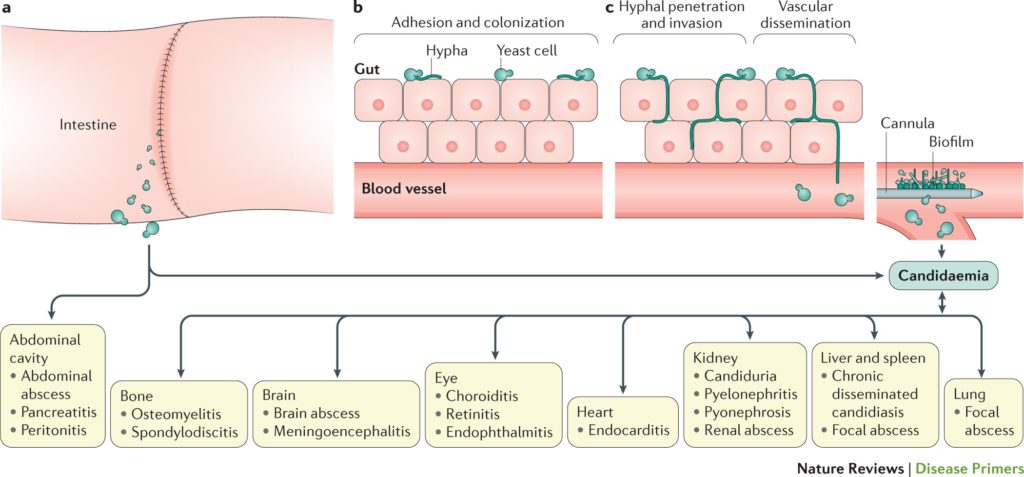
Di che candida parliamo?
La Candida è un fungo saprofita appartenente alla famiglia dei Saccaromiceti che fa parte del microbiota cutaneo, vaginale, oro-faringeo e intestinale. Si tratta di un patogeno opportunista in quanto determina malattia in caso di disregolazione dell’omeostasi immunitaria dell’ospite.
Al genere Candida appartengono numerose specie fungine ma circa il 90% delle Candidosi invasive è determinato da 5 specie: Candida albicans, C. glabrata, C. krusei, C. tropicalis, C. parapsilosis.
L’aumento delle candidosi invasive da “specie non albicans” probabilmente è dovuto al crescente uso di antifungini azolici verso cui le “specie non albicans” sono resistenti. C. parapsilosis è più frequente in Sud Europa, Australia e America Latina mentre C. glabrata è più frequente nella popolazione anziana.
I fattori di rischio per lo sviluppo della candidosi invasiva sono i seguenti:
• Lungodegenza
• Diabete mellito
• Insufficienza renale
• Emodialisi
• Chirurgia addominale
• Antibioticoterapia ad ampio spettro
• Immunosoppressori
• Chemioterapia
• Trapianto di organo solido o di midollo
• Catetere venoso centrale
• Nutrizione parenterale
• Colonizzazione multifocale mucocutanea
• Hematologic malignancy
Diagnosi: coltura e test non colturali
In caso di Candidosi invasiva la presentazione clinica è molto varia e il quadro sintomatologico dell’infezione sistemica può andare dalla febbre fino alla sepsi e allo shock settico. Le metodiche diagnostiche di laboratorio comprendono i test colturali e test non colturali.
L’emocoltura, da vena periferica o da vaso centrale se presente CVC, rimane il gold standard per la diagnosi di IC, è un test ad alta specificità ma non ad alta sensibilità in quanto risulta positiva solo nel 40% dei pazienti in cui la candidemia è associata a candidosi di organi interni e risulta negativa se si verifica candidosi di organi interni senza candidemia (in quest’ ultimo caso bisognerebbe fare la coltura di una biopsia del parenchima contaminato). Inoltre l’emocoltura richiede almeno due giorni per poter dare un risultato e questo è un limite importante perché non permette di poter impostare una terapia antifungina specifica precoce.
Insieme all’emocoltura è possibile effettuare test non colturali che hanno il vantaggio di essere più rapidi. I test non colturali più utilizzati sono il dosaggio del mannano e dell’ 1,3 β-D-glucano (BDG), l’ IgG test per mannano e antimannano, la PCR e il “T2 Candida panel”. In questo articolo ci soffermiamo sul test del BDG e sul “T2 Candida panel”, test diversi ma attualmente molto usati.
Il BDG è un antigene della parete cellulare di Candida e di moltissimi altri funghi fatta eccezione per Cryptococcus, Blastomyces e Mucorales dunque il test del BDG non può distinguere le diverse specie di Candida e non può distinguere le varie specie di Candida dagli altri funghi. Il problema del test del BDG sono i falsi positivi (bassa specificità del test) in quanto l’emodialisi e l’emofiltrazione, l’uso di derivati del sangue, la nutrizione enterale, alcuni β-lattamici e alcuni Gram+ possono alterare il risultato del test. Il dosaggio del BDG è particolarmente utile, insieme alla PCR, in caso di candidosi invasiva senza candidemia.
Il “T2 Candida panel” è una metodica mista di biologia molecolare risonanza magnetica in grado di identificare materiale genetico della Candida ma solo delle 5 specie sopra elencate (Candida albicans, C. glabrata, C. krusei, C. tropicalis, C. parapsilosis). Il risultato è riportato come positivo o negativo per la ricerca di C. albicans/C. tropicalis, di C. glabrata/C. krusei e di C. parapsilosis quindi questo test non distingue C. albicans da C. tropicalis e non distingue C. glabrata da C. krusei. Il tempo di attesa per il referto di un T2 è di 4,4 ± 1 h, dunque in meno di 5 ore si ha sicuramente un risultato positivo o negativo e questa rapidità diagnostica è importante soprattutto nei pazienti critici per i quali è necessario impostare una terapia fungina ottimale quanto prima. E’ ancora da approfondire l’utilità del T2 nei pazienti in cui sussiste un forte sospetto di candidosi invasiva con emocoltura negativa.
Le informazioni riportate nell’articolo in oggetto hanno esclusivamente scopo divulgativo, in nessun caso possono costituire la formulazione di una diagnosi o di una terapia.
Dr Riccardo Maria Botta, medico-chirurgo, specializzando in Anestesia, Rianimazione, Terapia Intensiva e del dolore
Bibliografia
- De Rosa FG, Garazzino S, Pasero D, Di Perri G, Ranieri VM. Invasive candidiasis and candidemia: new guidelines. Minerva Anestesiol. 2009 Jul-Aug;
- Calandra T, Roberts JA, Antonelli M, Bassetti M, Vincent JL. Diagnosis and management of invasive candidiasis in the ICU: an updated approach to an old enemy. Crit Care. 2016
- Clancy CJ, Nguyen MH. Diagnosing Invasive Candidiasis. J Clin Microbiol. 2018 Apr 25;56(5)
- Arendrup MC, Andersen JS, Holten MK, Krarup KB, Reiter N, Schierbeck J, Helleberg M. Diagnostic Performance of T2Candida Among ICU Patients With Risk Factors for Invasive Candidiasis. Open Forum Infect Dis. 2019 Mar
Complimenti al Dottore
La candidosi può causare anche fastidi agli occhi, fotosensibilità, puntini luminosi, ansia, tachicardia?
Ciao vorrei fare l’esame T2 candida panel ma l’infermiera del mio dottore non trova il codice per fare l’impegnativa. Come posso saperlo io???