I microrganismi possono avere un impatto devastante sull’ambiente. La loro introduzione in un ambiente favorevole in cui è presente un ospite suscettibile può comportare gravi conseguenze come la modifica del paesaggio, perdita di biodiversità e, nei casi peggiori, l’estinzione di una specie. L’epidemia di Cryphonectria parasitica, agente causale del cancro corticale del castagno, ha colpito i castagneti d’America e d’Europa e ha fatto di questo patogeno un esempio da manuale del severo impatto che può avere una patologia sulle foreste di un continente.
Caratteristiche
Cryphonectria parasitica è un fungo Ascomycota appartenente all’ordine delle Diaporthales. È un organismo omotallico sebbene la formazione dei periteci sia in massima parte dovuta all’incrocio di ceppi con polarità sessuale opposta. È l’agente del cancro corticale del castagno. Cryphonectria parasitica mostra una temperatura ottimale di crescita intorno ai 27 °C pur mantenendo una buona capacità di sviluppo tra i 15 e i 32 °C.
Filogenesi
| Dominio | Eukaryota |
|---|---|
| Regno | Fungi |
| Divisione | Ascomycota |
| Classe | Sordariomycetes |
| Ordine | Diaporthales |
| Famiglia | Cryphonectriaceae |
| Genere | Cryphonectria |
| Specie | Cryphonectria parasitica |
Il cancro corticale del castagno
Il cancro corticale del castagno è una malattia causata dal fungo Cryphonectria parasitica, che agli inizi del XX secolo ha colpito i boschi di castagno europei e americani. Il patogeno è nativo dell’Asia orientale e si è diffuso negli altri continenti tramite il commercio di piante di castagno infette.
In america
Viene segnalata per la prima volta in America nel 1904 nel giardino zoologico della città di New York, dove ha avuto gravi conseguenze colpendo i grandi popolamenti di castagno americano (Castanea dentata) su tutto il loro areale causandone quasi la scomparsa in pochi decenni e riducendone drasticamente la diffusione.
In europa
In Europa invece viene segnalato per la prima volta nel 1938 nei pressi di Genova e in un arco di tempo di circa 50 anni si diffonde coprendo tutto l’areale europeo del castagno (C. sativa). Ciò ha comportato un progressivo abbandono della castanicoltura europea nei decenni successivi alla seconda guerra mondiale. Tuttavia, gli esiti nel vecchio continente sono stati meno drammatici grazie alla maggiore resistenza dei castagni europei all’infezione e grazie all’avvento del fenomeno dell’ipovirulenza, una importante possibilità di controllo biologico che ha ridotto l’impatto del patogeno e ha salvato il castagno europeo dall’estinzione.

Patogenesi
Cryphonectria parasitica è un agente patogeno che colpisce le porzioni ipogee della pianta colonizzando i tessuti della corteccia i cui sintomi, la loro manifestazione e la loro entità, dipendono dalla suscettibilità, dall’età e dalla porzione della pianta colpita. Le infezioni producono lesioni necrotiche sulla corteccia che possono portare alla morte alcune parti della pianta come rami e ramoscelli, oppure, nei casi peggiori, l’intero fusto o la pianta intera.
I sintomi appaiono differenti a seconda della porzione che il fungo riesce a colonizzare. Sui tessuti corticali più giovani che presentano un aspetto liscio i cancri si presentano colorati con una pigmentazione arancione o bruno-rossastra, mentre sui tessuti vecchi la colorazione è meno pronunciata. Fusti e rami più spessi manifestano cancri permanenti che sussistono per anni prima di portare alla morte della pianta. Anche lo spessore della corteccia condiziona l’aspetto dei segni e dei sintomi osservabili. Se la corteccia è spessa può nascondere i cancri che rimarranno invisibili fintanto che su questa non si formeranno le lesioni necrotiche. Può assumere invece un aspetto affossato quando il cambio sottostante viene completamente ucciso.
Nei casi in cui il cancro corticale ricopre tutta la circonferenza del fusto significa che la malattia è ad uno stato avanzato e nella maggior parte dei casi la pianta è morta. Un altro tipo di sintomo manifestato dalle piante adulte che permette di individuare precocemente la malattia, consiste nella presenza di foglie a bandiera, ovvero le foglie secche che rimangono attaccate alla pianta. Infine, un altro sintomo osservabile, consiste in una reazione che le piante hanno a seguito dell’infezione, ovvero l’emissione di numerosi getti epicormici in prossimità dei cancri.
Ospiti colpiti
I principali ospiti appartengono alla famiglia delle Fagaceae, genere Castanea, e sono le specie di castagno americano (Castanea dentata) e castagno europeo (Castanea sativa), tra i quali il primo risulta il più suscettibile. Vengono colpiti anche il castagno giapponese (C. japonica) e il castagno cinese (C. mollissima) che, data la coesistenza con il patogeno, il quale è infatti proveniente dall’Asia, risultano essere più resistenti alla malattia. Possono essere colpite anche specie appartenenti alla famiglia delle Fagaceae come quelle del genere Quercus. Vengono colpiti occasionalmente anche specie del genere Acer e la specie Carpinus betulus. Tuttavia le infezioni al di fuori degli ospiti appartenenti al genere Castanea si manifestano solo nel caso in cui le piante colpite abbiano manifestato particolari condizioni di sofferenza dovuta ad altri fattori (stress abiotici, biotici, senescenza).

Ciclo vitale e riproduzione
Cryphonectria parasitica è un organismo necrotrofo che necessita di ferite fresche o fessurazioni della corteccia per invadere i tessuti dell’ospite le quali possono formarsi per cause naturali o artificiali. È inoltre in grado di causare le infezioni entrando nei tessuti tramite le galle causate dal cinipide del castagno (Dryocosmus kuriphilus). Le infezioni possono essere causate da entrambe le forme del fungo, asessuata e sessuata.
Il ciclo infettivo parte dalla germinazione delle spore che, depositandosi su una ferita nella corteccia della pianta e sviluppandosi, provocano delle lesioni necrotiche le quali successivamente prenderanno la forma di cancro corticale. Entrambi i corpi fruttiferi del fungo, sessuati (periteci) e asessuati (picnidi), possono coesistere sulla stessa porzione di corteccia contemporaneamente e generalmente necessitano di un elevato tasso di umidità atmosferica per poter sporulare.
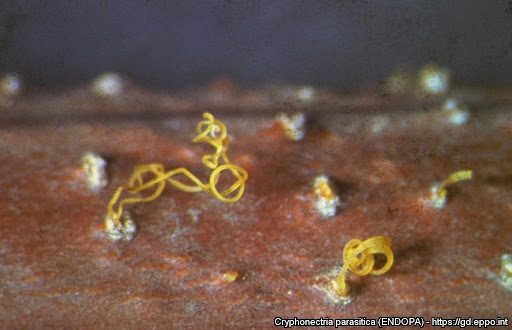
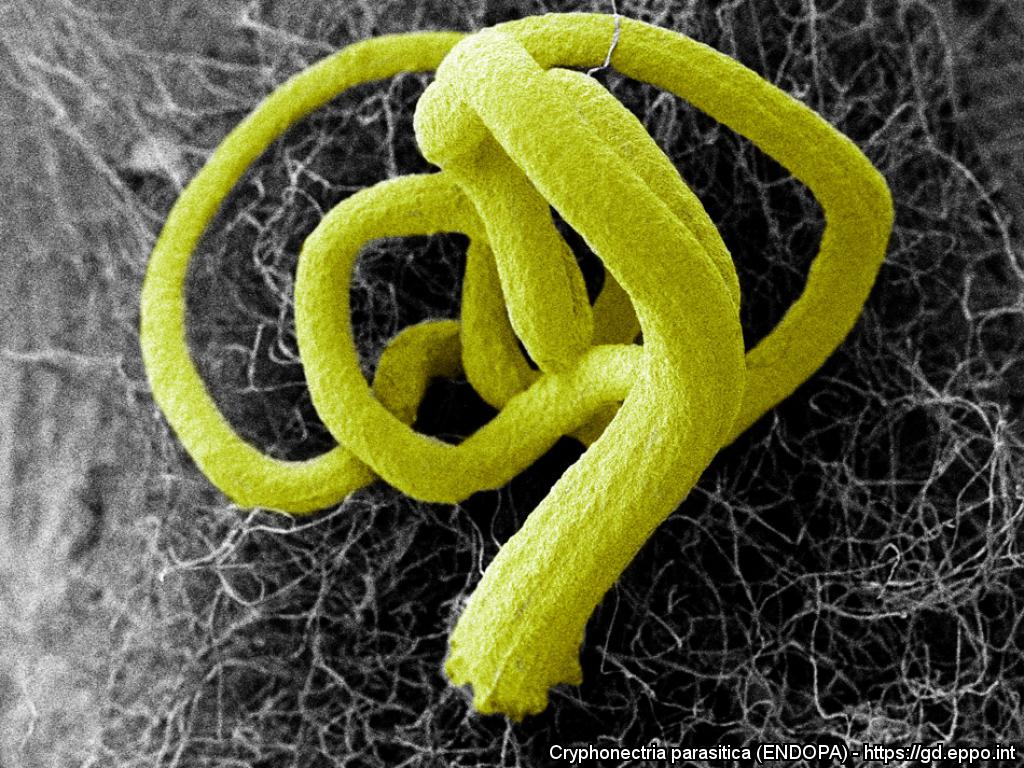
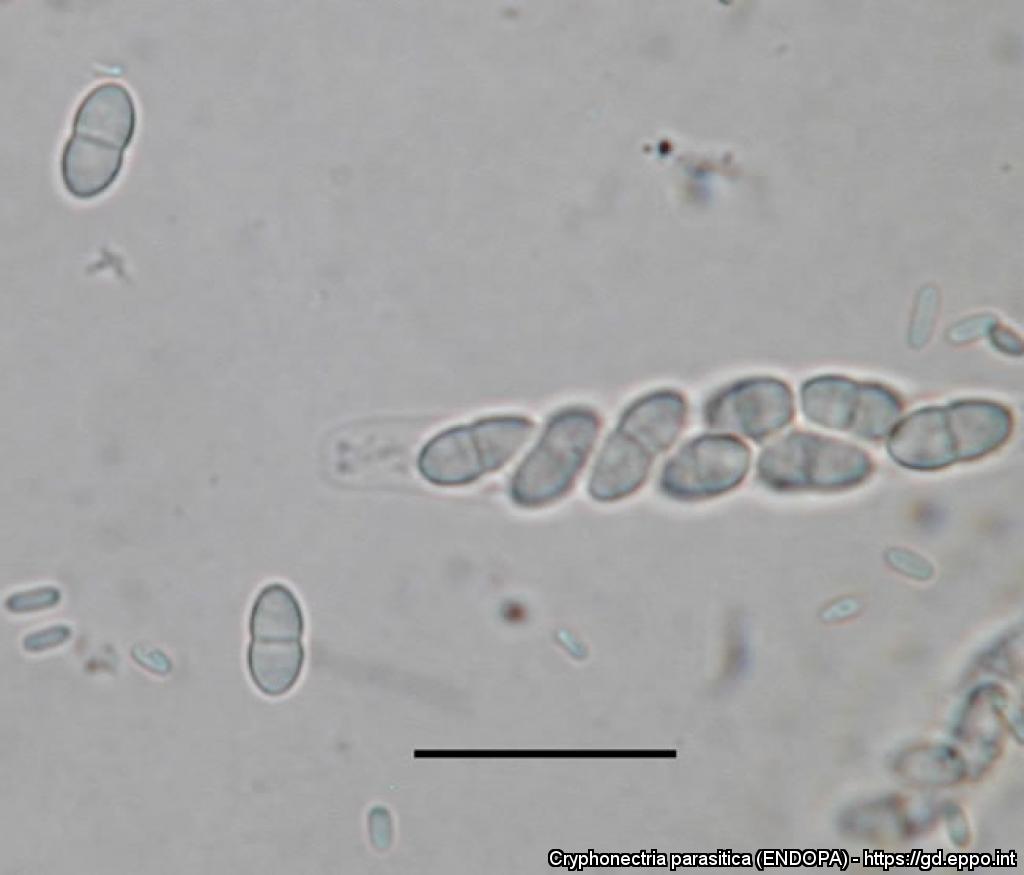
Sono visibili sulla corteccia sotto forma di pustole colorate giallo-arancioni o rosso-brune, alte 2.5 mm, aventi diametro variabile 0.5-4 mm, composte da tessuto stromatico che rimane all’interno dei tessuti corticali, eccezione fatta per le pustole che fuoriescono. I picnidi hanno la forma di una cavità irregolare nel tessuto stromatico e rilasciano i conidi in una struttura spiraliforme di colore giallo. Questi sono appiccicosi, asettati, ialini, aventi forma che può variare da bacilliforme a ellissoidale e occasionalmente ricurva. La loro dispersione su breve distanza può avvenire tramite gocce d’acqua piovana o tramite l’acqua che scorre sul fusto della pianta, mentre vento, insetti e uccelli, sono in grado di permettere ai conidi di coprire distanze più lunghe. I periteci hanno forma globosa a fiasco, caratterizzati da un lungo collo cilindrico (300–600 µm in lunghezza e 200 µm di diametro) terminante con un ostiolo. Le ascospore sono ellissoidali, bicellulari, lisce, racchiuse in aschi e disposte entro questi in file 2 per 4, e vengono espulse nell’aria riuscendo a diffondersi per poche centinaia di metri.
In Cryphonectria parasitica l’accoppiamento è controllato da un locus che condiziona la compatibilità vegetativa tra due individui tramite l’allele MAT-1 o MAT-2. Le indagini di popolazione hanno dimostrato che C. parasitica ha un sistema di accoppiamento misto, che comporta il manifestarsi di fenomeni di outcrossing e auto-fecondazione. La maggior parte degli isolati autofertili per il tipo di accoppiamento sono eterocariotici, e si formano attraverso fenomeni quali la consanguineità biparentale o la ricombinazione parassessuale, che coinvolgono il crossing over mitotico.
Epidemiologia
Nuove popolazioni di Cryphonectria parasitica possono stabilirsi con uno o più genotipi in un ambiente favorevole, attraverso introduzione accidentale o tramite la diffusione delle spore. Su questi processi giocano un ruolo chiave i fattori ambientali che, se risultano favorevoli per il fungo, possono avere un forte impatto sulle piante colpite. Le temperature influenzano la crescita e quelle ottimali sono pari a 20 °C per le popolazioni americane e 27 °C per quelle europee. L’umidità atmosferica influenza la sporulazione, che infatti avviene soltanto in condizioni di umidità elevata. Altro fattore importante è la condizione di salute delle piante che, in condizioni di sofferenza dovuta a fattori biotici o abiotici, possono renderle più suscettibili alle infezioni. Infine è determinante l’età delle ferite, poiché le spore riescono solo a colonizzare i tessuti se le ferite sono fresche, di uno-due giorni.
Lotta e controllo
Per prevenire il rischio di introduzione sono state stabilite in tutto il mondo norme di quarantena che regolamentano il commercio di materiali vegetali che possono essere vettori del patogeno (semi, legname, corteccia, piante vive). In Europa, l’EPPO (European and Mediterranean Plant Protection Organization) ha inserito C. parasitica nella lista A2, dove vengono inclusi patogeni presenti nel territorio euro-mediterraneo. Le piante di castagno e di quercia per la piantumazione necessitano di un passaporto speciale per essere commercializzate da un paese ad un altro, in modo da certificare che le piante in questione provengono da aree in cui C. parasitica non è presente e, che in prossimità del luogo di produzione e confezionamento delle piante, non è stata rilevata presenza della malattia dall’inizio dell’ultima stagione vegetativa.
Nelle zone focolaio sono state spesso intrapresi sforzi per l’eradicazione tramite tagli e combustione delle piante colpite che tuttavia non hanno portato effetti positivi, dato che è molto difficile individuare tutte le piante colpite in un popolamento.
Sulle singole piante è buona norma evitare tagli e spaccature della corteccia. Qualora questi non siano evitabili è indicato effettuarli al di fuori del periodo di sporulazione del fungo.
La lotta chimica con l’utilizzo di fungicidi è proibita in molti paesi ed è comunque sconsigliata in bosco, poiché queste sostanze andrebbero a colpire anche la microflora del suolo e, inoltre, C. parasitica potrebbe sviluppare una forma di resistenza al trattamento. La strategia più efficace rimane la lotta biologica tramite l’ipovirulenza indotta.
Lotta biologica: ipovirulenza indotta
Un aspetto molto importante è dato dalla possibilità di lotta biologica tramite l’induzione dell’ipovirulenza a seguito di infezioni di micovirus Cryphonectria hypovirus che colpiscono C. parasitica, fenomeno che è stato osservato per la prima volta in Italia negli anni ‘50. Si tratta di virus a RNA a filamento positivo, appartenente alla famiglia Hypoviridae, localizzati nel citoplasma dell’ospite fungino, la cui infezione inibisce nel fungo la possibilità di infettare le piante ospite, la crescita e la sporulazione. Il genere Hypovirus comprende attualmente quattro specie che sono state ben caratterizzate, chiamate Cryphonectria hypovirus (CHV-1, CHV-2, CHV-3, CHV-4). La trasmissione del virus può avvenire orizzontalmente da un fungo ad un altro tramite la formazione di anastomosi ifali tra due individui compatibili o verticalmente tramite la diffusione dei conidi infetti che, a seguito del loro sviluppo, formeranno anastomosi ifali con individui compatibili.
C. parasitica è inoltre ospite di altri micovirus che sono in grado di attenuarne la virulenza appartenenti alla famiglia Reoviridae e alla famiglia Narnaviridae
Si ringrazia Edoardo Scali per la gentile concessione dell’articolo
Fonti:
- Rigling, D., & Prospero, S. (2018). Cryphonectria parasitica, the causal agent of chestnut blight: Invasion history, population biology and disease control. Molecular Plant Pathology, 19(1), 7–20. https://doi.org/10.1111/mpp.12542
- https://gd.eppo.int/taxon/ENDOPA
bellissimo