Obiettivo della tecnica
La colorazione in negativo è indicata quando sia necessario osservare microrganismi che non si colorano facilmente, oppure nei casi in cui la colorazione potrebbe alterare la morfologia degli stessi (specialmente laddove la morfologia non sia ancora del tutto nota con certezza).
In questa metodica il colorante utilizzato, diversamente da quanto avviene nelle altre colorazioni non è trattenuto dalle cellule batteriche (o fungine) ma si dispone attorno ad esse, creando uno sfondo monocromatico su cui spiccano (chiari e ben visibili) i microrganismi.
Questo permette di osservare i microrganismi nella loro forma reale e ne preserva inoltre la piena vitalità, sia perchè la maggior parte dei coloranti utilizzati in Microscopia risultano tossici per gli stessi, sia perchè non necessita della preliminare fissazione al calore del campione.
La colorazione in negativo inoltre non presenta il rischio di creazione accidentale di forme artefatte (per eventuali reazioni anomale tra colorante e strutture cellulari).
Data la sua estrema versatilità, è utilizzata sia per identificare i batteri (tanto gram negativi quanto gram positivi), sia per l’identificazione di capsule di spore fungine: in quest’ultimo caso, vi si ricorre in clinica in modo specifico nelle diagnosi d’infezioni dovute a Cryptococcus neoformans, un fungo patogeno opportunista ed ubiquitario agente eziologico della Criptococcosi.
Vi si può ricorrere anche per lo studio della morfologia e l’identificazione di spirochete, protozoi e funghi in generale, per la diagnosi dei quali tuttavia in ambito clinico si preferisce la colorazione di Wright Giemsa (per approfondire al riguardo, si rinvia al nostro articolo)
La colorazione in negativo trova infine impiego nell’analisi ambientale (per la valutazione della presenza microbica nelle acque inquinate) e nei laboratori dove si producono colture cellulari (per la stima qualitativa del grado di sviluppo e di vitalità delle stesse).
Che cos’è e come funziona
Le tecniche di colorazione in negativo non mirano a colorare i microrganismi ma l’ambiente acquoso intorno ad essi, permettendo cosi’ di visualizzarli per contrasto su uno sfondo monocromatico.
Utilizzano a tal fine un unico colorante, sempre di natura acida e generalmente idrosolubile, che a causa della sua carica ionica negativa è respinto per interazione elettrostatica dalle cellule batteriche (anch’esse cariche negativamente in superficie), finendo per precipitare intorno ad esse.
La maggior parte dei protocolli attualmente in uso considerano ugualmente validi l’utilizzo della Nigrosina, dell’Eosina oppure del Nero China.
In questo articolo assumeremo come riferimento la Nigrosina, essendo il colorante sfruttato nelle analisi cliniche ed ambientali.
La Nigrosina inoltre ha un importante vantaggio: permette infatti di valutare con maggior precisione la vitalità dei microrganismi presenti nel campione d’indagine, dal momento che non penetra nelle cellule vitali ma può penetrare invece in quelle morte.
Questo colorante è in realtà costituito da una miscela di coloranti neri sintetici a base di anilina, anilina cloridrata e nitrobenzene, che vengono trattati in modo da ottenere alla fine un composto solubile in acqua.
(Nel protocollo che segue, viene utilizzato il microscopio con obiettivo ad immersione, che garantisce la miglior risoluzione per questo tipo specifico di colorazione; laddove esso non sia disponibile, si può comunque utilizzare ugualmente qualunque microscopio)
Materiale occorrente
- Vetrino per microscopia;
- Ago da microbiologia (oppure un’ansa per semina batterica);
- Nigrosina (con contagocce);
- Vetrino coprioggetti;
- Olio per immersione;
- Microscopio con obiettivo ad immersione.
Procedimento
- Strisciare sul vetrino il campione da analizzare;
- Aggiungere una goccia di Nigrosina e mescolare subito il campione e colorante per mezzo dell’ago (o dell’ansa), fino ad ottenere uno strato sottile ed uniforme tale da consentire il passaggio della luce;
- Far asciugare il vetrino per bene all’aria;
- Porre il vetrino coprioggetti sul campione;
- Posizionare una goccia di olio per immersione sopra la zona da osservare.
Il vetrino cosi’ trattato (Fig.1) è ora pronto per l’analisi al microscopio.

Osservazione del vetrino
Si consiglia d’iniziare l’osservazione con un ingrandimento 40X, aumentandolo poi gradualmente sino al 100X.
I microrganismi presenti nel campione appariranno incolori o bianchi, su uno sfondo monocromatico assicurato dal colorante (Fig.2).
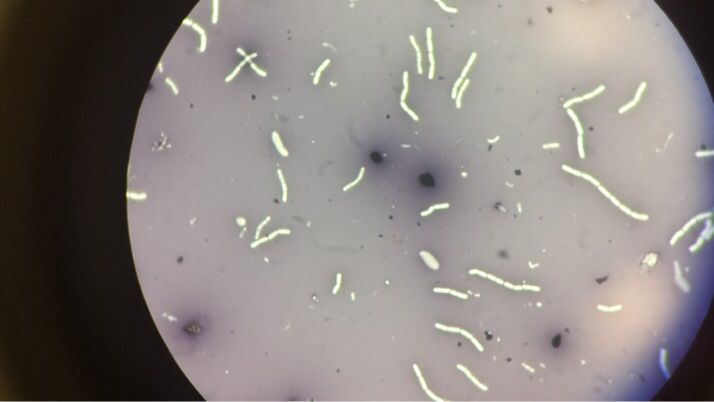
La loro morfologia sarà ben riconoscibile e ciò ne permetterà lo studio e l’identificazione (Fig.3 e Fig.4).


Fonti
Bibliografia di riferimento
- Green FJ (1990) The Sigma-Aldrich Handbook of Dyes, Stains and Indicators, pp.513-515.
Sitografia di riferimento
Per approfondire sulla natura chimica della Nigrosina:
Crediti per le immagini
Immagine in evidenza:
Figura 1:
Figura 2:
Figura 3:
Figura 4: