Caratteristiche
Il parassita di cui parliamo oggi può causare deformità fisiche molto debilitanti e affligge l’umanità da tempi immemori. Infatti la sua presenza si può intuire dai caratteristici rigonfiamenti degli arti nella statua del faraone Mentuhotep II (2055–2004 a.C.).
Wuchereria bancrofti è un nematode parassita presente nelle aree tropicali e sub-tropicali di Africa, Asia, Oceania e Americhe (inclusa Haiti), ed è responsabile del 90% dei casi di filariosi linfatica (filariosi bancroftiana). Invece la filariosi brugiana, endemica di alcune aree del sud e sud-est asiatico, è causata dalle specie Brugia malayi e Brugia timori. Tuttavia, la biologia e il ciclo vitale di questi tre parassiti sono comparabili.
Filogenesi
| Dominio | Eukaryota |
| Regno | Animalia |
| Phylum | Nematoda |
| Classe | Secernentea |
| Ordine | Spirurida |
| Famiglia | Onchodercidae |
| Genere | Wuchereria |
| Specie | W. bancrofti |
Ciclo vitale
Il parassita necessita di una zanzara per la trasmissione. Infatti, diverse specie appartenenti ai generi Anopheles, Aedes, Culex e Mansonia fungono da vettori in diverse parti del mondo. Infatti, quando la zanzara punge le larve infettive emergono dalla sua proboscide penetrando nella ferita della puntura. Successivamente, i parassiti maturano nel circolo sanguigno e una volta adulti raggiungono il sistema linfatico. Dopo l’accoppiamento, la femmina inizia a produrre le larve (microfilarie) che migrano nel circolo periferico. Successivamente, le microfilarie vengono ingerite dal vettore con il sangue. Il parassita penetra poi la parete dello stomaco e attraversa tre stadi di sviluppo nel torace dell’insetto. Infine, le larve infettive migrano nella testa e nella proboscide della zanzara e rimangono in attesa del prossimo ospite.

Morfologia strutturale
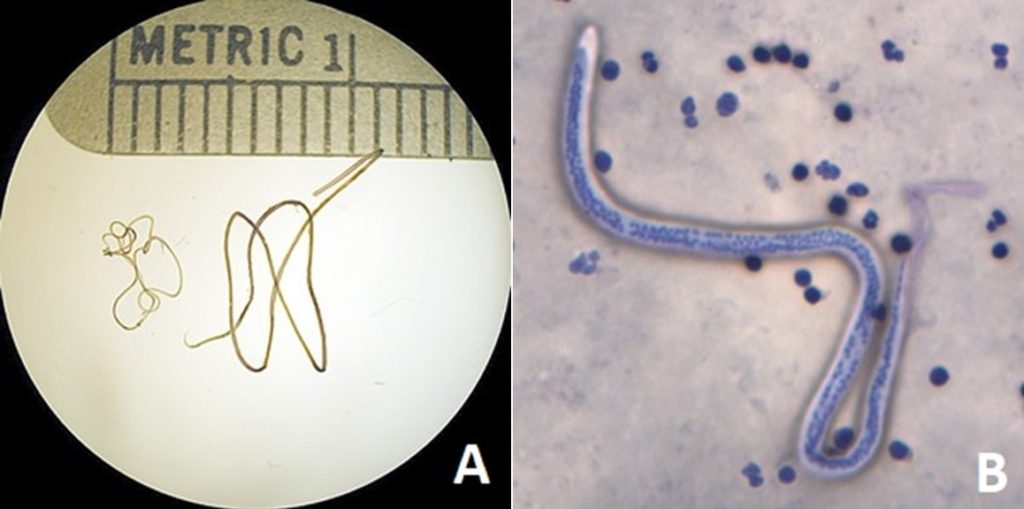
I vermi adulti sono filiformi e biancastri, con i maschi lunghi circa la metà (4 cm) delle femmine (10 cm), mentre le microfilarie misurano 240-300 μm. Gli stadi larvali nella zanzara variano per morfologia e lunghezza: le larve L1, tozze e simili a salsicciotti, misurano circa 100 μm mentre le larve infettive L3 sono più affusolate e raggiungono il millimetro.

Patogenesi
La patologia è causata dalla presenza dei vermi nei vasi linfatici e può essere molto debilitante. Le manifestazioni acute (con febbre e infiammazione dei linfonodi) possono precedere la malattia cronica, che di solito si manifesta dopo anni. Essa è causata dall’interruzione del normale flusso della linfa, il cui accumulo porta a linfedema tipicamente negli arti inferiori (ma che può interessare anche braccia, seno o scroto). Inoltre, questo ingrossamento degli arti inferiori può essere molto pronunciato e associato a un indurimento e ispessimento della cute. Per questo motivo la condizione è conosciuta anche come elefantiasi. Raramente, e solo in alcune aree dell’Asia, si osserva la cosiddetta eosinofilia polmonare tropicale: questa sindrome è accompagnata da un marcato aumento degli eosinofili nel sangue, broncospasmo, infiltrati polmonari e febbricola, ed è probabilmente dovuta a ipersensibilità alle microfilarie.

Metodi di identificazione
La diagnosi avviene soprattutto visualizzando al microscopio le microfilarie nel sangue periferico in un vetrino a goccia spessa, colorato con il metodo di Giemsa o con ematossilina ed eosina. Tuttavia, il campione va prelevato di notte quando le microfilarie sono presenti nel sangue periferico (ad eccezione delle isole del Pacifico, dove sono presenti di giorno). Inoltre, il sangue può essere filtrato e concentrato per aumentare la sensibilità del test. Esistono anche test immunoenzimatici (sierologici) per gli anticorpi IgG anti-filaria (in particolare IgG4, i cui livelli sono più elevati in infezioni attive) e un test immunocromatografico per l’antigene dei vermi adulti. In aggiunta, l’ecografia può risultare d’aiuto nel visualizzare i parassiti nei vasi linfatici.
Terapia
La dietilcarbamazina (DEC) (6 mg/kg/die) uccide efficacemente sia gli adulti che le microfilarie. Tuttavia, a causa di reazioni avverse associate alla co-infezione con altre due filarie (Onchocerca volvulus e Loa loa), in questi casi si devono usare farmaci alternativi. Per esempio l’uso di ivermectina (IVM) (200 μg/kg) con albendazolo (400 mg) per ridurre i livelli di microfilarie, oppure la doxiciclina (100 mg) per uccidere gli adulti (che muoiono a causa dell’azione dell’antibiotico sui batteri endosimbionti Wolbachia). Invece, la cute delle aree interessate da linfedema cronico va pulita meticolosamente per evitare infezioni secondarie. In aggiunta, interventi chirurgici possono essere necessari nei casi più gravi.
Prevenzione ed eliminazione
Misure efficaci includono l’uso di zanzariere e il controllo delle popolazioni dei vettori tramite insetticidi. Inoltre, l’Organizzazione Mondiale della Sanità ha lanciato a partire dal 2000 il programma globale per l’eliminazione della filariosi linfatica (GPELF). Questa iniziativa è stata incentrata sulla somministrazione in massa di microfilaricidi (IVM o DEC) alle popolazioni a rischio. L’approccio ha ridotto la prevalenza del parassita e portato alla sua eliminazione come problema di salute pubblica in diversi paesi.
Fonti
- CDC
- DPDX
- OMS
- MSD
- Erickson SM, Xi Z, Mayhew GF, Ramirez JL, Aliota MT, Christensen BM, et al. (2009) Mosquito Infection Responses to Developing Filarial Worms. PLoS Negl Trop Dis 3(10): e529. DOI: 10.1371/journal.pntd.0000529.