Caratteristiche generali
La cromatografica liquida è una tecnica di separazione fisica in cui una sostanza viene divisa nei suoi componenti costitutivi: la fase stazionaria (particelle porose impaccate nella colonna) e la fase mobile (o eluente, cioè il liquido che scorre tra le particelle). La separazione cromatografica può avere diversi obbiettivi. HPLC (Fig. 1) è l’acronimo di High Performance Liquid Chromatography (cromatografia liquida ad alta prestazione) dove, per alta prestazione, si intende che le particelle della fase stazionaria sono molto piccole: minore è il diametro delle particelle che costituiscono la fase stazionaria, minore è l’ampiezza delle bande di soluto e, quindi, l’ampiezza dei picchi nel cromatogramma. Questo strumento lavora ad alte pressioni per spingere la fase mobile all’interno della colonna (circa 400-4000 psi).
La cromatografia liquida ad alta prestazione vede il suo sviluppo negli anni Sessanta del secolo scorso e il suo impiego commerciale ha portato allo sviluppo di questa tecnica in vari ambiti, diventando indispensabile nell’industria farmaceutica e non solo. Oggi l’HPLC è in continuo sviluppo e miglioramento per aumentare la velocità, sensibilità ed efficienza dell’analisi. L’analisi fatta più frequente è quella quantitativa ovvero, si misura l’area sottesa da un picco sul cromatogramma in quanto proporzionale alla concentrazione della sostanza in esame (calcolata grazie alla curva di calibrazione). Per di più l’analisi può essere fatta anche per isolare piccoli volumi di materiale (separazione preparativa) o per l’identificazione di un componente (analisi qualitativa).

Componenti dell’HPLC
L’HPLC (Fig. 2) è uno strumento complesso e costituito da varie componenti. Di seguito verranno brevemente descritte le diverse parti che lo compongono.
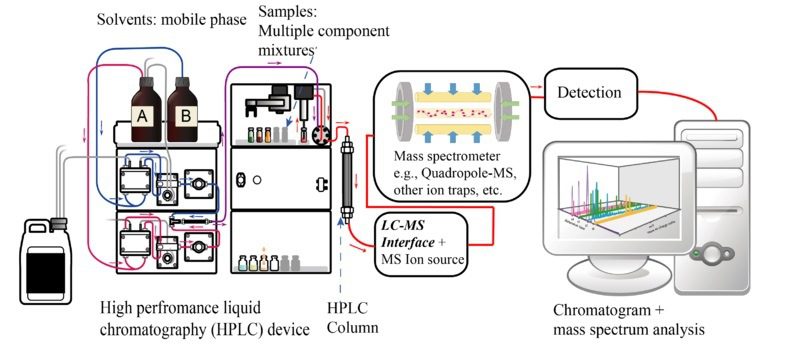
- Sistema di filtraggio del campione: componente molto importante. Il campione deve essere molto pulito per evitare che possibili granelli di materiale entrino nella colonna, compromettendo le analisi.
- Sistema degassaggio eluente: si utilizza un sistema a vuoto oppure facendo flussare un gas inerte nel liquido; questo processo è importante in quanto delle bolle potrebbero raggiungere il circuito del cromatografo e bloccare il flusso dell’eluente, oltre a creare problemi a pompe e rilevatori.
- Valvola d’iniezione: i campioni sono introdotti nel sistema tramite un iniettore costituito da una valvola e una siringa. Il metodo più utilizzato rimane il sampling loop che permette un’alta riproducibilità dei volumi che vengono iniettati. Spesso la valvola fa parte di un campionatore automatico, il quale preleva da ogni fiala i volumi di campione da iniettare.
- Pompa (con controllore): possono essere pompe per HPLC preparativa (peristaltiche) o pompe per HPLC analitica (alternative). Quest’ultime sono costituite da un misuratore di pressione e un sistema di eliminazione delle pulsazioni del flusso, dovute al movimento del pistone. Ogni funzione della pompa (Fig. 3) è regolata da un controllore elettronico.
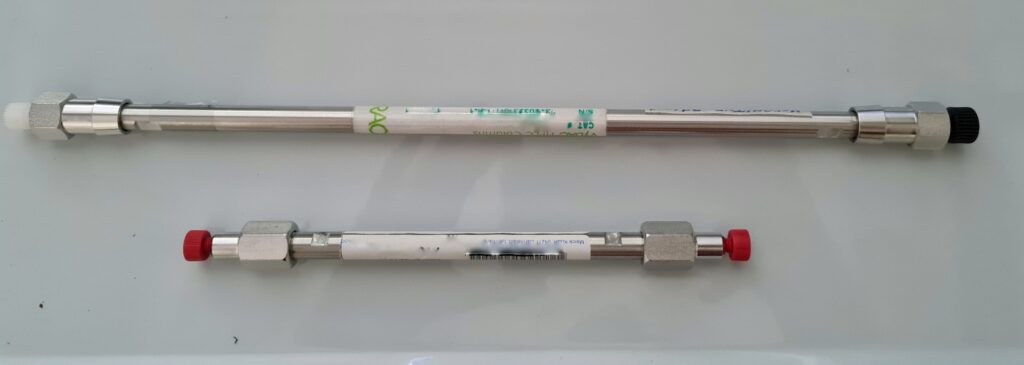
- Colonna e precolonna: le colonne (Fig. 4) possono essere preparative, analitiche o microanalitiche, in base alla quantità di campione che possono separare. La fase stazionaria al loro interno è caratterizzata dal diametro e forma delle particelle, porosità e chimica della superficie. Sono poste in appositi vani. La precolonna, più corta, è della stessa fase stazionaria della colonna e protegge quest’ultima da possibili inquinanti presenti nei campioni.
- Termostato: alloggiamento per la colonna utilizzato per mantenere una temperatura stabile, garantendo la riproducibilità delle analisi.
- Rilevatore: manda un segnale elettrico proporzionale alla concentrazione della sostanza cromatografata. È costituito da una cella al suo interno in cui passa il campione. Le tipologie di rilevatore verranno definite nel sottoparagrafo successivo.
- Integratore: registra il segnale che arriva dal rilevatore (su fogli di carta o collegato al PC).
- Sistema per la raccolta di dati.

Tipologie di rilevatore
Non esistendo rilevatori universali, questi dispositivi vengono giudicati in base a proprietà quali selettività, stabilità ed altre. I rilevatori possono essere delle seguenti tipologie:
- A UV-VIS: è il rilevatore (Fig. 5) più utilizzato in quanto la maggior parte delle sostanze assorbono nell’UV e la sensibilità del rilevatore nell’intervallo 190-600 nm è eccellente.
- A indice di rifrazione: misura la differenza di indice di rifrazione tra due celle, una di riferimento e quella del campione. Un fotodiodo converte la radiazione luminosa in segnale elettrico. Ha una bassa sensibilità di rilevazione.
- A fluorescenza: la lunghezza d’onda (di eccitazione) desiderata viene selezionata dalla luce UV-VIS e inviata alla cella. Quando una molecola fluorescente passa dalla cella, assorbe la luce e la riemette a una lunghezza d’onda di emissione diversa. È un rilevatore molto sensibile e selettivo.
- A schiera di diodi (Diode Array): molto simile al rilevatore UV-VIS, ha come differenza la possibilità di inviare nella cella fasci di radiazione luminosa di diversa lunghezza d’onda contemporaneamente. È utilizzato per valutare la purezza di una sostanza o per identificare i picchi.
- Elettrochimico: la misura utilizzata più di frequente per produrre rilevatori di questa tipologia è quella amperometrica (per ossidazione o riduzione dell’analita); è una tecnica molto sensibile. Esistono anche rilevatori elettrochimici che sfruttano la conducibilità degli elettroliti nel campione per identificare le sostanze in esame.
Sono presenti anche altri metodi di rilevazione come, ad esempio, quelli a radioattività nell’industria farmaceutica.

Metodi di separazione con HPLC
Alcuni dei metodi di separazione eseguiti con l’HPLC sono:
- A fase normale: è la tradizionale separazione in cui la fase stazionaria è più polare di quella mobile; i componenti a bassa polarità vengono eluiti per primi in quanto le molecole polari sono più o meno trattenute in base alle forze di interazione che creano con i gruppi funzionali sul particellato. L’eluente usato è a bassa o moderata polarità (ad esempio l’esano), mentre la fase stazionaria è comunemente costituita da un gel di silice con la possibile aggiunta di gruppi che provvedono alla polarità.
- A fase inversa: è la tecnica più comune in quanto può essere utilizzata con molte sostanze. In questo caso si ha una fase mobile polare e una fase stazionaria idrofobica. Gli eluenti utilizzati sono miscele acquose di solventi organici (la forza dell’eluente aumenta maggiore è il tenore del solvente organico); in questa separazione le sostanze più polari eluiscono per prime.
- A scambio ionico: utilizzato per separare sostanze ioniche, la sua fase stazionaria è costituita da gruppi funzionali ionici legati a gel di silice o polimeri adatti. In questo caso la fase mobile utilizzata è un tampone acquoso (a volte miscelato con metanolo o acetonitrile).
- A coppia ionica: utilizzata nella separazione di sostanze a multipla ionizzazione, fortemente polari e/o fortemente basiche. La fase stazionaria è uguale a quella utilizzata nella cromatografia a fase inversa o normale; all’eluente è aggiunto un contro-catione idrofobico che lega la molecola che si vuole separare (di carica opposta) formando una coppia ionica che si lega alla fase stazionaria.
- Ad esclusione molecolare: diversamente dalle altre metodologie, che separano grazie alle interazioni con la fase stazionaria, in questo caso le sostanze sono separate con un sistema di micropori, sulla base della dimensione delle molecole. Due tecniche di realizzazione sono cromatografia a permeazione del gel (GPC, con solventi organici) e cromatografia a filtrazione su gel (GFC, con soluzione acquosa).
Nel prossimo articolo, L’HPLC (Parte 2), si parlerà degli utilizzi, del funzionamento, i limiti dello strumento e le precauzioni da prendere durante l’utilizzo.
Fonti
- De Sio F. (1998). Introduzione all’HPLC – Manuale per corso di formazione “Addetti Controllo Qualità” 1997/1998.
- Dong M. W. (2006). Modern HPLC for Practicing Scientists. John Wiley & Sons, Inc.
- Snyder L.R, Kirkland J.J, Glajch J.L. (1997). Practical HPLC method development. A Wiley-Interscience Publication, John Wiley & Sons, Inc.
- www.bmscience.net
- www.disc.chimica.unipd.it
- www.waters.com