Il Whole Genome Sequencing (WGS) è una tecnica di sequenziamento del DNA che permette di determinare la sequenza completa del genoma di un organismo. In ambito microbiologico viene utilizzata principalmente per analizzare genomi di batteri o virus.

Procedimento
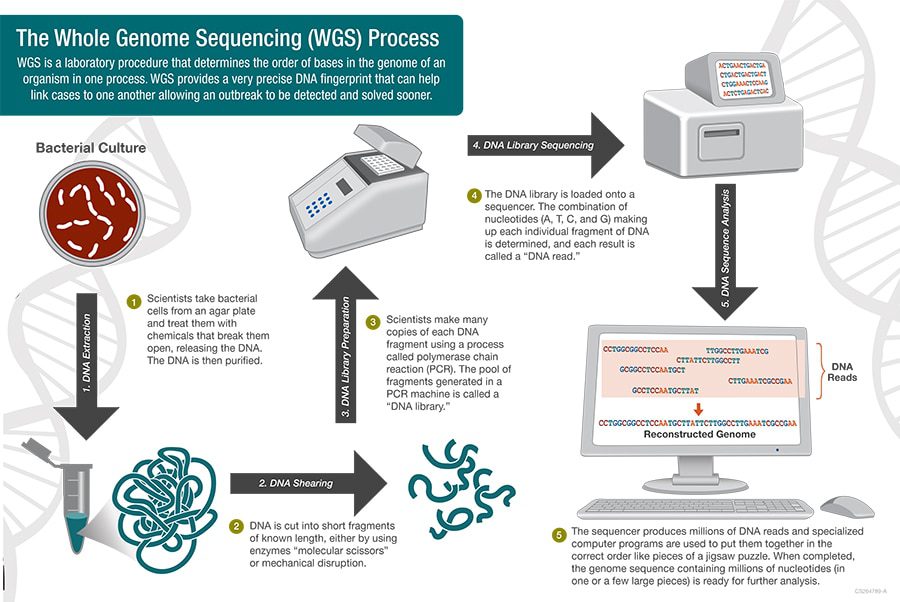
Le fasi che compongono il processo sono molteplici e combinano più tecnologie. Ecco come funziona in linea generale:
- Estrazione del DNA: il primo passo è l’estrazione del DNA dalle cellule dell’organismo di interesse. Il materiale di partenza varia a seconda dell’organismo in esame (può essere un campione di sangue, saliva, tessuti, cellule batteriche, colonie fungine, ecc.).
- Frammentazione: si procede alla frammentazione del DNA estratto mediante lisi meccanica o chimica perché le tecnologie di sequenziamento attuali possono leggere brevi tratti di DNA alla volta.
- Preparazione della libreria: ai frammenti di DNA devono essere aggiunte delle sequenze specifiche di nucleotidi che identificano i campioni (è possibile analizzare più campioni contemporaneamente) e delle sequenze di DNA necessarie alla tecnologia di sequenziamento utilizzato (adattatori o “adapters“). L’insieme dei frammenti così modificati prende il nome di libreria di sequenziamento. Affinchè la libreria sia pronta viene effettuata un apposita PCR.
- Sequenziamento: si sequenzia il DNA frammentato utilizzando tecniche di sequenziamento massivo in parallelo (NGS) di seconda o terza generazione (come PacBio o MinION). Questi metodi leggono le basi nucleotidiche (A, T, C, G) che compongono milioni di frammenti di DNA. Alla fine dell’analisi, tutti i frammenti sequenziati vengono memorizzati in appositi file.
- Allineamento: i dati grezzi generati dal sequenziamento subiscono una serie di processi bioinformatici (anche indicati come pipeline) necessari per confrontare i frammenti sequenziati con un genoma di riferimento. Questo è un passo fondamentale al fine di ricostruire la sequenza completa del genoma.
- Assemblaggio: si assemblano i frammenti mediante software, in modo da creare una sequenza digitalizzata continua che rappresenta l’intero genoma.
- Analisi: si analizza ulteriormente la sequenza completa del genoma così da identificare eventuali varianti genetiche, mutazioni e altre caratteristiche.
WGS in Microbiologia
Le applicazioni comuni del WGS nella diagnostica microbiologica consistono principalmente nella caratterizzazione degli isolati, nell’identificazione della resistenza antimicrobica e nella sorveglianza delle malattie infettive.
Caratterizzazione degli isolati
Il WGS può essere utilizzato per caratterizzare un isolato clinico, informando sulla probabile specie e/o sottotipo e consentendo il posizionamento filogenetico di una data sequenza rispetto a un set esistente di isolati. L’identificazione del ceppo basata su WGS fornisce una risoluzione di gran lunga superiore rispetto agli approcci basati su marcatori genetici come la tipizzazione di sequenze multilocus (MLST) e può essere utilizzata quando tecniche standard come l’elettroforesi su gel a campo pulsato (PFGE), la profilazione a ripetizione tandem a numero variabile (VNTR) e MALDI-TOF non riescono a distinguere accuratamente i lignaggi.
Identificazione della resistenza antimicrobica
Oltre all’identificazione e alla caratterizzazione delle specie, le sequenze del genoma forniscono una ricca risorsa che può essere sfruttata in modo da predire il fenotipo del patogeno. I principali tratti microbici di rilevanza clinica sono la resistenza ai farmaci e la virulenza, ma possono includere anche altri tratti come la capacità di formare biofilm o la sopravvivenza in un determinato ambiente.
Attraverso il sequenziamento dell’intero genoma, è possibile identificare geni e mutazioni specifiche che conferiscono resistenza ai farmaci. Ecco alcuni esempi:
- Gene blaNDM−1: Codifica per un enzima che degrada diversi antibiotici beta-lattamici
- Mutazioni nel gene rpoB: Conferiscono resistenza alla rifampicina in Mycobacterium tuberculosis
- Gene mecA: Responsabile della resistenza alla meticillina in Staphylococcus aureus (MRSA) [QUI un articolo di approfondimento]
L’uso del Whole Genome Sequencing in microbiologia rappresenta un progresso significativamente utile nella lotta contro le infezioni resistenti.
Sorveglianza delle malattie infettive
Quando un patogeno viene sequenziato, i dati genetici possono essere confrontati con quelli di altre infezioni, permettendo di stabilire collegamenti tra casi apparentemente isolati. Questo è particolarmente utile in situazioni di epidemie, dove è fondamentale identificare rapidamente i focolai e interrompere le catene di trasmissione. Ad esempio, durante l’epidemia di COVID-19, il sequenziamento del genoma del virus SARS-CoV-2 ha permesso di monitorare le varianti emergenti e di comprendere meglio la loro diffusione.
Oltre alle epidemie, il WGS viene utilizzato in alcuni laboratori di sanità pubblica per la sorveglianza delle malattie infettive causate da alcuni patogeni come ad esempio Mycobacterium tuberculosis e Legionella pneumophila.
I dati di sequenziamento possono inoltre essere condivisi tra i laboratori di tutto il mondo, migliorando la risposta globale alle malattie infettive.
Svantaggi del WGS in microbiologia
Il principale problema è sicuramente la mancanza di standardizzazione nelle analisi e l’accesso limitato ai controlli di qualità. A tal proposito, per alcune analisi microbiologiche, L’ECDC fornisce annualmente un controllo di qualità a tutti i laboratori nazionali di riferimento. Altri svantaggi sono i costi elevati della strumentazione e l’esigenza di disporre di professionisti qualificati e competenti, in particolare per le analisi bioinformatiche. Per tali motivi il WGS viene effettuato in pochi centri di riferimento. Infine, il WGS attualmente può essere eseguito solo su isolati batterici ottenuti dopo coltura. Questo può costituire un problema per l’analisi di batteri a lenta crescita.
Altre applicazioni del Whole Genome Sequencing
Il WGS non ha rivoluzionato solo la microbiologia. Una visione dettagliata e completa del genoma di un organismo è certamente utile in diverse applicazioni, vediamone alcune:
- In genetica medica permette di identificare tutte le varianti genetiche, comprese quelle rare e complesse. Il WGS consente anche di identificare nuove varianti genetiche che potrebbero non essere rilevate con altri metodi di sequenziamento. Questo è particolarmente utile per la ricerca di nuove malattie e per comprendere meglio le basi genetiche di molte condizioni. Inoltre il WGS può supportare la medicina di precisione, permettendo di adattare i trattamenti alle specifiche varianti genetiche del paziente. Questo approccio può migliorare l’efficacia delle terapie nonchè ridurre gli effetti collaterali.
- Nell’ambito della ricerca e sviluppo di nuovi farmaci, il WGS permette di studiare l’evoluzione delle specie, comprendere la diversità genetica delle popolazioni e sviluppare nuove terapie e vaccini.
- In agricoltura e zootecnia, il WGS può essere utilizzato per migliorare le caratteristiche genetiche delle colture e degli animali, migliorando la produttività e la resistenza alle malattie.
Altre tipologie di sequenziamento
Le tecniche di NGS permettono di sequenziare DNA genomico, il trascrittoma o l’epigenoma. Tra i metodi di sequenziamento del DNA genomico, possiamo distinguere:
- Sequenziamento dell’intero genoma (Whole-genome sequencing)
- Sequenziamento dell’esoma (Whole Exome Sequencing, Clinical Exome Sequencing)
- Sequenziamento di geni mirati (Targeted NGS)
Sequenziamento dell’esoma
Il sequenziamento dell’esoma consiste nel sequenziamento selettivo della piccolissima parte del genoma umano che codifica per le proteine. Il Whole Exome Sequencing (WES) permette di sequenziare tutti i geni umani mentre il Clinical Exome Sequencing (CES) permette di sequenziare tutti i geni fino ad ora noti per essere associati a malattia (circa 6.000).
Sequenziamento di geni mirati
Nel sequenziamento di geni mirati (Targeted NGS o tNGS) le sequenze target che si vogliono esaminare vengono prima amplificate e poi sequenziate. È un metodo utilizzato in microbiologia poichè consente di utilizzare direttamente campioni biologici come materiale di partenza, senza effettuarne una coltura microbica. Tuttavia, il tNGS fornisce informazioni su una frazione limitata del genoma.
Sequenziamento del trascrittoma (RNA)
La comprensione del trascrittoma è essenziale per interpretare gli elementi funzionali del genoma, per comprendere i costituenti molecolari di cellule e tessuti e per interpretare lo sviluppo e le malattie. In sintesi, gli obiettivi principali della trascrittomica sono:
- catalogare tutte le specie di trascritti, compresi gli mRNA, gli RNA non codificanti e i MicroRNA;
- determinare la struttura trascrizionale dei geni, in termini di siti di inizio, estremità 5′ e 3′, modelli di splicing e altre modifiche post-trascrizionali;
- quantificare i livelli di espressione di ciascun trascritto durante lo sviluppo e in condizioni diverse.
Sequenziamento epigenetico
Sono state sviluppate procedure che sequenziano aree del genoma in cui si sono verificate modificazioni epigenetiche. Ad esempio, esistono metodiche che permettono la mappatura ad alta risoluzione (a livello di singola base) dello stato di metilazione del DNA e di definire la struttura della cromatina dell’intero genoma.
Fonti
- Brlek P, Bulić L, Bračić M, Projić P, Škaro V, Shah N, Shah P, Primorac D. Implementing Whole Genome Sequencing (WGS) in Clinical Practice: Advantages, Challenges, and Future Perspectives. Cells. 2024 Mar 13;13(6):504. doi: 10.3390/cells13060504. PMID: 38534348; PMCID: PMC10969765.
- Balloux F, Brønstad Brynildsrud O, van Dorp L, Shaw LP, Chen H, Harris KA, Wang H, Eldholm V. From Theory to Practice: Translating Whole-Genome Sequencing (WGS) into the Clinic. Trends Microbiol. 2018 Dec;26(12):1035-1048. doi: 10.1016/j.tim.2018.08.004. Epub 2018 Sep 4. PMID: 30193960; PMCID: PMC6249990.
- Wang Z, Gerstein M, Snyder M. RNA-Seq: a revolutionary tool for transcriptomics. Nat Rev Genet. 2009 Jan;10(1):57-63. doi: 10.1038/nrg2484. PMID: 19015660; PMCID: PMC2949280.
- Almeida Da Silva PE, Palomino JC. Molecular basis and mechanisms of drug resistance in Mycobacterium tuberculosis: classical and new drugs. J Antimicrob Chemother. 2011 Jul;66(7):1417-30. doi: 10.1093/jac/dkr173. Epub 2011 May 9. PMID: 21558086.
- Cabibbe AM, Walker TM, Niemann S, Cirillo DM. Whole genome sequencing of Mycobacterium tuberculosis. Eur Respir J. 2018 Nov 1;52(5):1801163. doi: 10.1183/13993003.01163-2018. PMID: 30209198.
- https://bredagenetics.com/analisi-dellesoma-exome-sequencing/?lang=it
- https://www.who.int/publications/i/item/9789240061743
- https://bredagenetics.com/lista-dei-geni-whole-exome-sequencing/?lang=it