E’ stato pubblicato sulla rivista internazionale “Nature Medicine” il 28 febbraio 2022 un articolo riguardante uno studio clinico randomizzato di fase I che apre nuovi scenari nelle terapie oncologiche del tumore del rene. Il titolo di questo studio è “Nivolumab più ipilimumab con o senza supplementazione di batteri vivi nel carcinoma renale metastatico: uno studio randomizzato di fase 1”.
Questa ricerca conferma e avvalora anche gli studi e le teorie precedenti su cui sempre più clinici si concentrano, che mettono in relazione l’importanza del microbiota intestinale nella risposta all’immunoterapia.
Razionale dello studio
Lo studio è stato condotto dal team di Sarah Highlander del Translational Genomics Research Institute (TGen), a Phoenix, in Arizona. Esso ha compreso la partecipazione di 30 pazienti oncologici con uno specifico tumore del rene, il carcinoma metastatico con istologia a cellule chiare e/o sarcomatoide (fig. 1), e malattia a rischio intermedio o scarso in base ai criteri dell’International mRCC Database Consortium (IMDC).
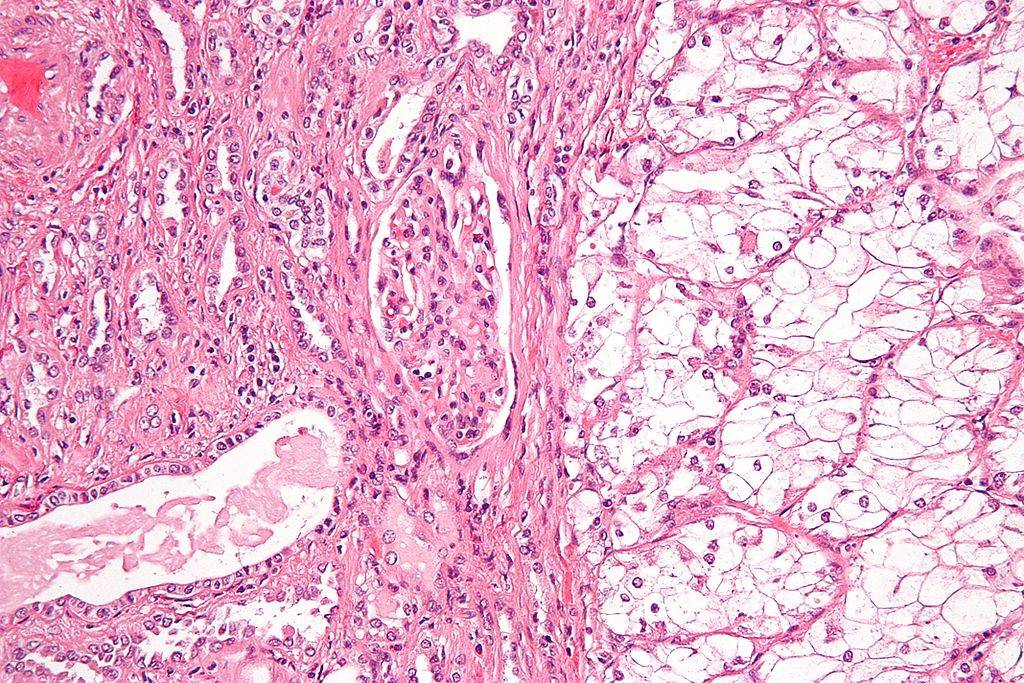
Tali pazienti sono stati randomizzati, e cioè suddivisi in due gruppi a cui sono stati assegnati casualmente in un rapporto di 2:1 a ricevere Nivolumab e Ipilimumab (immunoterapia) rispettivamente con o senza un probiotico da assumere per via orale giornalmente.
Uno dei criteri principali per l’arruolamento dei pazienti era che questo non dovesse aver già seguito una precedente terapia sistemica . La precedente terapia adiuvante era consentita a meno che con un farmaco inibitore dei checkpoint.
Il farmaco Nivolumab è un inibitore della morte programmata 1 (PD-1). Il farmaco Ipilimumab è un inibitore citotossico della proteina 4 associata ai linfociti T (CTLA-4). Questi trattamenti rappresentano uno standard di cura per il trattamento di prima linea del carcinoma renale metastatico a cellule chiare.
Durante lo studio è stato valutato anche il microbioma intestinale dei pazienti, per confrontare i cambiamenti nel tempo. Sono stati valutati anche i cambiamenti nei livelli di citochine circolanti e nelle popolazioni di cellule T regolatorie e soppressori di derivazione mieloide. Questi sono stati confrontati nel tempo per esaminare gli effetti di CBM588 (il probiotico) sul sistema immunitario.
Obiettivi dello studio
L’obiettivo primario di questa ricerca era valutare prospetticamente gli effetti del prodotto batterico vivo in questione abbinato alla terapia. Nello specifico, lo studio ha voluto caratterizzare l’effetto dell’agente sull’abbondanza relativa delle popolazioni microbiche intestinali e in particolare del Bifidobacterium spp.
Gli obiettivi secondari invece includevano il tasso di risposta, la sopravvivenza libera da progressione (PFS) e la tossicità.
Il probiotico utilizzato
Il prodotto batterico studiato è stato postulato sulla base di studi preclinici e altri studi clinici e fornito da Miyarisan Pharmaceuticals e OSEL in bustina.
Il nome che gli è stato assegnato è “CBM588”. Contiene Clostridium butyricum, un batterio sporigeno anaerobico produttore di butirrato. Ciascuna formulazione in bustina da 40 mg era composta da circa 2,0 × 108 cfu del principio attivo vitale, C. butyricum. Erano presente anche eccipienti farmaceutici come amido di mais, carbonato di calcio e lattosio.
Anche altri studi infatti supportano il ruolo di Bifidobacterium spp. nella modulazione della risposta ai farmaci inibitori dei checkpoint (CPI). In modelli preclinici inoltre il trapianto di materiale fecale arricchito con Bifidobacterium spp. da solo (anche senza CPI) si è dimostrato sufficiente per ritardare la crescita del tumore.
Risultati dello studio
I risultati dello studio hanno mostrato che aggiungendo questo probiotico alla terapia, la risposta antitumorale è stata potenziata. In particolare è stato determinato che specie come Bifidobacterium adolescentis (fig. 2) e Barnesiella intestinihominis sono state associate a un maggiore beneficio clinico dei CPI.
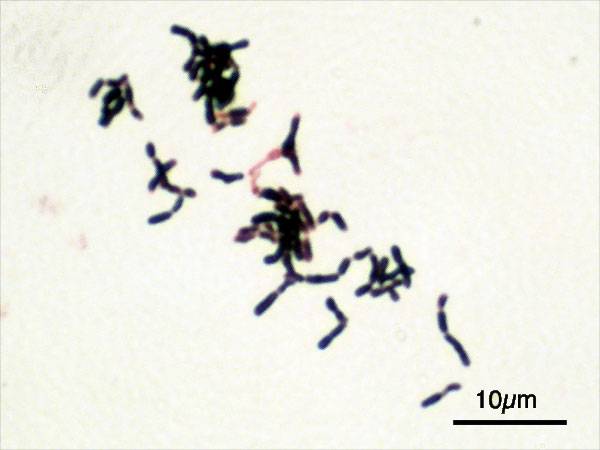
L’analisi dei dati finale (fig. 3) ha portato a queste conclusioni:
1) la sopravvivenza libera da progressione era significativamente più lunga nei pazienti trattati con il trattamento immunoterapico in associazione all’assunzione di CBM588 rispetto a quelli senza (12,7 mesi contro 2,5 mesi, hazard ratio 0,15, intervallo di confidenza 95% 0,05–0,47, P = 0,001);
2) Sebbene non statisticamente significativo, anche il tasso di risposta è stato più alto nei pazienti che hanno ricevuto CBM588 (58% contro 20%, P = 0,06);
3) Non è stata osservata alcuna differenza significativa in termini di tossicità tra i bracci dello studio
4) Una riduzione delle lesioni target del tumore del rene è stata osservata in 14 pazienti (74%) trattati con Nivolumab e Ipilimumab più CBM588 rispetto a 5 pazienti (50%) che hanno ricevuto solo la terapia oncologica.
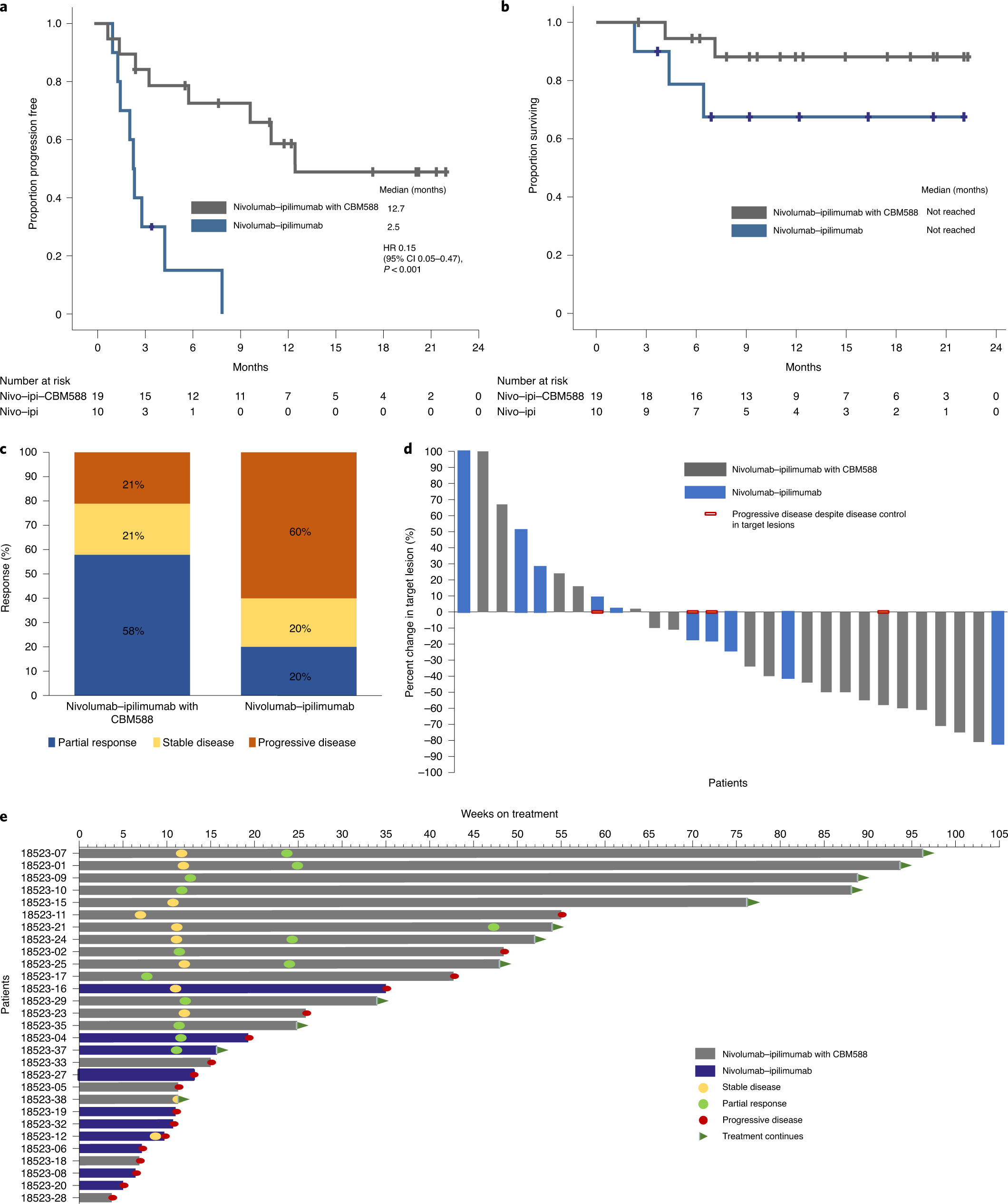
c – e, Migliore risposta per braccio di trattamento (c), miglior cambiamento nelle lesioni target rispetto al basale (d) e un diagramma dei nuotatori che mostra le caratteristiche di risposta e sopravvivenza (e). (Fonte: https://www.nature.com/articles/s41591-022-01694-6/ Credit license: http://creativecommons.org/licenses/by/4.0/).
Nonostante la dimensione piccola del campione di questo studio e la necessità di approfondire questa linea di ricerche, sempre più evidenze dimostrano l’importanza della modulazione del microbiota intestinale durante un trattamento oncologico.
Si aprono sicuramente nuovi e positivi scenari per questo tipo di tumore del rene.
Fonti:
- Dizman, N., Meza, L., Bergerot, P. et al. Nivolumab plus ipilimumab with or without live bacterial supplementation in metastatic renal cell carcinoma: a randomized phase 1 trial. Nat Med (2022).
- Routy B, Le Chatelier E, Derosa L, et al. Gut microbiome influences efficacy of PD-1-based immunotherapy against epithelial tumors. Science. 2018
- Lee, K.A., Thomas, A.M., Bolte, L.A. et al. Cross-cohort gut microbiome associations with immune checkpoint inhibitor response in advanced melanoma. Nat Med (2022).
1 commento su “Un probiotico a supporto della terapia oncologica per tumore del rene”
I commenti sono chiusi.