La rabbia è una patologia da non sottovalutare: nonostante esistano numerosi vaccini efficaci in commercio, essa infatti uccide ancora oggi più di 59000 persone ogni anno ed ha un tasso di mortalità che sfiora il 100% degli infetti non vaccinati; il virus che la causa (un virus ad RNA appartenente alla genere Lyssavirus ed alla famiglia dei Rhabdoviridae) è dotato di un capside oblungo, a forma di proiettile, con un rivestimento (envelope) che presenta caratteristiche proteine di membrana.
Tuttavia Lyssavirus potrebbe diventare in un futuro non troppo lontano un prezioso alleato nel combattere efficacemente devastanti malattie neurodegenerative ad oggi incurabili, quali il morbo di Parkinson e l’Alzheimer.
Un team di scienziati del Sainsbury Wellcome Center for Neural Circuits and Behavior di Londra guidato dal Dottor Andrew J.Murray, in collaborazione con altri gruppi di ricerca internazionali, ha pensato infatti di sfruttare la capacità del virus della rabbia di saltare da un neurone all’altro per visualizzare le connessione tra i vari neuroni del cervello al fine di crearne una vera e propria mappa dettagliata (Fig.1).

Studiando approfonditamente il meccanismo molecolare utilizzato dal virus per il suo viaggio, il team del Dottor Murray ha creato delle forme geneticamente modificate dello stesso che permettono di utilizzarlo come un vero e proprio tracciante, capace di emettere un segnale rilevabile ed identificabile con certezza, in ogni singolo neurone che attraversa; questo permette di costruire una mappa, una “cartina stradale” del suo itinerario sino al cervello, che coincide con la mappa dei neuroni e delle connessioni tra i neuroni stessi: le sinapsi.
Per raggiungere questo importante traguardo, è stato necessario manipolare il genoma del virus attraverso le tecnologie più moderne d’ingegneria genetica messe a disposizione dalla biologia molecolare; questo ha permesso di ottenere, dopo un lungo lavoro di anni che ha coinvolto numerosi gruppi di scienziati di diversi continenti, il cosiddetto: ”Sistema delta-G”: una forma finale di virus della rabbia geneticamente modificato, creato appositamente per essere un potente ed efficace strumento d’indagine della struttura fine dei circuiti e delle connessioni celebrali.
Sono stati necessari tre importanti interventi sul genoma del virus naive (Fig.2) per creare il Sistema delta-G che hanno richiesto l’uso di numerose metodiche diverse delle Biotecnologie.
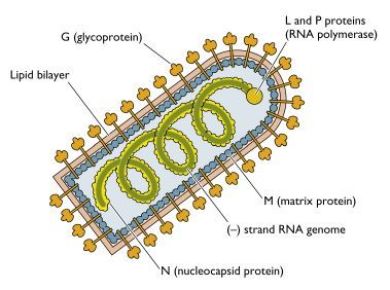
Dapprima, il gene per la glicoproteina è stato sostituito da un gene che codificasse una proteina fluorescente, una proteina cioè capace di emettere un segnale luminoso se eccitata a particolari lunghezze d’onda; in questo modo si è dato al virus la capacità di diventare un tracciante rilevabile.
Senza glicoproteina però esso è incapace di spostarsi tra i neuroni: per questa ragione è stato necessario accoppiarlo ad un altro virus, stavolta innocuo, che avesse un gene per la glicoproteina della rabbia nel suo DNA aggiunto artificialmente e che svolgesse un’infezione concomitante nello stesso neurone.
Si è scelto il virus AAV, un virus di origine aviaria che normalmente non infetta i mammiferi: quando esso entra nel neurone (grazie alla glicoproteina in questione) replica ma se nella stessa cellula è presente anche il virus della rabbia la sua glicoproteina è assunta da quest’ultimo, che può cosi’ proseguire senza problemi il suo viaggio in un altro neurone.
Tuttavia, occorreva risolvere un ultimo problema: era necessario poter controllare e regolare l’infezione del virus ai soli gruppi o popolazioni di neuroni d’interesse, evitando si diffondesse in maniera indiscriminata, cosi’ da disporre di uno strumento d’indagine veramente selettivo.
Se ad esempio si desiderasse usare il sistema delta-G per studiare il morbo di Parkinson, l’infezione dovrebbe essere circoscritta ai soli neuroni che rilasciano la dopamina (la cui carenza provoca appunto la patologia), che sono presenti solo in alcune regioni del cervello.
Dal momento che questi tipo di studi ed esperimenti sono condotti su modelli animali (per lo più murini) ben caratterizzati e di cui è ormai prassi consolidata manipolare il genoma nei modi più diversi, si è intervenuti sulla porzione di DNA del topo che codifica per le proteine di rivestimento dei neuroni, sostituendo i geni naive con geni di proteine che riconoscessero glicoproteine di rivestimento virali di virus aviari (che normalmente non infettano i mammiferi); parallelamente si è ulteriormente modificato il virus della rabbia, dotandolo di un rivestimento glicoproteico tipico dei virus aviari: il virus finale può perciò infettare solo quei neuroni trasformati che sono in grado di riconoscere il suo particolare rivestimento glicoproteico atipico.
E’ un sistema che, per usare un’immagine di facile comprensione, si può immaginare come il rapporto che esiste tra una chiave ed una serratura: i neuroni in cui è stato clonato il gene per la proteina che riconosce solo la glicoproteina del virus aviario sono le serrature, mentre quest’ultima è la chiave; la serratura è specifica per la sua chiave (e viceversa), nessun’altra chiave potrebbe aprire la porta (cioè dare l’accesso al neurone).
In questo modo l’infezione del virus tracciabile si diffonde solo nei neuroni che dispongono della giusta “serratura” che riconosce la sua “chiave”.
Il Dottor Murray ha affermato di poter osservare, grazie al sistema delta-G, interi circuiti neuronali scaricare impulsi nervosi nel topo quando l’animale compie un’azione o un movimento, visualizzando mappe dettagliate di quella rete intricata di neuroni che è il cervello; è stato inoltre in grado di attivarli o disattivarli a piacere eccitando la proteina fluorescente del virus geneticamente modificato e tutto questo fino ad un mese dopo che il virus aveva infettato il neurone, ottenendo cosi’ un ampio margine di tempo in cui poter eseguire test mirati.
Ovviamente la disponibilità di un metodo d’indagine tanto potente come il sistema delta-G non è limitato ai soli studi riguardanti le malattie neurodegenerative ma è applicabile anche negli studi comportamentali delle neuroscienze; capire infatti quali circuiti del cervello si attivino (e come) in risposta ad uno stimolo potrebbe permette d’indagare meglio anche molti disturbi della personalità come la depressione, la schizofrenia o la sindrome bipolare.
Tuttavia l’interesse maggiore è ovviamente rivolto all’utilizzo del virus della rabbia geneticamente modificato per indagare il morbo di Parkinson e l’Alzheimer, dato il loro devastante effetto invalidante e la disponibilità attuale di farmaci che possono solo alleviare i sintomi ma non dare un effetto terapeutico definitivo.
Il Dottor Murray è fiducioso che questo nuovo metodo d’indagine potrà, forse in un futuro non troppo lontano, portare ad un nuovo approccio terapeutico veramente risolutivo di queste terribili patologie del nostro sistema nervoso centrale.
Bibliografia di riferimento
“Le Scienze”; volume numero 605, pagine 56-61, edizione del 3 Gennaio 2019
Ulteriore sitografia di riferimento
Sulla rabbia negli animali, in particolare negli animali domestici:
http://www.vetinweb.it/cm_siv/sites/default/files/SELVATICI%20E%20ALTRI%20-%2001%20RABBIA.pdf
Sitografia delle immagini
Immagine in evidenza:
Figura 1:
https://www.medicinaoltre.com/patologie/patologie_dettaglio.php?id=621
Figura 2: