Scopri come CRISPR/Cas9 sta rivoluzionando il miglioramento genetico tramite le biotecnologie vegetali delle piante.
Indice
Da un sistema di difesa microbico a una delle tecnologie più promettenti per l’agricoltura del futuro: CRISPR/Cas9 sta cambiando il modo in cui pensiamo al miglioramento genetico delle piante, tra opportunità scientifiche e interrogativi etici.
La scoperta di CRISPR: una rivoluzione nata per caso da sequenze misteriose nel DNA microbico
Negli anni Novanta, studiando il genoma di alcuni microrganismi, i ricercatori notarono la presenza di strane sequenze ripetute, separate da frammenti di DNA apparentemente casuali. Queste sequenze vennero poi chiamate CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats), ma per molto tempo la loro funzione rimase ignota.
Un contributo decisivo arrivò nel 2005, quando il microbiologo Francisco Mojica propose un legame tra queste sequenze e i virus che infettano i microrganismi (batteri e archea), osservandolo in particolare nell’archeo Haloferax mediterranei. Questa intuizione, infatti, aprì la strada a una nuova interpretazione del sistema CRISPR come meccanismo di difesa adattativa.
In seguito, nel 2007, si scoprì che tale sistema rappresenta una vera e propria memoria immunologica: quando un microrganismo sopravvive a un’infezione virale, conserva piccoli frammenti del DNA del virus all’interno del proprio genoma, che vengono poi utilizzati per riconoscere e neutralizzare il patogeno in caso di nuove infezioni. In particolare, l’azione difensiva è resa possibile dalla combinazione delle sequenze CRISPR con proteine enzimatiche endonucleasiche chiamate Cas (CRISPR-associated), capaci di tagliare il DNA estraneo in modo altamente specifico (Figura 1)..
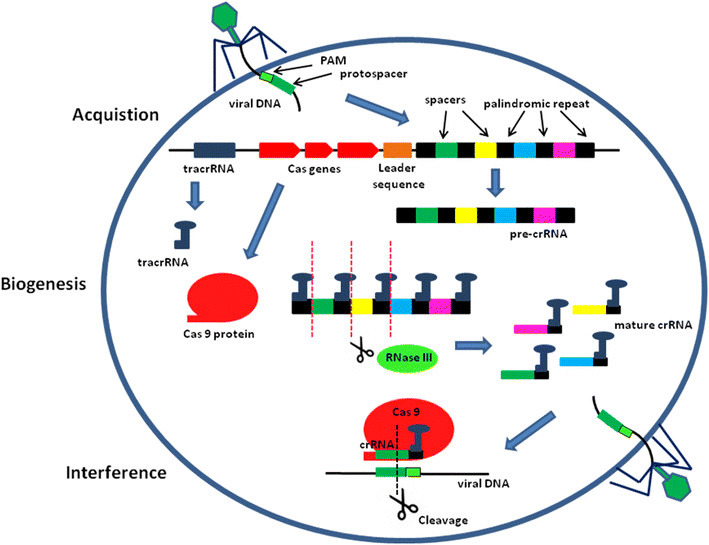
CRISPR/Cas9: come funziona la forbice molecolare
Dalla microbiologia all’ingegneria genetica
Il passaggio da meccanismo naturale a strumento biotecnologico avviene nel 2012, quando un gruppo di ricercatori dimostrò che il sistema CRISPR/Cas9 poteva essere riprogrammato per tagliare il DNA in punti specifici e controllati. La proteina Cas9, in particolare, si rivelò ideale per questo scopo grazie alla sua capacità di produrre un taglio netto a doppio filamento, facilmente guidabile tramite una sequenza di RNA complementare al gene bersaglio.
Un ruolo centrale in questa scoperta fu svolto da Jennifer Doudna e Emmanuelle Charpentier, che, lavorando in collaborazione con team di ricerca distribuiti tra Stati Uniti ed Europa, dimostrarono come CRISPR/Cas9 potesse essere trasformato in una vera e propria forbice molecolare programmabile. Questo risultato mise in luce l’importanza della cooperazione internazionale nella ricerca scientifica, sempre più basata su reti globali di competenze.
La scoperta assunse inoltre un forte valore simbolico: in un ambito storicamente dominato da figure maschili, il contributo decisivo di due scienziate evidenziò il ruolo fondamentale delle donne nella ricerca scientifica contemporanea. Il riconoscimento arrivò nel 2020, quando a Doudna e Charpentier fu assegnato il Premio Nobel per la Chimica, segnando una tappa significativa nella storia delle biotecnologie moderne.
Il meccanismo in breve
Il funzionamento di CRISPR/Cas9 è sorprendentemente semplice (Figura 2). Un RNA guida viene progettato per essere complementare al gene bersaglio e accompagna la proteina Cas9 fino al punto preciso del genoma, dove viene indotto un taglio a doppio filamento del DNA.
A questo punto entra in gioco la cellula, che attiva i propri meccanismi di riparazione del DNA. Il più comune è il Non-Homologous End Joining (NHEJ), un processo rapido ma impreciso che può introdurre piccole inserzioni o delezioni di nucleotidi (in/dels), spesso sufficienti ad inattivare un gene (knock-out). In alternativa, se viene fornito un frammento di DNA stampo, la cellula può sfruttare la Homology-Directed Repair (HDR), un meccanismo basato sulla ricombinazione omologa che consente l’inserzione precisa di unasequenza desiderata (knock-in).
Grazie alla combinazione tra taglio mirato e riparazione cellulare, CRISPR/Cas9 permette di silenziare un gene, modificarne la funzione oppure introdurre nuove sequenze genetiche, motivo per cui questa tecnologia viene spesso descritta come una forbice molecolare programmabile.
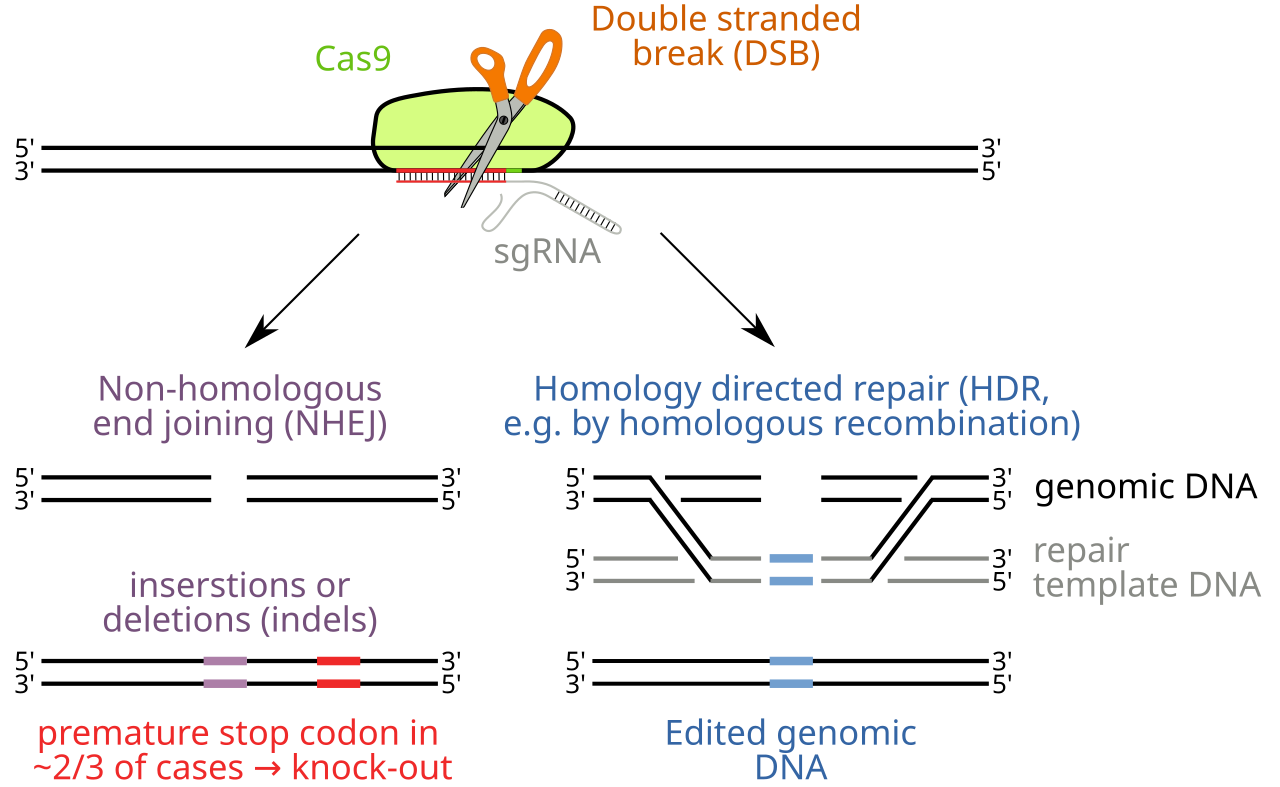
CRISPR e biotecnologie vegetali
Un nuovo approccio al miglioramento genetico
Nel settore delle scienze agrarie, CRISPR/Cas9 rappresenta un vero cambio di paradigma nel miglioramento genetico delle colture. Questa tecnologia rientra nel più ampio ambito del genome editing, un insieme di approcci che consentono di modificare in modo mirato la sequenza del DNA di un organismo, intervenendo direttamente sui suoi geni.
All’interno di questo contesto si collocano le Tecniche di Evoluzione Assistita (TEA), che comprendono strumenti come CRISPR/Cas9 e permettono di ottenere mutazioni specifiche senza introdurre necessariamente DNA esogeno. Per questo motivo, le piante sviluppate mediante le TEA si distinguono dagli organismi geneticamente modificati (OGM) ottenuti con tecniche di transgenesi classica, nelle quali viene inserito materiale genetico proveniente da altre specie.
Di conseguenza, molte piante ottenute tramite genome editing risultano geneticamente indistinguibili da quelle derivate da mutazioni naturali o da programmi di selezione tradizionale, pur beneficiando di un processo di sviluppo più rapido, controllato ed efficiente.
Applicazioni principali in agricoltura
L’uso di CRISPR nelle piante ha già generato risultati solidi in ambito sperimentale e, in alcune nazioni, sta iniziando a tradursi in applicazioni pre-commerciali o di mercato. Tra le principali direzioni di sviluppo si annoverano:
- aumento della resistenza a patogeni fungini, virali e batterici;
- miglioramento della tolleranza a stress abiotici, come siccità e salinità;
- incremento della resa e dell’efficienza d’uso delle risorse.
In un contesto di cambiamento climatico e crescita della popolazione mondiale, tale biotecnologia assume un valore strategico per favorire un’agricoltura più sostenibile (Figura 3). Piante più resistenti alle malattie richiedono un uso ridotto di fitofarmaci, mentre varietà più tolleranti allo stress idrico necessitano di minori volumi d’acqua. Tuttavia, la diffusione su larga scala dipende da valutazioni di sicurezza, accettazione sociale e, soprattutto, dai diversi quadri regolatori nazionali.

Aspetti etici e regolatori
Il dibattito scientifico e sociale
Nonostante le grandi potenzialità, CRISPR/Cas9 solleva importanti questioni etiche. Una delle principali riguarda la sicurezza: sebbene il genome editing consenta una mutagenesi altamente mirata, la possibilità teorica di effetti off-target, ovvero modifiche indesiderate in siti genomici simili alla sequenza bersaglio, richiede attente valutazioni e controlli. In altre parole, pur essendo una forbice molecolare progettata con grande precisione, la risposta dei sistemi biologici non può essere considerata completamente prevedibile.
Le implicazioni etiche del genome editing sono emerse con forza anche al di fuori dell’ambito delle scienze agrarie. Nel 2018, l’annuncio in Cina dell’editing genetico di embrioni umani destinati alla nascita di due gemelle, condotto dal ricercatore He Jiankui, ha suscitato un forte scalpore a livello internazionale. L’episodio, ampiamente condannato dalla comunità scientifica, ha evidenziato la necessità di regole condivise, trasparenza e responsabilità nell’uso di tali tecnologie.
Un ulteriore nodo critico è legato alla governance della tecnologia. Il controllo dei brevetti e l’accesso alle tecniche di genome editing potrebbero accentuare le disuguaglianze tra grandi aziende e piccoli produttori agricoli, rendendo centrale il tema di una regolamentazione equa e inclusiva.
Il caso europeo: OGM, TEA e regolamentazione
Nel contesto normativo dell’Unione Europea (UE), le piante ottenute tramite CRISPR sono state a lungo equiparate agli OGM tradizionali. Questa impostazione deriva in larga parte dalla sentenza della Corte di Giustizia dell’UE del 2018, che ha incluso le tecniche di genome editing nell’ambito di applicazione della direttiva sugli OGM, richiamando il principio di precauzione.
Tale interpretazione ha contribuito a rallentare la sperimentazione e l’adozione delle TEA rispetto alle nazioni extra-UE, dove il quadro regolatorio risulta più flessibile. Negli ultimi anni, tuttavia, il dibattito si è riaperto: la Commissione Europea ha avviato un processo di revisione normativa volto a distinguere le tecniche di transgenesi dal genome editing, riconoscendo il potenziale delle TEA nel favorire sistemi agricoli più sostenibili.
Anche a livello nazionale, il quadro normativo è in evoluzione. Infatti, recenti interventi legislativi hanno introdotto procedure semplificate per la sperimentazione in campo delle piante ottenute tramite TEA, segnando un primo passo verso un possibile allineamento con il dibattito europeo in corso.
Una tecnologia potente, non una soluzione magica
CRISPR/Cas9 non rappresenta una risposta universale a tutti i problemi dell’agricoltura moderna. Tuttavia, costituisce uno degli strumenti più promettenti oggi a disposizione delle biotecnologie vegetali, soprattutto in un contesto segnato da cambiamento climatico, pressione sulle risorse naturali e crescente domanda alimentare. Il vero obiettivo non è solo sviluppare piante più performanti, ma farlo in modo responsabile, trasparente e condiviso, integrando l’innovazione scientifica con valutazioni etiche, ambientali e sociali. In definitiva, la sfida non riguarda tanto la tecnologia in sé, quanto il modo in cui la società sceglierà di utilizzarla, regolamentarla e accettarla. È in questo equilibrio tra progresso scientifico e responsabilità collettiva che si gioca il futuro del genome editing in agricoltura.
Fonti
- Mojica, F. J. M., Díez-Villaseñor, C., García-Martínez, J., & Soria, E. (2005). Intervening sequences of regularly spaced prokaryotic repeats derive from foreign genetic elements. Journal of Molecular Evolution. 60(2), 174–182
- Barrangou, R., et al. (2007). CRISPR provides acquired resistance against viruses in prokaryotes. Science. 315(5819), 1709–1712.
- Jinek, M., et al. (2012). A programmable dual-RNA–guided DNA endonuclease in adaptive bacterial immunity. Science. 337(6096), 816–821.
- Doudna, J. A., & Charpentier, E. (2014). The new frontier of genome engineering with CRISPR-Cas9.
Science, 346(6213), 1258096. - The Nobel Prize in Chemistry 2020. Press release: The Nobel Prize in Chemistry 2020. The Royal Swedish Academy of Sciences.
- Puchta, H. (2005). The repair of double-strand breaks in plants: mechanisms and consequences for genome evolution. Journal of Experimental Botany, 56(409), 1–14.
- Chen, K., Wang, Y., Zhang, R., Zhang, H., & Gao, C. (2019). CRISPR/Cas genome editing and precision plant breeding in agriculture. Annual Review of Plant Biology, 70, 667–697.
- EFSA Panel on Genetically Modified Organisms (GMO). (2021). Applicability of the EFSA GMO Panel guidance documents to plants developed using New Genomic Techniques. EFSA Journal, 19(3).
- Sprink, T., et al. (2016). Regulatory hurdles for genome editing: process- vs. product-based approaches. Plant Cell Reports, 35, 1493–1508
- Cyranoski, D. (2018). What CRISPR-baby prison sentences mean for research. Nature, 577, 154–155.
- Lander, E. S., et al. (2019). Adopt a moratorium on heritable genome editing. Nature, 567, 165–168.
- World Health Organization (WHO). (2021). Human genome editing: recommendations. World Health Organization.
- Court of Justice of the European Union. (2018). Judgment of the Court (Grand Chamber) of 25 July 2018, Case C-528/16.
- European Commission. (2021). Study on the status of new genomic techniques under Union law and in light of the Court of Justice ruling in Case C-528/16. European Union.
- European Commission. (2023). Proposal for a Regulation on plants obtained by certain new genomic techniques and their food and feed.
- Legge 24 febbraio 2023, n. 14. Conversione in legge, con modificazioni, del decreto-legge 29 dicembre 2022, n. 198.
Crediti e Immagini
- Immagine in evidenza: Immagine originale realizzata dall’autore con il supporto di intelligenza artificiale (ChatGPT, OpenAI)
- Figura 1: Link1
- Figura 2: Link2
- Figura 3: Immagine originale realizzata dall’autore con il supporto di intelligenza artificiale (ChatGPT, OpenAI)