Perdite da milioni di tonnellate
Nei Paesi in via di sviluppo, ogni anno, si registrano perdite di milioni di tonnellate di raccolti a causa delle infezioni fungine. Alcuni funghi del genere Aspergillus producono un metabolita tossico per la salute umana, le aflatossine. La contaminazione degli alimenti da tali micotossine può avvenire in qualsiasi punto della filiera. Inoltre, essendo termostabili e quindi resistenti a qualsiasi trattamento termico industriale, impongono un maggiore controllo dalla materia prima al prodotto finito. Il regolamento (UE) 165/2010, considerando i rischi per noi consumatori ha esplicitato i massimi limiti tollerabili, espressi in μg/kg, basandosi sulle categorie di prodotto e vietando l’uso di prodotti chimici per la decontaminazione.
Più di 100 paesi hanno restrizioni legislative sul livello massimo di aflatossine negli alimenti e nei mangimi. Le pratiche agronomiche di prevenzione attuali, come controlli con ceppi atossigenici di Aspergillus, metodi di stoccaggio e uso di agenti intrappolanti per bloccare la tossina, risultano però inadeguate.
L’approccio con gli RNAi
In questo contesto uno studio condotto dall’Università dell’Arizona, guidato dalla Dottoressa Monica Schmidt, apre nuove prospettive per la sicurezza alimentare. Basandosi sui risultati ottenuti da studi precedenti che dimostravano scambi genetici (in particolare di RNA) tra pianta ospite e funghi del genere Aspergillus, i ricercatori hanno pensato di usare l’interferenza a RNA (RNAi) per difendere la matrice dalle aflatossine.
Host-Induced Gene Silencing
Gli studiosi hanno introdotto nel mais un DNA ingegnerizzato, tramite una tecnica chiamata HIGS (Host-Induced Gene Silencing), già utilizzata per limitare danni provocati da insetti, nematodi parassiti e crescita di funghi patogeni. L‘interferenza di RNA è un potente strumento per chiarire la funzione genica nelle piante e alterare l’espressione genica per i tratti desiderati. I piccoli RNA sono generalmente realizzati producendo RNA a doppio filamento (dsRNA) in piante transgeniche. Questo può essere introdotto in cellule vegetali con agrobatteri o virus che si replicano attraverso dsRNA. In questo modo, durante l’infezione, l’RNA del mais passato nel fungo interferisce con l’enzima necessario alla produzione dell’aflatossine.
Le aflatossine più dannose
Tra le 20 aflatossine che conosciamo, la B1, B2, G1 e G2 sono le più dannose. Il primo passo nella sintesi delle quattro aflatossine è la formazione di una struttura centrale politetidica dell’acetato, catalizzata da tre enzimi. Due sintasi dell’acido grasso e la polichetide. La polichetide sintasi aflC (pksA) è un enzima unico in questo processo, cosa che lo rende il candidato ideale per l’obiettivo di interferenza a RNA (RNAi); il gene codificante per pksA è stato clonato sia da A.flavus che A.parasiticus. La trasformazione in piante transgeniche è stata mediata da Agrobacterium tumefaciens di una linea ibrida B73 x A118.
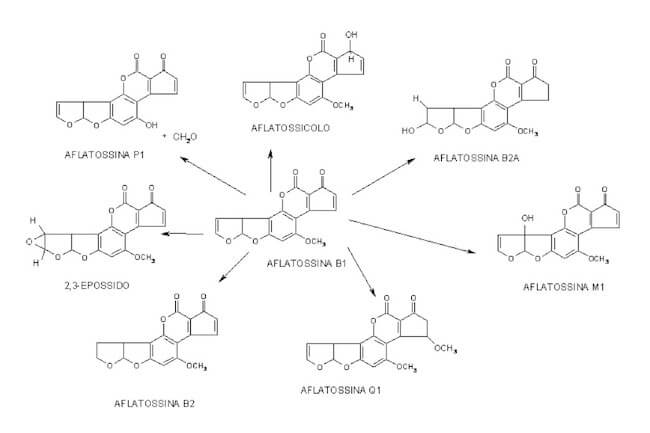
Il mais come sistema modello per gli studi sulle aflatossine
In questo lavoro è stato utilizzato come sistema modello il mais, poiché rappresenta una delle colture più gravemente colpite, ma la tecnica potrà essere estesa a differenti matrici. Dopo un mese dall’infezione con Aspergillus, il mais non trattato presentava livelli di aflatossine tra i 1000 e i 10.000 ppm (parti per milione), mentre nel mais transgenico la tossina non era rilevabile. Le piante “modificate” non hanno mostrato alcun cambiamento, e l’unica differenza evidenziata è stato il blocco della produzione del metabolita tossico.
Conclusioni sul mais e le aflatossine
Ci vorranno ancora molteplici esperimenti per valutare le potenzialità della tecnica e per avere la certezza della mancanza di effetti collaterali, ma i sorprendenti risultati aumenteranno la ricerca e l’attenzione nel settore alimentare per la sicurezza della salute umana.
Veronica Nerino
Fonti:
- Un mais transgenico per combattere le infezioni fungine – Le Scienze
- Aflatoxin-free transgenic maize using host-induced gene silencing-Science Advances
- https://www.microbiologiaitalia.it/micologia/muffe-aflatossina/
- https://www.microbiologiaitalia.it/micologia/aspergillus-flavus-produttore-di-micotossine/