Obiettivo della tecnica
La colorazione lattofenolo cotton blu viene utilizzata in microscopia ottica per l’osservazione specifica degli eumiceti: lieviti, funghi e muffe.
In ambito medico clinico, è usata per la diagnostica delle patologie di origine fungina e viene applicata a strisci di fluidi corporei molto diversi tra loro: espettorati, lavaggi, aghi aspirati, feci, impronte oppure essudati (per approfondire sull’importanza e sulla diffusione delle micosi, si rimanda al nostro articolo).
Permette inoltre di analizzare direttamente la crescita delle colture cellulari in agar, prelevando semplicemente una piccola porzione delle colonie dalla superficie della piastra, ponendola su un vetrino e colorandola poi in un solo passaggio: è infatti una procedura di tipo “one step” semplice da realizzare.
La letteratura scientifica evidenzia tuttavia come questa colorazione a volte non conservi la posizione originale oppure la struttura di conidi, spore ed altri elementi fungini caratterizzanti: se ne sconsiglia pertanto l’utilizzo negli studi di tassonomia in senso stretto.
Che cos’è e come funziona
La colorazione Lattofenolo cotton blu si basa sull’utilizzo di tre sostanze diverse: fenolo, acido lattico e cotton blu.
Il colorante principale (nonché unico, trattandosi di una colorazione semplice) è proprio quest’ultimo: il cotton blu, carico negativamente, si lega infatti selettivamente alla chitina contenuta nella parete cellulare dei miceti (Fig.1).
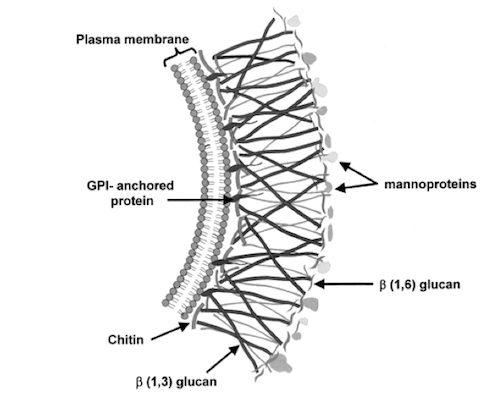
Il fenolo svolge invece funzione battericida, uccidendo eventuali altri microrganismi viventi che si trovino nel campione.
L’acido lattico infine, serve per gonfiare le cellule dei miceti (agisce presumibilmente tramite meccanismi osmotici), aumentandone cosi’ la risoluzione ottica da parte dello strumento.
Sino a non molti anni fa, il protocollo di questa metodica prevedeva il trattamento preliminare del campione da osservare con acido lattico puro o diluito, quindi con il cosiddetto: ”Lattofenolo di Amann” (una miscela di fenolo, acido lattico e glicerina in soluzione acquosa al 20%).
Queste due sostanze prendevano anche il nome di “liquidi di montaggio”, in quanto avevano tra l’altro la funzione di garantire la fissazione ed il mantenimento della colorazione il più possibile.
Fenolo, acido lattico e cotton blu sono tuttavia attualmente disponibili in commercio come un unico preparato in soluzione acquosa: appunto il “Lattofenolo cotton blu” che dà il nome a questa tecnica.
Esso svolge pertanto funzione sia cromogenica che di liquido di montaggio in una sola volta, anche laddove si parta da preparati umidi, evitando cosi’ all’operatore di dover pretrattare il campione come invece si faceva in precedenza.
Nel protocollo riportato di seguito, verrà pertanto illustrato come procedere unicamente col Lattofenolo cotton blu.
In seguito a colorazione, le cellule di lieviti e miceti (nonché le strutture fruttificanti) assumeranno una tonalità blu delicato, mentre lo sfondo si colorerà invece di un azzurro appena percettibile.
Materiale occorrente
(Per questa colorazione, alcuni protocolli attualmente in uso prevedono l’utilizzo del microscopio ad immersione; tuttavia ciò non è assolutamente indispensabile. Si raccomanda di operare sotto cappa e di proteggere le mani indossando dei guanti: il lattofenolo cotton blu è infatti fortemente acido e può risultare tossico per inalazione, contatto con la pelle oppure ingestione. )
- un vetrino per microscopio (con rispettivo coprioggetti);
- lattofenolo cotton blu in soluzione acquosa (in una boccetta munita di contagocce);
- una soluzione di KOH al 10% (in una boccetta munita di contagocce): opzionale (il suo utilizzo è infatti riservato solo al caso in cui si analizzino campioni provenienti da fluidi biologici umani oppure da raschiamento cutaneo);
- ago da microbiologia.
Procedimento
- Porre il campione da analizzare sul vetrino: se si sta utilizzando questa colorazione per osservare la morfologia dei miceti, esso non dovrà essere strisciato per non compromettere la struttura dei miceli. In caso contrario, come accade se si desidera ad esempio analizzare dei fluidi biologici, è invece necessario effettuare lo striscio.
(Diversamente da quanto previsto da altre colorazioni utilizzate in microscopia ottica, in questa tecnica il campione NON dev’essere fissato al calore ma va semplicemente lasciato asciugare all’aria, laddove ovviamente sia necessario).
Se il campione deriva da fluidi biologici umani:
- utilizzando l’ago, mescolare il campione con una o al massimo due gocce di soluzione di KOH.
Altrimenti (oppure di seguito):
- aggiungere due gocce (non di più) di lattofenolo cotton blu;
- Coprire con attenzione col vetrino coprioggetti, premendo delicatamente per ottenere un preparato sottile ed evitare la formazione di bolle d’aria;
- Lasciar agire la colorazione in questo modo per due minuti abbondanti.
Il vetrino cosi’ trattato è ora pronto per l’osservazione al microscopio.
Osservazione del vetrino
Si consiglia di analizzare il preparato su vetrino ad un ingrandimento di 100X mantenendo una bassa illuminazione.
Quindi si salirà gradualmente con l’ingrandimento sino al 430X (o comunque al massimo consentito dallo strumento in dotazione).
Se nel campione sono presenti dei miceti, essi appariranno colorati di una tonalità in blu più o meno intensa, ben visibili su di uno sfondo azzurro pallido (Fig.2).
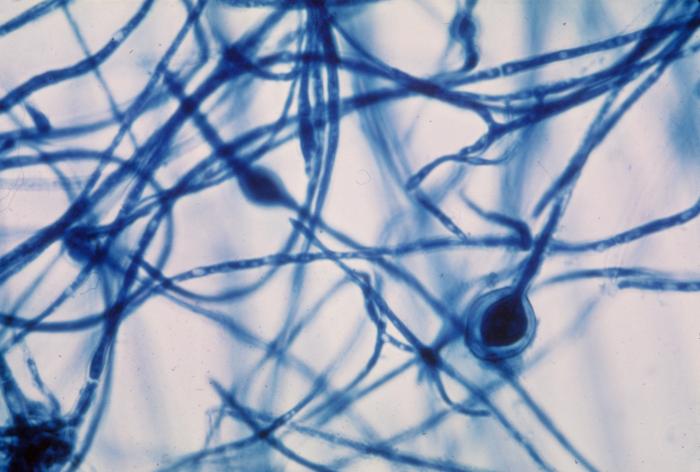
Il lattofenolo cotton blu non permette d’identificare eventuali altri microrganismi che siano eventualmente presenti, ma assicura un ottimo livello di risoluzione di tutte le principali strutture fungine (Fig.3).

In caso di utilizzo di questa colorazione a scopi diagnostici, l’assenza di elementi fungini riconoscibili implica ovviamente un risultato negativo per gli stessi.
Se si sospetta che nel campione siano presenti anche batteri riconducibili alle specie “gram” oppure di altro tipo, per poterli identificare occorrerà tuttavia ricorrere ad un’altra colorazione oppure ad una tecnica diagnostica diversa.
Fonti utilizzate
Sitografia di riferimento
http://www.apsi.it/public/ufiles/smi/tp39_2_1_it_150902.pdf
Scheda tecnica del lattofenolo cotton blu della ditta Merck:
https://catalog.hardydiagnostics.com/cp_prod/Content/hugo/LactophenolCottonBlStn.Htm
Crediti per le immagini
Immagine in evidenza (e figura 3):
http://www.pharmamicroresources.com/2017/10/drug-quality-and-security-act-and.html
Figura 1:
Figura 2:
Spero di non sbagliarmi, ma la foto n. 3 mi ricorda più una specie del genere Penicillium o simile che non del gen. Aspergillus.