Oggi parliamo dei plasmodi “minori” che causano la malaria nell’uomo: Plasmodium malariae, Plasmodium ovale, Plasmodium knowlesi, Plasmodium cynomolgi e Plasmodium simium. Queste specie sono meno frequenti rispetto a Plasmodium falciparum e Plasmodium vivax, e alcune di esse sono delle zoonosi.
Caratteristiche generali
I plasmodi della malaria sono parassiti intracellulari obbligati che necessitano di due ospiti: un vertebrato (l’uomo o le scimmie) e un invertebrato vettore (le zanzare del genere Anopheles).
Il Plasmodium malariae è presente nell’Africa subsahariana, in Asia e nelle Americhe ma solitamente con una bassa prevalenza. Invece il Plasmodium ovale (che presenta due sottospecie, curtisi e wallikeri) è presente prevalentemente nell’Africa subsahariana e sporadicamente in Asia.
Le altre tre specie sono zoonosi. Il Plasmodium knowlesi e il Plasmodium cynomolgi sono trasmessi dai macachi nel Sudest asiatico, mentre il Plasmodium simium dalle scimmie della foresta atlantica brasiliana.
In generale le infezioni provocate da queste specie sono di solito meno virulente rispetto a quelle provocate da P. falciparum, ma alcuni aspetti della loro biologia, epidemiologia e patologia rimangono da chiarire.
Filogenesi
| Dominio | Eukaryota |
| Regno | Protista |
| Sottoregno | Chromalveolata |
| Phylum | Apicomplexa |
| Classe | Aconoidasida |
| Ordine | Haemosporida |
| Famiglia | Plasmodiidae |
| Genere | Plasmodium |
| Specie | malariae, ovale, knowlesi, simium, cynomolgi |
| Sottospecie | ovale curtisi, ovale wallikeri |
Ciclo vitale
I plasmodi della malaria umana si moltiplicano asessualmente (ciclo “schizogonico”) nei primati e sessualmente (ciclo “sporogonico”) nella zanzara (Figura 1).
Il ciclo inizia con gli sporozoiti inoculati dalla zanzara che invadono il fegato. Dal fegato i parassiti infettano gli eritrociti, iniziando il ciclo schizogonico che porta alla formazione dei gametociti. Questi ultimi vengono ingeriti dalla zanzara, nel cui stomaco si generano i gameti. Quindi i gameti si uniscono a formare lo zigote e poi l’oochinete, che successivamente penetra la parete dello stomaco dell’insetto maturando in oociste. Nelle oocisti nascono gli sporozoiti, che migrano nelle ghiandole salivari della zanzara. Quindi la zanzara con gli sporozoiti ricomincerà il ciclo quando pungerà un nuovo ospite.
In aggiunta, il Plasmodium ovale (come P. vivax) produce ipnozoiti dormienti nel fegato che si possono riattivare dopo mesi o anni iniziando un nuovo ciclo schizogonico.

Morfologia strutturale
Nel sangue i plasmodi attraversano quattro stadi di sviluppo.
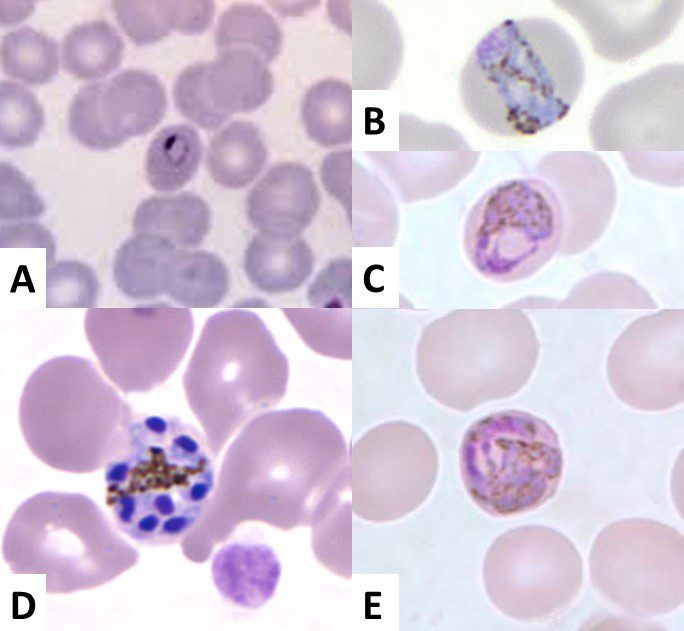
Plasmodium malariae (Figura 2)
- Gli anelli hanno un grosso nucleo e un citoplasma compatto.
- I trofozoiti hanno un citoplasma compatto, e mostrano spesso forme cosiddette a “banda” o “cestino” con evidente pigmento malarico.
- Gli schizonti contengono da 6 a 12 merozoiti. I merozoiti assumono spesso una caratteristica forma a “rosetta” che circonda il pigmento malarico accumulato al centro.
- I gametociti, tondeggianti, occupano di solito l’intero volume dell’eritrocita e hanno il pigmento malarico diffuso.
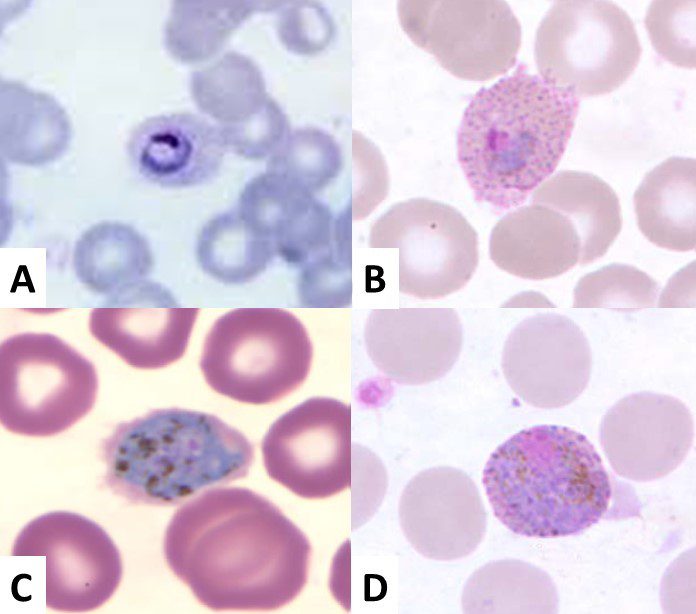
Plasmodium ovale (Figura 3)
- Gli anelli, con un grosso nucleo, hanno un citoplasma compatto.
- I trofozoiti hanno un citoplasma compatto o leggermente irregolare, e le granulazioni di Shuffner possono apparire sulla superficie dell’eritrocita (come in P. vivax).
- Gli schizonti, con 6-14 merozoiti, e i gametociti presentano le stesse caratteristiche di quelli di P. vivax.
Plasmodium knowlesi
- Gli anelli hanno 1-2 nuclei e il citoplasma è delicato.
- I trofozoiti, gli schizonti (con 16 merozoiti) e i gametociti hanno una morfologia sovrapponibile a quella di P. malariae.
Plasmodium cynomolgi e Plasmodium simium
Gli stadi di sviluppo di Plasmodium cynomologi e simium sono indistinguibili da quelli di P. vivax.
Per tutte le specie trattate, le oocisti e gli sporozoiti nella zanzara hanno le stesse caratteristiche degli altri plasmodi (vedi P. vivax).
Patogenesi
Dal punto di vista clinico la malaria si manifesta con mialgie, mal di testa, vomito, diarrea, eccessiva sudorazione, brividi e picchi di febbre (parossismo malarico). La febbre coincide con la rottura dei globuli rossi e il rilascio dei parassiti e dei loro cataboliti nel sangue. Nelle infezioni da Plasmodium malariae i picchi febbrili si verificano approssimativamente ogni 72 ore (febbre quartana). Invece, il Plasmodium ovale causa picchi ogni 48 ore (febbre terzana). Infine, il parossismo malarico in Plasmodium knowlesi ha un ciclo di sole 24 ore.
Le infezioni da Plasmodium malariae o Plasmodium ovale tendono a essere meno gravi rispetto a quelle causate da P. falciparum, ma per entrambe le specie sono stati descritte complicazioni e casi fatali. Al contrario, Plasmodium knowlesi provoca un decorso simile (e pertanto grave) a P. falciparum.
Infine, non esistono ancora informazioni certe sulla gravità delle infezioni causate da Plasmodium cynomologi o Plasmodium simium.
Metodi di identificazione
La diagnosi di malaria si fonda soprattutto sull’osservazione microscopica dei parassiti in strisci di sangue sottili o a goccia spessa, colorati con il metodo di Wright-Giemsa. Tuttavia, la colorazione di Giemsa è consigliata per visualizzare meglio le granulazioni di Shuffner (in Plasmodium ovale).
Le caratteristiche diagnostiche più importanti delle specie qui trattate sono:
- Le infezioni multiple sono presenti in ovale e knowlesi, ma assenti in malariae.
- Gli eritrociti infetti sono di dimensioni normali o ridotte in malariae e knowlesi, mentre sono spesso più grandi e ovali con le estremità che possono apparire frastagliate (fimbriate) in ovale.
- La presenza delle forme a banda o a cestino (trofozoiti) e a rosetta (schizonti) in malariae e knowlesi.
- La presenza delle granulazioni di Shuffner in ovale (caratteristica condivisa con P. vivax).
- Gli stadi di Plasmodium cynomolgi e simium sono indistinguibili rispetto a P. vivax.
Per Plasmodium knowlesi, cynomolgi e simium risulta quindi fondamentale la diagnosi tramite PCR unita alle informazioni sulla provenienza o i luoghi visitati recentemente dal paziente.
I test immunocromatografici rapidi usati per rilevare gli antigeni o gli enzimi di P. falciparum o vivax non consentono di diagnosticare in modo specifico gli altri plasmodi.
I test sierologici rilevano solo l’esposizione pregressa ai plasmodi ma non consentono di diagnosticare un’infezione in corso.
Terapia
Il trattamento farmacologico della malaria varia a seconda della gravità dell’infezione e della presenza di resistenza alla clorochina nei parassiti:
- Per le infezioni non complicate, si consigliano clorochina/idrossiclorochina solfato oppure chinina solfato (con doxiciclina o tetraciclina) o atovaquone/proguanil, se si sospetta clorochina-resistenza (Papua Nuova Guinea, Indonesia).
- Per le infezioni gravi, si consiglia artesunato EV, seguito da uno dei seguenti: artemetere/lumefantrina, atovaquone/proguanil, doxiciclina, o clindamicina (nelle donne in gravidanza).
- In aggiunta, primachina o tafenochina vengono utilizzate per eliminare gli ipnozoiti di Plasmodium ovale nel fegato.
Prevenzione
La prevenzione della malaria da parte dei viaggiatori in aree endemiche si basa sull’utilizzo di zanzariere e repellenti contro le zanzare Anopheles e sulla chemioprofilassi. Quest’ultima fa uso di farmaci che vanno scelti a seconda del Paese visitato, tipo di viaggio e tempo di permanenza.
Epidemiologia dei plasmodi zoonotici
Il Plasmodium knowlesi è un parassita delle scimmie del genere Macaca. Malgrado la maggior parte delle infezioni risultino da spillovers dalle scimmie all’uomo nelle zone rurali e di foresta, questo parassita viene anche trasmesso da uomo a uomo. I macachi ospitano anche il Plasmodium cynomolgi, e coinfezioni knowlesi/cynomologi sono frequenti in questi primati (e sembrerebbe anche nell’uomo).
Casi di Plasmodium simium nell’uomo sono stati recentemente riportati nelle zone di foresta atlantica nel Brasile meridionale. Questo parassita infetta diversi primati incluse le scimmie urlatrici (generi Alouatta e Brachyteles) e le scimmie cappucine (generi Cebus e Sapajus).
Le infezioni da plasmodi zoonotici sono legate ad attività umane (incluso il turismo) in aree abitate da scimmie e da vettori che si alimentano sui primati. La loro biologia è ancora largamente sconosciuta.
Fonti
- CDC DPDX
- ISS
- MSDS
- Sutherland CJ. Persistent Parasitism: The Adaptive Biology of Malariae and Ovale Malaria. Trends Parasitol. 2016;32(10):808-819. doi:10.1016/j.pt.2016.07.001
- Anstey NM, Grigg MJ. Zoonotic Malaria: The Better You Look, the More You Find. J Infect Dis. 2019;219(5):679-681. doi:10.1093/infdis/jiy520
- Brasil P, Zalis MG, de Pina-Costa A, et al. Outbreak of human malaria caused by Plasmodium simium in the Atlantic Forest in Rio de Janeiro: a molecular epidemiological investigation. Lancet Glob Health. 2017;5(10):e1038-e1046. doi:10.1016/S2214-109X(17)30333-9