Utilizzo
Il PCA agar (Plate Count Agar; Fig.1) è un terreno di coltura per la determinazione della carica microbica totale (microrganismi vivi e aerobi) in campioni alimentari, acque reflue e in campioni clinici.
Il numero di batteri può essere espresso in CFU/g (Unità Formanti Colonia/g) per campioni solidi e in CFU/ml per campioni liquidi.

Preparazione e composizione
Gli ingredienti e le dosi necessarie per la preparazione del PCA sono i seguenti (Tabella 1):
| Ingredienti | Quantità (g/l) |
| Triptone | 5,0 |
| Estratto di lievito | 2,5 |
| Destrosio (glucosio) | 1,0 |
| Agar | 15,0 |
La formula in questione è quella consigliata per ottenere una performance ideale del terreno con pH finale di 7,0 +/- 0,2.
Per preparare il PCA agar è necessario sospendere i 23,5 g di polvere in 1000 ml di acqua deionizzata.
Il tutto deve essere bollito e messo in agitazione fino alla completa dissoluzione delle polveri.
Successivamente, il terreno deve essere autoclavato a 121°C per 15 minuti e fatto raffreddare a 45-50°C prima di essere colato in piastre Petri sterili.
Metodo
Il PCA agar è stato formulato per la prima volta da Buchbinder e collaboratori e il suo utilizzo è attualmente consigliato da svariati enti per la sicurezza alimentare come la FDA (Food and Drug Administration).
L’azoto e il carbonio per la crescita microbica sono forniti dal triptone, dagli amminoacidi a catena lunga e da altri nutrienti essenziali, mentre, l’estratto di lievito fornisce l’importante vitamina B.
E’ possibile utilizzare il terreno con semina classica (con l’utilizzo di un’ansa sterile) oppure, come raccomandato, per inclusione (Pour Plate Technique; Fig.2).
In questo secondo caso è necessario preparare diverse diluizione del campione di partenza e ognuna di queste sarà addizionata ad una piastra Petri.
Ad ogni piastra si aggiunge poi l’agar sterile che andrà omogeneizzato, tramite delicati movimenti circolatori, con il resto del campione.
Le piastre vanno poi incubate per 3 giorni tra i 20 e i 30°C. Sarà poi necessario scegliere la piastra con numero leggibile di colonie (tra 25-250), numero che andrà poi moltiplicato per il fattore di diluizione per ottenere la stima più attendibile della carica batterica totale del campione di partenza.

Risultati e immagini
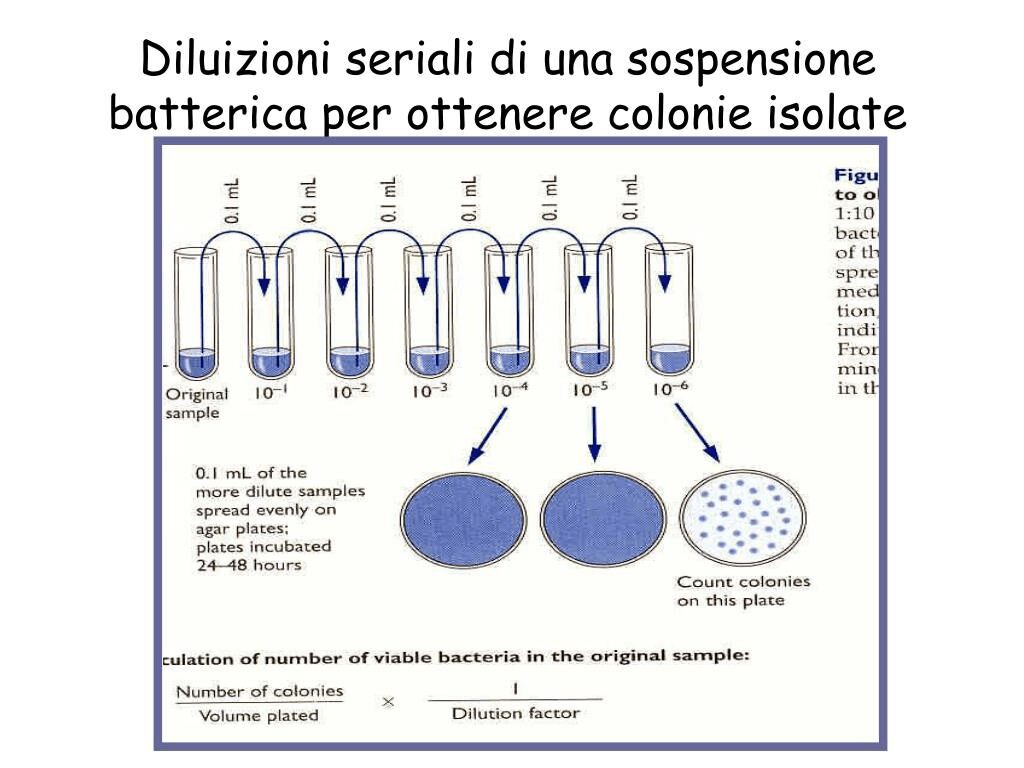
Per il conteggio dei microrganismi tramite l’utilizzo del PCA agar si fa quindi riferimento, nella maggior parte dei casi, al metodo delle diluizioni seriali di una sospensione batterica (Fig.3).
Per farlo si utilizza la seguente formula:
(Numero di colonie/Volume di inoculo) x (1/Fattore di diluizione).
Limitazioni
Il PCA agar è utile per il suo scopo, ovvero la stima della carica microbica totale di un campione, ma non supporta la crescita dei microrganismi fastidiosi.
Controllo qualità
Per il controllo qualità del PCA agar devono essere presi in considerazione diversi parametri tra cui:
- Aspetto della polvere: dal crema al giallo, polvere libera.
- Aspetto del terreno solido: colore giallo chiaro leggermente opalescente.
- Gelling: aspetto fermo, confrontabile con un 1,5% di gel di agarosio.
- pH: tra 6,80 e 7,20.
- Risposta all’inoculo: crescita visibile dopo 18-48 h di incubazione a 35-37°C.
Nello specifico, per il controllo qualità si possono seguire i suddetti parametri (Tabella 2):
| Microrganismo | Inoculo (CFU) | Crescita |
| Bacillus subtilis subsp. spizizenni ATCC 6633 | 50-100 | vigorosa (>=70%) |
| Enterococcus faecalis ATCC 29212 | 50-100 | vigorosa (>=70%) |
| Escherichia coli ATCC 25922 | 50-100 | vigorosa (>=70%) |
| Lactobacillus casei ATCC 9595 | 50-100 | vigorosa (>=70%) |
| Staphylococcus aureus subsp. aureus ATCC 25923 | 50-100 | vigorosa (>=70%) |
| Streptococcus pyogenes ATCC 19615 | 50-100 | vigorosa (>=70%) |
Fonti
- Himedia Scheda Tecnica;
- Biokar Diagnostics;
- Microbe Notes;
- Corso di microbiologia clinica;
- Buchbinder L., Baris Y., Aldd E., Reynolds E., Dilon E., Pessin V., Pincas L. and Strauss A., 1951, Publ. Hlth. Rep., 66:327;
- Baird R.B., Eaton A.D., and Rice E.W., (Eds.), 2015, Standard Methods for the Examination of Water and Wastewater, 23rd ed., APHA, Washington, D.C.
Crediti immagini
- Figura:
- 1: no.frederiksen.eu;
- 2: ResearchGate;
- 3: corso di microbiologia clinica;
- In evidenza: no.frederiksen.eu.