Virus Chikungunya (CHIKV)
Il virus Chikungunya (Figura 1) è un virus a RNA a singolo filamento positivo, appartenente alla famiglia delle Togaviridae e al genere degli Alphavirus. La trasmissione da un individuo all’altro avviene per mezzo delle zanzare del genere Aedes. È diffuso prevalentemente nell’emisfero orientale e, dal 2013, ha infettato milioni di persone nel solo continente americano.
I sintomi della patologia, causata dall’infezione da parte del virus, sono altamente variabili. Circa la metà delle persone infettate risulta asintomatica, alcuni sviluppano febbre e dolori articolari che durano all’incirca una settimana, il 10-30% dei soggetti infettati sviluppa artrite debilitante che persiste per mesi e addirittura anni. Ad oggi non sono ancora conosciute le ragioni per cui la gravità della malattia sia così variabile tra un individuo e l’altro.
Virus Chikungunya e microbiota: esiste una correlazione?
Un gruppo di ricercatori della Washington University School of Medicine di St. Louis ha individuato una correlazione, nei topi, tra gravità della malattia e microbioma intestinale.
Il microbiota svolge differenti e importanti compiti nell’organismo, primo fra tutti la digestione. Infatti si occupa di trasformare le sostanze che ingeriamo in vitamine e altri sottoprodotti, che vengono assorbiti dalle cellule intestinali. Questi stessi composti possono essere anche metabolizzati – dallo stesso microbiota – per regolare l’infiammazione e la risposta immunitaria.
Proprio per questo, numerosi studi, ad oggi, evidenziano l’importanza del microbiota non solo per l’intestino, ma per l’intero organismo. Studi simili a quello analizzato in questo articolo, condotti sempre su modelli murini, hanno dimostrato come topi privi di microbiota dessero vita a risposte immunitarie – innate e adattative – difettive nei confronti di virus come virus dell’influenza e virus dell’epatite B.
E nel caso del virus Chikungunya? Per valutare cosa accade, in seguito ad infezione, i ricercatori hanno utilizzato tre gruppi di modelli murini: topi privi di microbiota, cresciuti in un ambiente sterile sin dalla nascita, topi con microbiota difettivo, poichè trattati con un cocktail di ampicillina e vancomicina (due antibiotici comunemente utilizzati) e topi controllo.
Dopo aver infettato i topi con il virus, i ricercatori hanno osservato come il virus si fosse moltiplicato rapidamente nei topi con microbiota alterato, e avesse raggiunto più facilmente la circolazione sanguigna e, da lì, il resto dell’organismo.
Microbiota e risposta immunitaria compromessa
Questo accade perché i topi con microbiota difettivo hanno delle cellule del sistema immunitario, le cellule dendritiche plasmacitoidi, compromesse. Queste cellule, in condizioni normali, esprimono prevalentemente il recettore TLR7 che riconosce gli RNA virali a singolo filamento. Dopo aver legato l’acido nucleico virale, attivano una via di segnalazione che porta ad una risposta immunitaria dipendente dall’interferone di tipo I (IFN). Nel caso in cui queste cellule sono compromesse, viene meno la via di segnalazione e si ha minore produzione di IFN. In questo modo, i monociti circolanti esprimono meno geni IFN-dipendenti e favoriscono l’ingresso del virus nelle cellule (Figura 2).
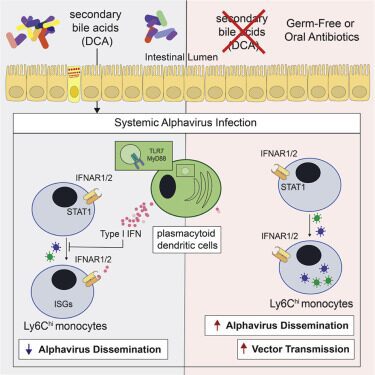
L’importanza di Clostridium scindens e degli acidi biliari
Clostridium scindens (Figura 3) è un batterio comunemente presente nel microbiota umano, ma non in quello murino. Il suo ruolo nell’uomo è quello di modificare gli acidi biliari (BA) prodotti dal fegato in acidi biliari secondari. In particolare, un ruolo rilevante è quello dell’acido desossicolico (DCA), che deriva dall’acido colico, poiché influenza la risposta immunitaria. Infatti, questo stimola le cellule dendritiche plasmacitoidi, favorendo la produzione di IFN.
I ricercatori hanno deciso di sfruttare le proprietà di questo batterio a loro vantaggio. Dopo l’infezione, hanno introdotto, in topi con microbiota difettivo, il batterio e hanno ottenuto degli ottimi risultati. In questo modo, infatti, hanno ripristinato la produzione di IFN e la risposta immunitaria in grado di bloccare efficacemente la diffusione del virus. Non solo, lo stesso risultato è stato ottenuto anche attraverso la semplice somministrazione di acido desossicolico.
Il ruolo del microbiota nella trasmissione del virus
Sapendo che un microbiota difettivo promuove una maggiore diffusione del virus nella circolazione sanguigna, diventa maggiore anche la probabilità di trasmissione. Il virus Chikungunya viene trasmesso attraverso zanzare, che si nutrono di sangue, e, se questo è ricco di particelle virali, sarà più facile la trasmissione. Per verificare questo i ricercatori hanno infettato tre gruppi di topi: topi trattati con antibiotici per eliminare i batteri intestinali, topi trattati con antibiotici e a cui, successivamente, veniva somministrato C. scindens, topi con un normale microbiota.
Dopo un giorno dall’infezione, i ricercatori hanno prelevato il sangue dai topi dei tre gruppi per offrirlo, come nutrimento, alle zanzare. Il risultato? Più della metà delle zanzare che si erano nutrite del sangue di topi privi di microbiota si era infettata ed era in grado di trasmettere il virus. Al contrario, meno di un terzo delle zanzare che avevano ricevuto sangue da topi trattati con C. scindens o con microbiota normale presentava il virus.
Prospettive future
Questo studio ha evidenziato come un microbiota sano sia molto importante come limitatore di diffusione di Alphavirus nel nostro organismo. Probabilmente è proprio la differenza di composizione microbica tra gli indiviui alla base dell’elevata variabilità di sintomi che caratterizzano la patologia causata dal virus Chikungunya.
Sicuramente, oltre a C. scindens, nel nostro microbiota ci sono anche altri batteri in grado di svolgere le stesse funzioni. Questi potrebbero essere usati in futuro per la creazione di un probiotico che possa riequilibrare il microbiota alterato, ridurre al minimo la malattia nei soggetti infettati e ridurre la diffusione del virus nella comunità.
Emanuela Pasculli
Fonti
- “Gut Microbiome Protects against Severity of Mosquito-Borne Viral Disease” (15 Luglio 2020). Estrapolato da https://www.genengnews.com/topics/omics/gut-microbiome-protects-against-severity-of-mosquito-borne-viral-disease/;
- Winkler, Emma S., et al. “The Intestinal Microbiome Restricts Alphavirus Infection and Dissemination through a Bile Acid-Type I IFN Signaling Axis.” Cell (2020);
- Kawasaki, Takumi, and Taro Kawai. “Toll-like receptor signaling pathways.” Frontiers in immunology 5 (2014): 461.